ブデソニド・ホルモテロール
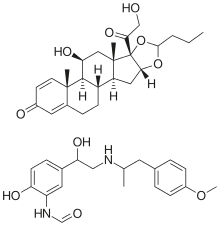 | |
| 成分一覧 | |
|---|---|
| ブデソニド | 副腎皮質ステロイド |
| ホルモテロール | 長時間作用型β刺激薬 |
| 臨床データ | |
| 販売名 | シムビコート |
| 胎児危険度分類 |
|
| 法的規制 |
|
| データベースID | |
| CAS番号 |
|
| ATCコード | R03AK07 (WHO) |
ブデソニド・ホルモテロール(Budesonide/Formoterol)は、気管支喘息および慢性閉塞性肺疾患(COPD)の治療に用いられるステロイドとアドレナリンβ刺激薬の配合剤。
アストラ・ゼネカが同社の吸入ステロイド喘息治療剤ブデソニドに長時間作用型気管支拡張薬であるホルモテロールを配合し、同時に吸入できるようにした合剤で、日本では、2009年にアステラス製薬とアストラ・ゼネカが、同剤の日本での販売及び共同販促に関する契約を締結し、アステラス製薬販売でシムビコートタービュヘイラー(EU&USA:Symbicort)として2010年1月に発売されたが、10年間の契約満了に伴い、2019年7月31日以降はアストラ・ゼネカが単独で流通・販売、情報提供活動を行っている。後発品として、ブデホル吸入粉末剤がある。
効能・効果
[編集]- 気管支喘息(維持療法と頓用吸入)[1]
- 慢性閉塞性肺疾患(COPD)(増悪時の急性期治療には使用できない。)
- スウェーデンでは喘息発作時の頓用吸入にも適応を持つ。日本でも2012年6月にSMART療法が認可された。
禁忌
[編集]下記の患者には禁忌である。
- 有効な抗菌剤の存在しない感染症、深在性真菌症の患者
- 製剤成分に対して過敏症(接触性皮膚炎を含む)の既往歴のある患者
- 結核性疾患の患者(原則禁忌)
副作用
[編集]治験時の副作用は、気管支喘息の維持療法:18.5%、喘息維持療法中の頓用吸入:3.9%、COPDの維持療法(国内+海外):7.8%であった。主な副作用は、振戦、血中カリウム減少、肺炎、嗄声、筋痙攣、動悸、咽喉頭疼痛、口腔カンジダ症、動悸であった[2]。
重大な副作用としては、アナフィラキシー(1%未満)と重篤な血清カリウム値の低下(1%未満)が記載されている。
概要
[編集]2000年にスウェーデンではじめて承認されて以降、世界100カ国以上で気管支喘息治療薬として承認されている。アドエアに比べ粒子径が小さく、細小気管支へも到達することを特徴のひとつとしている。
薬理
[編集]ホルモテロールはアドレナリンβ2受容体刺激薬であるが、吸入にその効果がすみやかにあらわれること、そして長時間持続することを特徴としている。吸入1分後からSABA(短時間作用性吸入β2刺激薬)であるサルブタモールと同様の効果を示す[3]。
またフルチカゾン250µg・サルメテロール50µg(製品名アドエア250)との比較では、吸入直後1分間から30分間までを通じて1秒率はシムビコートが優っていた[4]。
出典
[編集]- ^ 長期管理に用いるICS/LABA配合剤を、発作時に追加投与して急性症状を緩和する治療法をSMART療法と呼ぶ。
- ^ “シムビコートタービュヘイラー30吸入/60吸入” (2015年1月). 2016年6月28日閲覧。
- ^ Jonkers RE, Bantje TA, Aalbers R (2006). “Onset of relief of dyspnoea with budesonide/formoterol or salbutamol following methacholine-induced severe bronchoconstriction in adults with asthma: a double-blind, placebo-controlled study.”. Respir Res 7: 141. doi:10.1186/1465-9921-7-141. PMC 1713239. PMID 17144916.
- ^ van der Woude HJ, Boorsma M, Bergqvist PB, Winter TH, Aalbers R (2004). “Budesonide/formoterol in a single inhaler rapidly relieves methacholine-induced moderate-to-severe bronchoconstriction.”. Pulm Pharmacol Ther 17 (2): 89-95. doi:10.1016/j.pupt.2003.11.001. PMID 15123230.