ベンゾジアゼピン離脱症候群
| ベンゾジアゼピン離脱症候群 | |
|---|---|
| 概要 | |
| 診療科 | 精神医学 |
| 分類および外部参照情報 | |
| ICD-10 | F13.3 |
ベンゾジアゼピン離脱症候群(ベンゾジアゼピンりだつしょうこうぐん、Benzodiazepine withdrawal syndrome)は、ベンゾジアゼピン系薬の服用により身体的依存が形成されてから、用量を減量するか、断薬することによって生じる一連の離脱症状。その症状は頻繁に深刻な睡眠障害、易刺激性、不安と緊張の増加、パニック発作、手の震え、発汗、集中困難、混乱と認識困難、記憶の問題、吐き気やむかつき、体重減少、動悸、頭痛、筋肉の痛みと凝り、多くの知覚変化、幻覚、てんかん発作、精神病[1]、インフルエンザ様症状[2]、また自殺[3]といった特徴がある(#兆候と症状節の完全な一覧を参照)。さらに、これらの症状は単純に直線的に着々と減少するのではなく、重症度が日々あるいは週ごとに変化し、一進一退することで有名である[4][5]。
発生する症状は、潜在的に深刻な状態であり、複雑でしばしば長期化しうる[6][7]。アルコールやバルビツール酸系の離脱症候群と、ベンゾジアゼピン系の離脱症状は類似している[8]。長期間の使用は、3か月以上の日常的な使用と定義され[9]、その患者らに離脱症状が出現する割合は15%から44%の間だと推定されている[10]。このような使用は依存のリスクの増加[11]、用量の増加や効果の減少、特に高齢者における事故と転倒のリスクの増加[12]、また認知的[13]、神経学的および知的な障害[14]に結びつくため望ましくない。短時間作用型の睡眠薬の使用は入眠障害には有効だが、離脱の影響によって睡眠の後半は悪化する[15]。
症状の重症度は、重篤なものになりえ[6]、特に長期的な使用や高用量からの離脱、突然あるいは急速すぎる減量では、発作のような致命的なものになる[16]。しかし徐々の減量や、また比較的低用量・短期的な使用からであっても[17](動物実験では1回の大量投与の後でも[18][19])重篤な離脱反応が起きることもある。離脱時には、致命的となる可能性のある振戦せん妄の兆候の評価が必要である[20]。患者の少数では遷延性離脱症候群が起こり、ベンゾジアゼピンの中止後も急性症状の下位の水準で数カ月あるいは数年にわたって持続する可能性がある。服用量をゆっくり徐々に減少させることによって遷延性離脱症候群の発症の可能性を最小限にすることができる。[21]
発生機序は、慢性的なベンゾジアゼピンへの暴露により、薬の影響を弱めようと神経系が適応し、耐性と身体依存が生じることによる[22]。治療用量内であっても長期的な使用により、服薬と服薬との間において離脱症状が出現することがある[23]。この状態で投与が中止あるいは減量されれば、離脱症状が生じる可能性があり、これは体の生理的適応が逆転するまで残存しうる[24]。これらの反跳性症状は、当初に薬を服薬することとなった症状と同様か、もしくは退薬症状である[25]。重篤な症例では、離脱反応は躁病、統合失調症、発作性疾患(特に高用量)のような、精神医学的なまた医学的に重篤な状態に似ていることがある[26]。治療者が退薬症状を見分けられなければ、ベンゾジアゼピンを再服用する誤った根拠となり、これは離脱の失敗とベンゾジアゼピンの再投薬へと戻ることになり、それはしばしば高用量となってしまう[26]。
離脱症状の啓もう、患者別の離脱重症度に沿った漸減計画、ベンゾジアゼピン離脱支援団体への紹介や支援は、すべて離脱の成功率を高める[27][28]。しかしながら、ベンゾジアゼピンの長期使用者の場合は彼らの意思に反しての離脱を強制すべきではない[6]。
| ベンゾジアゼピン |
|---|
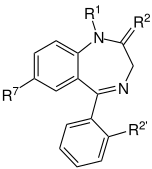
|
| ベンゾジアゼピン系の核となる骨格。 「R」の表記部分は、ベンゾジアゼピンの異なる 特性を付与する側鎖の共通部位である。 |
| ベンゾジアゼピン |
| ベンゾジアゼピンの一覧 |
| en:Benzodiazepine overdose |
| ベンゾジアゼピン依存症 |
| ベンゾジアゼピン薬物乱用 |
| ベンゾジアゼピン離脱症候群 |
| ベンゾジアゼピンの長期的影響 |
歴史とガイドライン
[編集]


1960年に初のベンゾジアゼピンであるクロルジアゼポキシドがホフマン・ラ・ロシュ社より市場に出され、日本ではコントール、海外ではLibriumの商品名で知られる。そのすぐ後にジアゼパム(セルシン、Valium)が登場した。そしてすぐ後の1961年には、ホリスターらが1〜7か月の間でクロルジアゼポキシドを使用した入院患者において、不眠症から痙攣発作までの離脱症状を報告した[30]。こうした1960年代の初期の報告は、治療用量よりも高用量で長期的に使用した後の中止により生じたものであったが、後に治療用量でも離脱症状が生じることをいくつかの試験が示していった[31]。
世界保健機関は、1961年に公布された麻薬を規制する麻薬に関する単一条約の後に登場した、新たな向精神薬の乱用を懸念した。1971年には向精神薬に関する条約が公布され、ベンゾジアゼピン系ではクロルジアゼポキシドやジアゼパムを含めた20種以上が指定され、後に登場したものでも国際的に乱用されたものについては追加されていった。アメリカでは1975年には、クロルジアゼポキシドやジアゼパムは規制物質法の管理下に置かれた[32]。
ロシュ社は1980年まで非依存性であると主張し続けたが、今日の医薬品の添付文書は明らかに乱用や身体依存への注意を促している[32]。日本の医薬品添付文書でも同様に依存と、不眠から発作までを含めた離脱症状に注意し、慎重な減量を促している。1980年代にイギリスのヘザー・アシュトンによるベンゾジアゼピン系の離脱専門診療所が開設される。1988年には、英国医薬品安全委員会は国内の医師に処方ガイドラインを送付し、ベンゾジアゼピン系の処方は4週間以内にすべきとした[33]。
1996年には、世界保健機関がベンゾジアゼピンの合理的な使用に関するガイドラインを出版し、処方は30日以下にすべきであるとした[34]。この報告書では、具体的な離脱の方法としてヘザー・アシュトンの論文を出典とし、全体の量の50%は数日で減量できるが、次の25%は数週間までを必要とすることがあり、最後の残りの25%は6カ月までを要する場合があり、まれに入院を要し、個々人に沿った管理の必要性が示されている[35]。また半減期が短い薬剤は、長時間型に置換することにも言及している[35]。
2002年には、ヘザー・アシュトンによる『ベンゾジアゼピン-それはどのように作用し、離脱するにはどうすればよいか』(Benzodiazepines: How They Work and How to Withdraw)[6]がオンラインで入手可能となる。邦訳は2012年8月に公開され、これは出典論文が省略され、新たな付記も存在する。内容としては、離脱を管理するために長時間型のジアゼパムに置換し、ジアゼパムが10mgになるまで週あたり残りの10%を減量するといった、1996年の世界保健機関によるものよりさらにペースを落とした方法が紹介されている。
国内外の診療ガイドラインを比較すれば以下のようになる。
2012年の日本うつ病学会のうつ病の診療ガイドラインは、そもそも軽症のうつ病では安易な薬物療法の選択を避ける姿勢が優先されているが、薬物療法は抗うつ薬を基本とし、ベンゾジアゼピンを併用するとしても単剤かつ必要最小限とし、常用量依存に注意すべきとしている[36]。
2013年の日本睡眠学会による診療ガイドラインでは、多剤併用によりさらなる有効性があるというよりは副作用の頻度を高めるのでできるだけ避け、臨床常⽤量を超える使用は絶対に避け、休薬する場合に複数の離脱症状を呈する患者は20〜40%とされ、漸減法などを用いて慎重に減量し、例として1〜2週間ごとに1/4錠ずつ減量し問題がなければこのように続行するなど時間をかけることが必要とされている[37]。さらに、長期間、高用量、多剤併用が離脱症状の危険因子であり、2錠以上あるいは2種類以上である場合には緩やかな減量が必要だとしている。
この診療ガイドラインの医師向け解説では、単に1〜2週ごとに服用量の25%ずつ減薬するのが標準的であると書かれ「1錠の1/4」という情報が消去されている。多剤では半減期が短いものを先に減量するのが望ましく、単剤の超短時間作用型である場合には長時間型に置換してもいいとされる。この診療ガイドラインの睡眠薬の離脱症状の出現率の論拠は、非ベンゾジアゼピン系のゾピクロン(アモバン)の7.5mgかゾルピデム(マイスリー)の10mgを3カ月使用した後に徐々に減量した場合のものである[38]。説明のある通り、非ベンゾジアゼピン系の薬剤は、受容体のサブタイプに対してより選択的に作用することで抗不安作用が少ないといった改良された睡眠薬であり、依存と離脱症状の点において古いベンゾジアゼピン系よりも改良された利点がある[2]。睡眠薬での懸念は抗不安薬とは異なり、長年にわたった投薬からの急な断薬は、低用量においてさえも、痙攣発作を起こすなど非常に悲惨で危険となりうるため、低力価で長時間型の薬剤を使用し、特に何年も使用した場合には数カ月にわたって漸減すべきである[2]。
2007年の英国国立薬物乱用治療庁の臨床ガイドラインでは、明らかに依存の症状がある場合にはジアゼパムに等価用量で置換して減量を開始し、治療用量の場合には、はじめにジアゼパムで2〜2.5mg減量し症状が出ればおさまるまで維持し、2週間ごとに1日の用量の8分の1(4分の1から10分の1の間)で減量するとしている[39]。
2012年のコロンビア大学嗜癖物質乱用国立センター(The National Center on Addiction and Substance Abuse at Columbia University)によるさまざまな薬物の嗜癖についての科学的根拠の精査は[40]、ベンゾジアゼピンのような中枢神経抑制剤からの離脱は、アルコールにおける発作やせん妄に似た症状により一部では致死的となる場合があり、離脱症状は一般的には10 - 14日だが半年程度持続することもあるため、数週間から数か月にわたって漸減すべきであり、選択肢としてクロルジアゼポキシドやクロナゼパムのような長時間型の薬剤を処方することもあるとしている。
アメリカ精神医学会(APA)による2009年のパニック障害のガイドラインでは、主とする治療薬は抗うつ薬となるが、初期にベンゾジアゼピンを使用しても身体依存に注意して2〜3か月をめどとし、中止は2〜4カ月にわたって週に10%の減量を超えないように漸減し中止する[41]。
イギリスでは『英国国民医薬品集』(British National Formulary)にて漸減を推奨している[42]。英国国立医療技術評価機構(NICE)の2004年不眠症診療ガイドラインでは、処方は4週間を限度とし、かつベンゾジアゼピンの慢性的使用者の10〜30%が身体的依存を生じ、半数が離脱症状を経験すると記されている[43]。
イギリスでは、フルニトラゼパム(サイレース、ロヒプノール)はNHSブラックリストに載っており国民保健サービスでは処方できない[43]。アメリカでも医薬品として認可されておらず[44]、国際的にも、1995年には他のベンゾジアゼピンよりも強い乱用傾向のため向精神薬に関する条約のスケジュールIIIへと規制が1段階昇格している[45]。
対照的に、日本ではフルニトラゼパムが利用可能である上に、厚生労働省の研究において、睡眠薬の基準をフルニトラゼパムで等価換算しているし、2010年の精神科における2534名の処方歴から実際に26.3%と最も多い比率で処方されている[46]。睡眠薬/抗不安薬をジアゼパムに等価換算し、1剤では平均8.6mg、同様に2剤で17.3mg、3剤で25.8mg、4剤で38.1mg、5剤は48.6mg、6剤以上では72.1mgである[47]。多剤併用では、高力価のベンゾジアゼピンの使用や、3剤以上とですでに高用量となっている場合に注意が必要である。
ジアゼパムでは30〜40mgからの中止によってせん妄や痙攣発作が生じやすい[48]。アルコールなどの併用を除外して、ベンゾジアゼピン依存症だと同定された108人のうち高用量から突然断薬となった12%(13人)にせん妄や痙攣が生じ、せん妄が10%(11人)、痙攣が3%(3人)である[49]。別の調査では、ベンゾジアゼピンの一年以上の使用者の離脱反応として、7%に精神病症状、4%にてんかん発作が生じている[50]。
『精神障害の診断と統計マニュアル』第5版(DSM-5)には、ジアゼパムに換算して15mgの「少量〔ママ〕」でも、数か月にわたり毎日服用していれば離脱が生じることが報告されており、換算40mgでは臨床的な離脱症状を起こしやすく、100mgではせん妄や痙攣を、よりおこしやすいことが記載されている[51]。
明確に高用量からの離脱に言及したものは、上述したヘザー・アシュトンの『ベンゾジアゼピン』や[6]、2007年の英国国立薬物乱用治療庁の臨床ガイドラインや[39]、2012年の英国精神薬理学会(BAP)の物質使用障害に関する科学的根拠に基づくガイドライン[52]、また2009年の世界保健機関による薬物依存と離脱の管理のための臨床ガイドラインがある[53]。
- 『ベンゾジアゼピン』はジアゼパムに換算して100mgを超えるケースにも詳細に言及し、またもっとも遅い減量ペースであるが離脱症状が長期化するのを避けることに焦点を当てているためである。
- イギリス国民保健サービスの臨床ガイドラインでは、ジアゼパムに換算して30mg以上はごくまれにしか処方されるべきでなく、離脱を目的として短期間に限るべきとしている。ジアゼパムに換算して50mg以上のような非常に高用量の場合、専門家による評価が必要だとしている。
- 英国精神薬理学会のものは、単に長期的に処方された治療用量の依存と、高用量となりがちな処方薬の誤用や違法な乱用を伴う依存を区別し、後者は先に治療用量に減量することが目的であるとしている。その具体的な手法には言及していない。ジアゼパムに換算して30mgの高用量は滅多に処方されるべきではないとし、この量は非常に高用量となったベンゾジアゼピンからの離脱痙攣を予防するのに十分な量であるためである。
- 世界保健機関のガイドラインは、ベンゾジアゼピンは数週間で依存を形成し、離脱症状の重症度の変動が激しいため離脱尺度による計測は推奨できないとしている。また、最も安全な離脱の管理法は、用量を徐々に減量することであるとし、このことで離脱症状を軽減し発作の発症を予防できる。換算を超えても最大40mgまでの等価用量のジアゼパムを1日に3等分して投与し置換して、4〜7日続け安定化させる。その後は、低用量と元が40mg以上だった高用量とに漸減計画が分かれこれに従って1〜2週間ごとに減量していき、症状には波があるので症状が弱まるまで現行の用量を維持するとしている。(最大でも40mgの高用量のジアゼパムはアルコールの離脱の管理においても適切な量である[54])
長時間型のジアゼパムに置換し、昼、朝、夜の順で減量し減薬していく方法は、ヘザー・アシュトンの『ベンゾジアゼピン』と世界保健機関の診療ガイドラインとで共通し、夜を最後に回す理由はアシュトンによれば睡眠のためである。この2つを参考にすれば減量幅やペースは個々の症状の重症度に合わせて変化するだろうが、おおよそ以下のような手順である。
| 朝 | 昼 | 晩 | 合計(ジアゼパム換算) |
|---|---|---|---|
| 短時間型A薬100% | 短時間型A薬100% | 中間型B薬100% | 20mg |
| 短時間型A薬100% | 短時間型A薬100% | 中間型B薬50% ジアゼパム5mg |
20mg |
| 短時間型A薬100% | 短時間型A薬100% | ジアゼパム10mg | 20mg |
| ジアゼパム5mg | ジアゼパム5mg | ジアゼパム10mg | 20mg |
| ジアゼパム5mg | ジアゼパム2.5mg | ジアゼパム10mg | 17.5mg |
| ジアゼパム5mg | ジアゼパム10mg | 15mg | |
| ジアゼパム2.5mg | ジアゼパム10mg | 12.5mg | |
| ジアゼパム10mg | 10mg | ||
| ジアゼパム7.5mg | 7.5mg | ||
| ジアゼパム5mg | 5mg |
夜10mgのみとなってからの減量幅はアシュトンの『ベンゾジアゼピン』では1mgずつ、また13の症例が例示されている。米国のNPO離脱支援団体 では、微量づつ減量していくマイクロテーパリング法 を紹介している。
- 『精神科救急のすべて』(Handbook of Emergency Psychiatry)は、救急医療におけるものだが、ベンゾジアゼピンを含む鎮静催眠剤の離脱はアルコールと同様の処置が必要であるとし、バルビツール酸系のフェノバルビタールの置換や、ベンゾジアゼピン系のクロルジアゼポキシドやクロナゼパムへの置換を候補として挙げ、1日の服用量をフェノバルビタールに等価換算し1日に3分割して投与する方法を紹介している[55]。しかし、すでに見てきたように通常ベンゾジアゼピン系において用いられるのはバルビツール酸系ではなく、ベンゾジアゼピン系である。
2007年のイギリスの薬物依存の臨床ガイドラインは、重篤な離脱症状を呈し対処されていない患者は、症状緩和のために用量を増加させる必要があるかもしれないとしている[39]。
他のさまざまな薬物を併存したケースの治療の科学的根拠の比較については、英国精神薬理学会のガイドラインが言及している[56]。『精神科救急のすべて』は、アルコールや違法薬物を含めた併存した離脱における救急状態について、実際の救急医療に基づき言及している[55]。精神科の多剤大量処方によって複雑な多剤処方となっている場合の減量について、笠陽一郎の『精神科セカンドオピニオン』にさまざまな事例が紹介されている[57]。
兆候と症状
[編集]ベンゾジアゼピン、バルビツール酸、アルコールなどの鎮静催眠剤の離脱の影響は、深刻な医学的合併症となる。アヘンなどのオピオイドの離脱を引き合いにしてもその危険性を上まわる[58]。たいていの患者は医師からの助言や中止のための支援はわずかである[59]。一部の離脱症状は、薬が処方されることとなった症状と同じであり[25]、急性であったり長期化したりする。症状の発症は、長い半減期をもつベンゾジアゼピンでは3週間まで遅れる場合があるが、短時間型のものでは一般的に24〜48時間で現れる[60]。高用量あるいは低用量の中止による症状には、基本的な違いはないが、高用量のほうが重篤化しやすい傾向がある[61]。
日中における再発と、服用間離脱とも呼ばれる反跳性の離脱症状は、依存が始まれば生じることがある。再発は、薬が最初に処方された症状の再来である。対照的に、反跳症状は、ベンゾジアゼピンが最初に服用された症状の以前より激しい再来である。一方で、離脱症状は服用量が減少した期間中に初めて出現し、不眠症、不安、苦悩、体重減少、パニック、抑うつ、現実感喪失、偏執病などの特徴があり、トリアゾラムやロラゼパムのような短時間型のベンゾジアゼピンの中止によく関連している。トリアゾラムやロラゼパムでは7日の使用後でも離脱症状を発症させた証拠がある。[26][62]日中の症状は、夜間にベンゾジアゼピン[63][64]あるいはゾピクロンのようなZ薬[65]を使用しだしてから数日から数週間後に生じる。離脱に関連した不眠症は、治療前よりも悪化して反跳する[66][67]。これはベンゾジアゼピンを断続的に使用した場合でもそうである[68]。
以下の症状が、徐々にあるいは急に減量した期間中に生じる。
- うずきと痛み[69]
- 動揺また落ち着かない[69]
- アカシジア
- 不安、恐怖とパニック発作もありうる[1][69]
- かすみ目[69]
- 胸痛[69]
- 離人症[70]
- 抑うつ(深刻となりえる)[71]、自殺念慮もありうる
- 現実感喪失[72]
- 下痢
- 瞳孔拡大[26]
- めまい[69]
- 複視
- 口渇[69]
- 不快[73][74]
- 電撃の感覚[6][75]
- 血圧の上昇[76]
- 疲労と衰弱[69]
- インフルエンザ様症状[69]
- 胃腸の問題[77][77][78]
- 聴覚障害[69]
- 頭痛[1]
- 火照りや寒気[69]
- 嗅覚過敏[79]
- 高血圧[80]
- 入眠時幻覚[21]
- 病気不安症[69]
- 触覚に対する過敏[72]
- 音に対する過敏[69]
- 頻尿[69]
- 優柔不断[69]
- 不眠症[81]
- 集中力低下[1]
- 記憶と集中の障害[69]
- 食欲不振と体重減少[82]
- 金属味(味覚の問題)[79]
- 軽度から中等度の失語[79]
- 気分変動[69]
- 筋痙攣、筋肉痛、筋攣縮[83]
- 吐き気と嘔吐[81]
- 悪夢[81]
- 痺れとうづき[69]
- 強迫性障害[84][85]
- 痺れ[72][79]
- 偏執病[79]
- 止まっているものが動くような知覚[72]
- 汗[1]
- 羞明(光で目が痛い)[79]
- 起立性低血圧(立ちくらみ)[81]
- 反跳性REM睡眠[86]
- むずむず脚症候群[28]
- 音がいつもより騒がしい[72]
- 凝り[69]
- 味覚と嗅覚の障害[69]
- 頻脈[87]
- 耳鳴り[88]
- 振戦(ふるえ)[89][90]
- 視覚障害
- 角質減少
ベンゾジアゼピンの急な、あるいは急速すぎる中止は、さらに重篤で不快な離脱症状となる可能性がある
- 筋萎縮、筋減少
正に症状は「生きているのか夢の世界にいるのか」という症状となり、外出も不可なほどとなる。 患者は離脱の進行と共に、改善された気分や認知能力を伴った身体と精神の健康に気づく。
機序と病態
[編集]ベンゾジアゼピンはGABA阻害を増強する。もし長期投与などによりこの阻害が継続すると、神経適応はこの中枢神経系の抑制強化に対して、GABA阻害の減少とグルタミン酸興奮性の増強によってバランスをとる。ベンゾジアゼピンを中断すると神経適応はあらわとなり、神経系の興奮と離脱症状の出現がおこる。
離脱時にグルタミン酸系の興奮作用が増加することが、キンドリング現象を起こすと考えられている[22]。 ベンゾジアゼピン離脱の既往歴を持っている人は再度の離脱には成功する確率が低いことが知られている[111]。 アルコール離脱と同様、ベンゾゼジアピン離脱を繰り返すと中枢神経系の感作やキンドリングにつながり、認知能力の悪化、症状と離脱期間の悪化となる[112][113][114]。
管理
[編集]WHOのガイドラインに従えば、離脱は長期作用型のベンゾジアゼピンに置換し、8-12週間以上をかけて行うべきとされている[115]。
心理学的な介入は、徐々に減量する(漸減する)だけよりも、中止後の追跡調査において小さいが有意に追加の利益をもたらす可能性がある[116]。調査された心理学的な介入とは、リラクゼーションの訓練、不眠症に対する認知行動療法、消費量と症状の自己管理、目標設定、離脱の管理と不安時の対処である[116]。
十分な動機づけと適切な方法により、ほとんどの人がベンゾジアゼピンからの離脱に成功する。しかし、長期化した重篤な症状は、結婚の破たん、企業の倒産、破産、入院につながり、最も深刻な悪影響は自殺である[3]。このように、長期的な使用者は自らの意思に反して中止されてはならない[6]。急速すぎる離脱、説明不足、一時的な離脱症状に対する安心付けの怠りは、狂ってしまうのではないかというパニックと恐れを増加させ、その結果として心的外傷後ストレス障害に似た状況に陥らせやすい。ゆっくりとした離脱は、周囲の人々からの励ましと相まって成功を高める[6][21]。
2017年の高齢者のベンゾジアゼピン漸減の補助についてのシステマティック・レビューでは、患者教育が最も成功率に寄与しており、認知行動療法は一貫しない結果がみられるが全体的には有益であり、ほかの薬物の使用は結論を出せなかった[117]。
医薬品との相互作用
[編集]いくつかの代替の薬物療法には見込みがあるが、それらを利用するには現在の証拠では不十分である[116]。いくつかの研究により実際に代替の薬物療法への突然の置き換えは、漸減法単独よりも有効性が低いことが判明しており、3つの研究だけが、漸減法と共にメラトニン[118]あるいはパロキセチン[119]、あるいはトラゾドンとパルプロ酸[120]を追加することによる利益を見出している。
2018年の薬理学的介入についてのコクランレビューは、研究規模が小規模なため確固とした結論を導くことはできないとし、三環系抗うつ薬、フルマゼニル、長期的な追加では効果が持続しなかったパロキセチンなどが含まれる[121]。
- アルコールは、たとえ適度の飲酒であっても、ベンゾジアゼピンとの交叉耐性のためか、離脱失敗の有意な予測因子であることが判明している[6][122][123]。
- 抗精神病薬は、ベンゾジアゼピン離脱に誘発された精神病には、たいてい無効である[75][124]。抗精神病薬は、ベンゾジアゼピン離脱中は痙攣などの離脱症状を悪化させる傾向にあるため避けるべきである[60][125][126][127]。一部の抗精神病薬、特にクロザピン、オランザピン(ジプレキサ)、低力価のフェノチアジン系(クロルプロマジンなど)は他よりも離脱時のリスクが高い。それらは発作閾値を低下させ、離脱症状を悪化させる。もし使われていた場合は、細心の注意が必要となる[128]。
- バルビツール酸系は、ベンゾジアゼピンとの交叉耐性があるため避けるべきである。
- ベンゾジアゼピンや交叉耐性のある薬物は、断薬後には時々でさえ避けるべきである。これには同様の作用機序を持つ非ベンゾジアゼピン系のZ薬も含まれる。なぜなら、ベンゾジアゼピン系への耐性は、個々人の生化学により離脱後も4カ月から2年にわたり存在することが証明されているからである。ベンゾジアゼピンへの再暴露によって、通常、耐性とベンゾジアゼピン離脱症状は再燃した。[122][129]
- ブプロピオンは、主に抗うつ薬や禁煙に使用されるが、発作のリスクを高めるため、ベンゾジアゼピンや他の鎮静催眠薬(アルコールなど)の急な離脱を経験した患者には禁忌である[130]。ブプロピオンには持続的な覚醒作用がある。
- ブスピロン(セディール)による増強では、中止の成功率を高めることは判明しなかった[9]。
- カフェインは覚醒の性質のため、離脱症状を悪化させることがある[6]。興味深いことに、動物実験においてカフェインは、発作閾値を低下させるようなベンゾジアゼピン部位の調整を示した[131]。痙攣が起きやすくなる可能性がある。
- カルバマゼピンは、抗てんかん薬だが、ベンゾジアゼピンの離脱の管理と治療において、いくらかの有益な効果があるようである。とはいえ、現時点では研究が限られているためベンゾジアゼピンの離脱に推奨するほどの特性はない。[122]
- フルマゼニルは、ベンゾジアゼピンの解毒剤であるため、身体依存が形成され現在服用している最中には非常に危険である。これは医薬品添付文書においても禁忌である[132]。フルマゼニルは、耐性を反転させ受容体の機能の正常化を促すことが分かっている。しかしながら、離脱治療においての作用についての、無作為化試験の実施が求められている[133]。フルマゼニルは、GABAA受容体のベンゾジアゼピン受容体における上方制御を促し、脱共役を反転させる。その結果、耐性を反転させ、離脱症状や再発率の低減を図る[134][135]。これは研究レベルに限定されておりリスクを抱えるため、フルマゼニルによる解毒法は議論の余地があり、医学的監視下で入院してのみ行うことができる。
- ベンゾジアゼピン受容体拮抗薬であるフルマゼニルの、離脱後に持続するベンゾジアゼピン離脱症状における影響についての研究が、レーダーとモートンによって実施された。被験者は、ベンゾジアゼピンなしとなってから1か月から5年であった。しかし全員がさまざまな程度の離脱の影響が続いていると報告した。持続的な症状には、思考が鈍い、疲労感、首の凝りのような筋肉の症状、離人症、痙攣と震え、またベンゾジアゼピンの離脱に特徴的な知覚の症状、しびれてチクチクする感じ、灼熱感、痛みと身体がゆがむような主観的な感覚が挙げられた。偽薬対照において、0.2 - 2mgのフルマゼニルの静注投薬はこれらの症状を減少させた。ベンゾジアゼピン受容体拮抗薬は中立であり臨床的な効果はないので興味を引く。研究者によれば、この研究が示唆するありそうな説明として、ベンゾジアゼピンの使用に続く耐性によって、逆作動薬の構造へとGABA-BZD受容体複合体における構造が固定され、そして、拮抗薬のフルマゼニルはベンゾジアゼピン受容体を元の感度に初期化するというものである。この研究ではフルマゼニルは長期化したベンゾジアゼピンの離脱症状の治療に成功したことが分かったが、さらなる研究が必要である[136]。スウェーデンのボーグ教授による調査は、長期離脱に苦しむ患者で同様の結果を報告した[69]。2007年には、フルマゼニルのメーカーであるホフマン・ラ・ロシュは、長期化したベンゾジアゼピン離脱症状の存在を認識したが、その症状をフルマゼニルで治療することは推奨していない[137]。オーストラリアのメルボルンにあるセントヴィンセント病院では、フルマゼニルを徐々に体内に放出するポンプを使い重篤な離脱症状をもつベンゾジアゼピンの依存の治療を行っている[138]。
- フルオロキノロン系抗生物質は、アシュトンによって指摘されており、また他の研究者によってベンゾジアゼピン依存または離脱中に、あるいは一般集団の1 - 4%において重篤な中枢神経毒性の発生率を増加させることが実証されている。これはおそらくベンゾジアゼピン受容体部位からベンゾジアゼピンを完全に外すという、GABA拮抗作用の結果である。この拮抗作用は急性離脱症状を引き起こし、数週間から数カ月持続させることもある。これには不安、精神病、偏執病、重篤な不眠症、耳鳴り、光や音への過感受、振戦、痙攣状態、自殺念慮や自殺企図が含まれる。ベンゾジアゼピンの依存や離脱中には禁忌である。[6][139][140][141][142]非ステロイド性抗炎症薬(NSAID)にも弱いGABA拮抗の性質があり、動物実験でベンゾジアゼピンをその結合部位から外すことが示されている。しかしNSAIDがフルオロキノロンと併用された場合、GABA拮抗作用、GABA毒性、発作や他の重篤な副作用を著しく増加させることになる。(en:adverse effects of fluoroquinolonesも参照)[143][144][145]
- イミダゼニルは、離脱の管理においていくつかの研究であげられているが、現在は離脱には使われていない[146]。
- イミプラミン(イミドール、トフラニール)は、三環系抗うつ薬に属し、統計的に投薬中止の成功率を高めることが判明している[9]。
- メラトニンによる増強は不眠症の患者において、統計的に投薬中止の成功率を高めることが判明している[9]。他と異なり、メラトニンには離脱症状がなく、増強した医薬品に対して新たに身体依存が形成されるリスクはない。
- フェノバルビタール(バルビツール酸系)は、「解毒」施設や他の入院施設において、急速な離脱期間中の発作を予防するのに用いられている。フェノバルビタールは、1〜2週間で漸減するが、よりゆっくりなほうが優先される。[26]比較研究ではベンゾジアゼピンを用いた急速な減量のほうが、フェノバルビタールを用いた急速な減量よりも優れていることが分かっている[147][148]。
- プレガバリン(リリカ)は、ベンゾジアゼピン離脱症状の重症度を下げ[149]、再発リスクを低下させる可能性がある[150]。ただし、ベンゾジアゼピンと同じくGABA受容体に作用する。
- プロゲステロンは、離脱の管理には無効だと判明している[133]。
- プロプラノロール(インデラル)は、中止の成功率を高めるかは判明しなかった[9]。
- SSRI系抗うつ薬の追加は、ベンゾジアゼピン離脱の治療には少ししか効果がないことが判明している[151]。
- トラマドールは、オピオイド鎮痛剤に属し、発作閾値を低下させるためベンゾジアゼピンの離脱中には避けるべきである。
- トラゾドン(SSRI、レスリン、デジレル)が、中止の成功率を高めるかは判明しなかった[9]。
予防
[編集]『英国国民医薬品集』(すべての英国医師に発行される医療指導本)に従えば、ベンゾジアゼピンからの急速な離脱よりも、非常にゆっくりのほうが最善である[152]。減量の速度が適切であれば、症状の強さと重症度を最小化する。おまけに、ゆっくりであれば、重篤な長期化する症状の発症リスクを低下させるだろう。
ジアゼパムやクロルジアゼポキシドのような長い半減期のベンゾジアゼピンらは、反跳作用を最小化し、またそれらは入手可能な低力価の薬剤である。一部の人々は、減量速度がゆっくりな時でも減量と減量との間で十分に安定化させない。そのような人々では時に完全に離脱するまでの間、具合が良くないことが続く。[10]
予後
[編集]最初に急な離脱が試まれ失敗し、続いて体系的に徐々に中止した場合の成功率は、中央値58%で25%から100%の範囲である[9]。パニック障害に対する認知行動療法、不眠症に対するメラトニン、フルマゼニルとバルプロ酸ナトリウムは、成功率の向上に有益であった[9]。10年にわたる追跡からは、長期的な使用からの離脱の成功から2年後にまだ過半数が断薬を継続しており、この2年時点の状態を維持することができていた場合には、10年時点でも維持されている可能性が高かった[12]。ある調査では、ベンゾジアゼピンの長期的な使用からの禁断後1年で、認知、神経学的、知的な障害は正常に戻っていた[153]。
以前に精神科の診断歴のあるものにおいても、2年の追跡調査時点で、徐々の減量により同様の成功率であった[10][154]。ベンゾジアゼピンからの離脱は、抗うつ薬の使用の増加に関連しなかった[155]。
2018年の薬理学的介入についてのコクランレビューは、薬物を置き換えるような薬理学介入について、ランダム化比較試験のより長期的な転機を必要とし、製薬産業からは独立して試験を実施すべきとした[121]。
離脱の管理
[編集]短時間型あるいは中間作用型のベンゾジアゼピンからの離脱は、服用間の反跳性症状の強さのために難しくなる[6][156][157][158]。さらに、短時間型ベンゾジアゼピンは、より強い離脱症状を生じさせる傾向にある[159]。この理由のため減量による中止は、短時間型のベンゾジアゼピンを、ジアゼパム(セルシン、ホリゾン)やクロルジアゼポキシド(コントール、バランス)のような長時間型のものに等価換算した量に置換して行われる。正確な量の使用に失敗すれば、重篤な離脱反応を引き起こしうる[160]。
- 24時間以上の半減期のベンゾジアゼピンには、ジアゼパム(セルシン)やクロルジアゼポキシド(コントール)のほかに、ロフラゼプ酸エチル(メイラックス)、クロナゼパム(リボトリール)、フルラゼパム(ダルメート)、メダゼパム(レスミット)、プラゼパム(セダプラン)、クアゼパム(ドラール)などがある。
- 24時間以下の半減期のベンゾジアゼピンには、アルプラゾラム(ソラナックス、コンスタン、カームダン)、ブロマゼパム(レキソタン、セニラン)、ブロチゾラム(レンドルミン、グッドミン)、エチゾラム(デパス)、フルニトラゼパム(ロヒプノール、サイレース)、ロラゼパム(ワイパックス、ユーパン)、ロルメタゼパム(エバミール、ロラメット)、ミダゾラム(ドルミカム)、ニメタゼパム(エリミン)、ニトラゼパム(ベンザリン)、トリアゾラム(ハルシオン)などがある。
利用者が少ない薬剤では、入手可能性が限られる可能性もある。また長時間型でも、クロナゼパム(リボトリール)では高力価であるし、クアゼパム(ドラール)などは15mgと20mgの錠剤型しかない。ジアゼパムは世界的に広く用いられ、2mgと5mgと10mgの錠剤に加え、散剤、液剤、また重篤な症状を呈した救急時には医療機関に注射剤もあり、換算基準であるため把握が容易である。
等価用量に置換してから、徐々に減量していく。アシュトンの方法における減量の幅は、反応と重症度に従って1〜2週間ごとに残っている用量から10%削減し、最終的な用量はジアゼパムの0.5mgまたはクロルジアゼポキシドの5mgである[6]。
期間
[編集]最後の服薬の後、離脱の急性期はたいてい2週間ほど続く。遅延性離脱症状は、6か月から12カ月持続し徐々によくなるが[10][61]、臨床的に有意な離脱症状は数年にわたり持続することもある。とはいえ、これもまた徐々に減少していく。
わずか8週間、アルプラゾラム(ソラナックス)を服用した臨床試験では、記憶障害の長期化症状を引き起こし中止後にも8週間持続した[161]。
遷延性離脱症候群
[編集]遷延性離脱症候群(Protracted withdrawal syndrome)は、数カ月から数年にわたって持続する症状である。
ベンゾジアゼピンから離脱した人々の少数、おそらく10〜15%は、遷延性離脱症候群が出現し、時に深刻となりえる。症状は、耳鳴り[88][162]、精神病、認知障害、胃腸に関する訴え、不眠症、痺れ(しびれと疼き)、痛み(たいてい手足の)、筋肉痛、筋力低下、凝り、痛みを伴う震え、震えの発作、ひきつけ、眼痙[21]、これらの症状は、既往歴がなくても生じることがある。ベンゾジアゼピンの減量中あるいは中止により生じた耳鳴りは、再服薬によって軽減される。
神経心理学な要因をテストした調査では、精神生理学的な指標が通常とは異なることを見出し、そして遷延性離脱症候群が長期的な使用が原因となる本物の医原性の病態であると結論した[163]。持続する症状の原因は、薬剤誘発性の受容体の変化のような薬理学的な要因と、心理的な要因との複合であり、特に高用量の使用者では薬剤による、構造上の脳損傷や、神経損傷が原因である[21][164]。症状は時間と共に改善し、無能力の数年を過ごしてもそのうち普段の生活を取り戻す。[6]
ゆっくりな離脱は、長期化し重篤な症状の状態となるリスクを有意に低下させる。遷延性離脱症候群は、いい時と悪い時の時期によって中断することがある。長期化した離脱の間には、生理的な変化によって瞳孔拡大や、血圧や心拍数の増加など周期的に症状の増加が起こることもある[26]。症状の変化は、耐性反転の過程の間の、受容体におけるGABAへの感度の変化によるものであるとの説もある[6]。メタアナリシスによれば、ベンゾジアゼピンの使用が原因の認知障害は離脱から6ヵ月後には改善しているが、残りの認知障害は永続するか、6か月以上必要な可能性がある[165]。
長期化した症状は、数か月から数年にわたって薄れていく。長期化したベンゾジアゼピンの離脱症状を治す方法は、時間を除いて知られていないが[21]、フルマゼニルは、1か月から5年間の間ベンゾジアゼピンなしであった患者の敵意や攻撃性の感情を減少させるのに偽薬よりも有効であることが判明している[166]。つまり、フルマゼニルが遷延性離脱症候群を治療することを示唆している。
疫学
[編集]離脱症候群の重症度と期間は、減量のペース、服用期間と服用量、おそらく遺伝的要素などに関係すると思われる[6][167]。
特別集団
[編集]高齢者
[編集]ベンゾジアゼピン依存症の高齢者を対象とした研究によると、高齢者はほとんど合併症を引き起こすことなく離脱を達成でき、その後は睡眠と認知能力の改善をもたらす可能性があることが判明した。
離脱成功者は離脱の52週間後には、認知能力に22%の改善がみられ社会機能にも改善がみられた。ベンゾジアゼピンの使用を継続している人達は認知能力の5%が減少し、これは通常の老化の速度よりも早く老化が進んでいるように見られる。このことは、ベンゾジアゼピンの服用を長く続ければ続けるほど認知能力が低下していくということを示唆している。
ベンゾジアゼピン断薬後の最初の数ヶ月の間は、高齢者には症状の悪化が見られたが、その後の24週間のフォローアップ(経過観察)後、ベンゾジアゼピンの使用を継続している人達に比べて明らかに改善がみられた。睡眠の改善が、24週間および52週間のフォローアップ後に見られた。著者達は、ベンゾジアゼピンは離脱による反跳性不眠の抑制作用を除いて、睡眠問題に対して長期的には有効でないと結論した。
ベンゾジアゼピン離脱の24週間後から52週間後の間にわたって、睡眠やいくつかの認知能力や、技能能力など多くの点で改善が見られた。ベンゾジアゼピンに敏感な一部の人の認知能力やエピソード記憶は改善しなかった。しかし、著者達は3.5年の追跡調査では全く記憶障害を示さなかった若年者の調査を引用し、慢性的なベンゾジアゼピン使用から特定の記憶機能が回復するためには時間がかかると推測し、ベンゾジアゼピン離脱の52週間よりもさらに後に、高齢者の認知機能のさらなる改善が起きる可能性があると推測した。
ベンゾジアゼピンの使用中止後、改善が見られるまでに24週間かかった理由は、脳がベンゾジアゼピンのない環境に適応するためにそれだけの時間が必要だったからである。24週の時点で、脳における情報処理の精度の向上を含むかなりの改善が見られた。しかし、ベンゾジアゼピンの使用を継続した人にはその退化がみられた。52週の継続調査でさらに改善が認められ、これはベンゾジアゼピンの中止により、継続的に改善が進んでいることを示している。ベンゾジアゼピンで若年者にも視空間記憶の認知能力の低下が見られたが、認知能力は高齢者ほどには影響を受けなかった。
高齢の患者はベンゾジアゼピンを断ってから52週目で反応時間に改善がみられた。高齢者が車を運転するときに、ベンゾジアゼピン使用者は交通事故のリスクの増大があるので、この反応時間の改善は重要である。
24週間のフォローアップで、患者の80%がベンゾジアゼピンからの離脱に成功した。この離脱成功の一因は、ベンゾジアゼピンの心理的な依存を断ち切った「偽薬手法」に起因する:高齢の患者が気づいた時は彼らは数週間前にゆっくりなペースでの減薬を完了しており、すでに偽薬のみを服用していた。この離脱の成功により、高齢者は薬なしで眠れることができるようにり安堵することができた。
著者達はまた、新しい非ベンゾジアゼピン系のZ薬の薬理学的な、また作用機序の類似性を警告した[168]。
他の半減期の長いベンゾジアゼピンと同様に、ジアゼパムとクロルジアゼポキシドの耐性は、高齢者にとっては若年者に比べて2倍程度に長くなる。多くの医師は、高齢に応じてベンゾジアゼピンの投与量を調整することはしない[169]。
妊娠中
[編集]新生児離脱症候群
[編集]ベンゾジアゼピンは、特に妊娠後期中に取られた場合は、新生児に重度ベンゾジアゼピン離脱症候群を引き起こす可能性がある。
この節の加筆が望まれています。 |
2010年には厚生労働省から、重篤副作用疾患別対応マニュアル(新生児薬物離脱症候群)[170]がでている。
日本国内でも新生児の副作用が認知されており、ベンゾジアゼピンの添付文書を見ると以下の警告文も明記されている。
妊婦、産婦、授乳婦等への投与
- 妊婦(3カ月以内)又は妊娠している可能性のある婦人には,治療上の有益性が危険性を上回ると判断される場合にのみ投与すること.〔動物実験により催奇形作用が報告されており,また,妊娠中に他のベンゾジアゼピン系薬剤(ジアゼパム)の投与を受けた患者の中に奇形を有する児等の障害児を出産した例が対照群と比較して有意に多いとの疫学的調査報告がある.〕
- 妊娠後期の婦人には,治療上の有益性が危険性を上回ると判断される場合にのみ投与すること.〔ベンゾジアゼピン系薬剤で新生児に哺乳困難,嘔吐,活動低下,筋緊張低下,過緊張,嗜眠,傾眠,呼吸抑制・無呼吸,チアノーゼ,易刺激性,神経過敏,振戦,低体温,頻脈等を起こすことが報告されている.なお,これらの症状は,離脱症状あるいは新生児仮死として報告される場合もある.また,ベンゾジアゼピン系薬剤で新生児に黄疸の増強を起こすことが報告されている.なお,妊娠後期に本剤を連用していた患者から出生した新生児に血清CK(CPK)上昇があらわれることがある.〕
- 分娩前に連用した場合,出産後新生児に離脱症状があらわれることが,ベンゾジアゼピン系薬剤で報告されている.
- 授乳婦への投与は避けることが望ましいが,やむを得ず投与する場合は,授乳を避けさせること.〔ヒト母乳中へ移行し,新生児に体重増加不良があらわれることがある.また,他のベンゾジアゼピン系薬剤(ジアゼパム)で嗜眠,体重減少等を起こすことが報告されており,また黄疸を増強する可能性がある.〕
妊娠中の断薬
[編集]妊娠中のベンゾジアゼピン系薬または抗うつ薬の突然の断薬は、重篤な合併症を引き起こす危険性が高いので、推奨できない。ベンゾジアゼピン系薬または抗うつ薬の突然の断薬は希死念慮や重度のリバウンド効果などの極端な離脱症状のリスクが高い。妊婦に精神疾患が存在するなら、妊娠中の母親の入院につながることができ、潜在的に自殺未遂、母、胎児の死を回避できる可能性がある。
この節の加筆が望まれています。 |
出典
[編集]- ^ a b c d e Petursson, H. (1994). “The benzodiazepine withdrawal syndrome”. Addiction 89 (11): 1455–9. doi:10.1111/j.1360-0443.1994.tb03743.x. PMID 7841856.
- ^ a b c 英国精神薬理学会 2013.
- ^ a b c Colvin, Rod (2008-08-26). Overcoming Prescription Drug Addiction: A Guide to Coping and Understanding (3 ed.). United States of America: Addicus Books. pp. 74–76. ISBN 978-1-886039-88-9. "I have treated ten thousand patients for alcohol and drug problems and have detoxed approximately 1,500 patients for benzodiazepines – the detox for the benzodiazepines is one of the hardest detoxes we do. It can take an extremely long time, about half the length of time they have been addicted – the ongoing relentless withdrawals can be so incapacitating it can cause total destruction to one’s life – marriages break up, businesses are lost, bankruptcy, hospitalization, and of course suicide is probably the most single serious side effect."
- ^ 世界保健機関 2009, p. 40.
- ^ ヘザー・アシュトン 2012, Chapt.3.
- ^ a b c d e f g h i j k l m n o p ヘザー・アシュトン 2012.
- ^ O'Connor, RD (1993). “Benzodiazepine dependence--a treatment perspective and an advocacy for control”. NIDA research monograph 131: 266–9. PMID 8105385.
- ^ MacKinnon, Glenda L.; Parker, William A. (1982). “Benzodiazepine Withdrawal Syndrome: A Literature Review and Evaluation”. The American Journal of Drug and Alcohol Abuse 9 (1): 19–33. doi:10.3109/00952998209002608. PMID 6133446.
- ^ a b c d e f g h Voshaar, R. C. O.; Couvée, JE; Van Balkom, AJ; Mulder, PG; Zitman, FG (2006). “Strategies for discontinuing long-term benzodiazepine use: Meta-analysis”. The British Journal of Psychiatry 189 (3): 213–20. doi:10.1192/bjp.189.3.213. PMID 16946355.
- ^ a b c d Higgitt, A C; Lader, M H; Fonagy, P (1985). “Clinical management of benzodiazepine dependence”. BMJ 291 (6497): 688–90. doi:10.1136/bmj.291.6497.688. PMC 1416639. PMID 2864096.
- ^ Nutt, David (1986). “Benzodiazepine dependence in the clinic: Reason for anxiety?”. Trends in Pharmacological Sciences 7: 457–60. doi:10.1016/0165-6147(86)90420-7.
- ^ a b De Gier, N.; Gorgels, W.; Lucassen, P.; Oude Voshaar, R.; Mulder, J.; Zitman, F. (2010). “Discontinuation of long-term benzodiazepine use: 10-year follow-up”. Family Practice 28 (3): 253–9. doi:10.1093/fampra/cmq113. PMID 21193495.
- ^ Authier, Nicolas; Boucher, Alexandra; Lamaison, Dominique; Llorca, Pierre-Michel; Descotes, Jacques; Eschalier, Alain (2009). “Second Meeting of the French CEIP (Centres d'Évaluation et d'Information sur la Pharmacodépendance). Part II: Benzodiazepine Withdrawal”. Thérapie 64 (6): 365–70. doi:10.2515/therapie/2009051. PMID 20025839.
- ^ Heberlein, A.; Bleich, S.; Kornhuber, J.; Hillemacher, T. (2008). “Benzodiazepin-Abhängigkeit: Ursachen und Behandlungsmöglichkeiten [Benzodiazepine Dependence: Causalities and Treatment Options]” (German). Fortschritte der Neurologie · Psychiatrie 77 (1): 7–15. doi:10.1055/s-0028-1100831. PMID 19101875.
- ^ Lee-chiong, Teofilo (2008-04-24). Sleep Medicine: Essentials and Review. Oxford University Press, USA. p. 468. ISBN 0-19-530659-7
- ^ Evans, Katie; Sullivan, Michael J. (2001). “Withdrawal and Medical Issues”. Dual Diagnosis: Counseling the Mentally Ill Substance Abuser (2nd ed.). Guilford Press. pp. 52–3. ISBN 978-1-57230-446-8
- ^ Lader, M (1987). “Long-term anxiolytic therapy: The issue of drug withdrawal”. The Journal of clinical psychiatry 48 Suppl: 12–6. PMID 2891684.
- ^ Boisse, NR; Periana, RM; Guarino, JJ; Kruger, HS; Samoriski, GM (1986). “Pharmacologic characterization of acute chlordiazepoxide dependence in the rat”. The Journal of Pharmacology and Experimental Therapeutics 239 (3): 775–83. PMID 3098961.
- ^ Boisse, NR; Periana, RM; Guarino, JJ; Kruger, HS (1986). “Acute chlordiazepoxide dependence in the rat: Comparisons to chronic”. NIDA research monograph 67: 197–201. PMID 3092067.
- ^ Galanter, Marc; Kleber, Herbert D (2008-07-01). The American Psychiatric Publishing Textbook of Substance Abuse Treatment (4th ed.). United States of America: American Psychiatric Publishing Inc. p. 58. ISBN 978-1-58562-276-4
- ^ a b c d e f Professor Heather Ashton (2004). Protracted Withdrawal Symptoms From Benzodiazepines. Comprehensive Handbook of Drug & Alcohol Addiction 2014年3月11日閲覧。
- ^ a b Allison C, Pratt JA (May 2003). “Neuroadaptive processes in GABAergic and glutamatergic systems in benzodiazepine dependence”. Pharmacol. Ther. 98 (2): 171-195. doi:10.1016/S0163-7258(03)00029-9. PMID 12725868.
- ^ Herman, JB; Brotman, AW; Rosenbaum, JF (1987). “Rebound anxiety in panic disorder patients treated with shorter-acting benzodiazepines”. The Journal of clinical psychiatry 48 Suppl: 22–8. PMID 2889722.
- ^ Allgulander, C; Bandelow, B; Hollander, E; Montgomery, SA; Nutt, DJ; Okasha, A; Pollack, MH; Stein, DJ et al. (2003). “WCA recommendations for the long-term treatment of generalized anxiety disorder”. CNS spectrums 8 (8 Suppl 1): 53–61. PMID 14767398.
- ^ a b Salzman, Carl (1993). “Benzodiazepine treatment of panic and agoraphobic symptoms: Use, dependence, toxicity, abuse”. Journal of Psychiatric Research 27: 97–110. doi:10.1016/0022-3956(93)90021-S. PMID 7908335.
- ^ a b c d e f Gabbard, Glen O. (2007-05-15). Gabbard's Treatments of Psychiatric Disorders, Fourth Edition (Treatments of Psychiatric Disorders). American Psychiatric Publishing. pp. 209–211. ISBN 1-58562-216-8
- ^ Onyett, SR (1989). “The benzodiazepine withdrawal syndrome and its management”. The Journal of the Royal College of General Practitioners 39 (321): 160–3. PMC 1711840. PMID 2576073.
- ^ a b c Ashton, Heather (1991). “Protracted withdrawal syndromes from benzodiazepines”. Journal of Substance Abuse Treatment 8 (1–2): 19–28. doi:10.1016/0740-5472(91)90023-4. PMID 1675688.
- ^ 加藤隆一監修、鈴木映二『向精神薬の薬物動態学 -基礎から臨床まで』星和書店、2013年、表紙帯頁。ISBN 978-4791108374。 出版社による書籍の概要ページに薬物動態学を苦手とする精神科医が多いという旨が書かれている。
- ^ Hollister, Leo E.; Motzenbecker, Francis P.; Degan, Roger O. (February 1961). “Withdrawal reactions from chlordiazepoxide ("Librium")”. Psychopharmacologia 2 (1): 63–68. doi:10.1007/BF00429621. PMID 13715373.
- ^ WHO Programme on Substance Abuse 1996, p. 20.
- ^ a b John Fauber, Kristina Fiore (2014年2月25日). “Killing Pain: Benzo 'Boost' Can Be Deadly”. MedPage Today 2014年3月11日閲覧。
- ^ “Hidden world of tranquilliser addicts”. BBC 2014年3月11日閲覧。
- ^ WHO Programme on Substance Abuse 1996, p. 30.
- ^ a b WHO Programme on Substance Abuse 1996, p. 26.
- ^ 日本うつ病学会、気分障害のガイドライン作成委員会『日本うつ病学会治療ガイドライン II.大うつ病性障害2012 Ver.1 (pdf)』(レポート)(2012 Ver.1版)、日本うつ病学会、気分障害のガイドライン作成委員会、2012年7月26日、22、24、26頁。2013年1月1日閲覧。
- ^ 厚生労働科学研究・障害者対策総合研究事業「睡眠薬の適正使⽤及び減量・中止のための診療ガイドラインに関する研究班」および⽇本睡眠学会・睡眠薬使用ガイドライン作成ワーキンググループ 編、気分障害のガイドライン作成委員会「Q26、Q31、Q34、Q38、Q39、Q40」『睡眠薬の適正な使用と休薬のための診療ガイドライン-出口を見据えた不眠医療マニュアル (pdf)』(レポート)(2013年10月22日改訂版(医師向け解説が削除された版)版)、日本うつ病学会、気分障害のガイドライン作成委員会、2013年6月25日、31、35、37、38-40頁。2014年3月12日閲覧。
- ^ Lemoine, P; Allain, H; Janus, C; Sutet, P (1995). “Gradual withdrawal of zopiclone (7.5 mg) and zolpidem (10 mg) in insomniacs treated for at least 3 months”. European Psychiatry 10: 161s–165s. doi:10.1016/0924-9338(96)80098-8. PMID 19698413.
- ^ a b c 英国国立薬物乱用治療庁 2007, pp. 60–61.
- ^ コロンビア大学嗜癖物質乱用国立センター 2012, pp. 91–93.
- ^ アメリカ精神医学会; Work Group on Panic Disorder; Murray B. Stein, Marcia K. Goin, Mark H. Pollack, Peter Roy-Byrne, Jitender Sareen, Naomi M. Simon, Laura Campbell-Sills (2009年1月). APA Practice Guideline for the Treatment of Patients With Panic Disorder, Second Edition (Report). doi:10.1176/appi.books.9780890423905.154688. 2009年7月12日閲覧。
- ^ 英国精神薬理学会 2012, p. 17.
- ^ a b 英国国立医療技術評価機構 (2004年4月). Insomnia - newer hypnotic drugs (TA77) (Report). National Institute for Health and Clinical Excellence. Chapt.2.10、2.13.
- ^ “Scheduling of Drugs Under the Controlled Substances Act”. FDA (1999年3月11日). 2013年2月23日閲覧。
- ^ 世界保健機関 (1995年). WHO Expert Committee on Drug Dependence - Twenty-ninth Report / WHO Technical Report Series 856 (pdf) (Report). World Health Organization. ISBN 92-4-120856-2。
- ^ 中川敦夫ら 2011, pp. 3–4.
- ^ 中川敦夫ら 2011, p. 8.
- ^ a b De Bard, ML (1979). “Diazepam withdrawal syndrome: A case with psychosis, seizure, and coma”. The American Journal of Psychiatry 136 (1): 104–5. PMID 103443.
- ^ Wolf, B.; Grohmann, R.; Biber, D.; Brenner, P.; Rüther, E. (March 1989). “Benzodiazepine Abuse and Dependence in Psychiatric Inpatients”. Pharmacopsychiatry 22 (02): 54–60. doi:10.1055/s-2007-1014578. PMID 2566180.
- ^ Schopf J (January 1983). “Withdrawal phenomena after long-term administration of benzodiazepines. A review of recent investigations”. Pharmacopsychiatria 16 (1): 1-8. doi:10.1055/s-2007-1017439. PMID 6131447.
- ^ アメリカ精神医学会『DSM-5 精神疾患の診断・統計マニュアル』日本精神神経学会日本語版用語監修・高橋三郎・大野裕監訳・染矢俊幸・神庭重信・尾崎紀夫・三村將・村井俊哉訳、医学書院、2014年6月30日、552頁。ISBN 978-4260019071。
- ^ 英国精神薬理学会 2012, pp. 16–18.
- ^ 世界保健機関 2009, p. 40-41.
- ^ Mayo-Smith, Michael F. (July 1997). “Pharmacological management of alcohol withdrawal. A meta-analysis and evidence-based practice guideline. American Society of Addiction Medicine Working Group on Pharmacological Management of Alcohol Withdrawal.” (pdf). JAMA 278 (2): 144. doi:10.1001/jama.1997.03550020076042.
- ^ a b Jorge R. Petit 著、山内俊雄(監修) 編『精神科救急のすべて』深津亮・松木秀幸(監訳)、新興医学出版社、2011年4月、214-224頁。ISBN 978-4880027210。、Handbook of Emergency Psychiatry, 2004
- ^ 英国精神薬理学会 2012.
- ^ 笠陽一郎、誤診・誤処方を受けた患者とその家族たち『精神科セカンドオピニオン―正しい診断と処方を求めて』シーニュ、2008年7月。ISBN 978-4-9903014-1-5。
- ^ Lindsay, S.J.E.; Powell, Graham E., eds (1998-07-28). The Handbook of Clinical Adult Psychology (2nd ed.). Routledge. p. 363. ISBN 978-0-415-07215-1
- ^ Authier, N.; Balayssac, D.; Sautereau, M.; Zangarelli, A.; Courty, P.; Somogyi, A.A.; Vennat, B.; Llorca, P.-M. et al. (2009). “Benzodiazepine dependence: Focus on withdrawal syndrome”. Annales Pharmaceutiques Françaises 67 (6): 408–13. doi:10.1016/j.pharma.2009.07.001. PMID 19900604.
- ^ a b Committee on Safety of Medicines (2007年). “Hypnotics and anxiolytics”. British National Formulary. 2007年9月17日閲覧。(要登録)
- ^ a b c Murphy, S. M.; Tyrer, P. (1991). “A double-blind comparison of the effects of gradual withdrawal of lorazepam, diazepam and bromazepam in benzodiazepine dependence”. The British Journal of Psychiatry 158 (4): 511–6. doi:10.1192/bjp.158.4.511. PMID 1675901.
- ^ Adam, Kirstine; Oswald, I. (2008). “Can a Rapidly-eliminated Hypnotic Cause Daytime Anxiety?”. Pharmacopsychiatry 22 (3): 115–9. doi:10.1055/s-2007-1014592. PMID 2748714.
- ^ Scharf, Martin B; Kales, Judith A; Bixler, EO; Jacoby, JA; Schweitzer, PK (1982). “Lorazepam—Efficacy, side effects, and rebound phenomena”. Clinical Pharmacology and Therapeutics 31 (2): 175–9. doi:10.1038/clpt.1982.27. PMID 6120058.
- ^ Walsh, James K; Schweitzer, Paula K; Parwatikar, Sadashiv (1983). “Effects of lorazepam and its withdrawal on sleep, performance, and subjective state”. Clinical Pharmacology and Therapeutics 34 (4): 496–500. doi:10.1038/clpt.1983.203. PMID 6617072.
- ^ Fontaine, Réjean; Beaudry, Paul; Le Morvan, Patrick LE; Beauclair, Linda; Chouinard, GUY (1990). “Zopiclone and Triazolam in Insomnia Associated with Generalized Anxiety Disorder”. International Clinical Psychopharmacology 5 (3): 173–83. doi:10.1097/00004850-199007000-00002. PMID 2230061.
- ^ Kales, Anthony; Bixler, Edward O.; Soldatos, Constantin R.; Jacoby, Judith A.; Kales, Joyce D. (1986). “Lorazepam: Effects on Sleep and Withdrawal Phenomena”. Pharmacology 32 (3): 121–30. doi:10.1159/000138160. PMID 3960963.
- ^ Bonnet, M H; Arand, D L (1999). “The use of lorazepam TID for chronic insomnia”. International Clinical Psychopharmacology 14 (2): 81–9. doi:10.1097/00004850-199903000-00004. PMID 10220122.
- ^ Kales, Anthony; Manfredi, Rocco L; Vgontzas, Alexandras N; Bixler, Edward O; Vela-Bueno, Antonio; Fee, Eric C (1991). “Rebound insomnia after only brief and intermittent use of rapidly eliminated benzodiazepines”. Clinical Pharmacology and Therapeutics 49 (4): 468–76. doi:10.1038/clpt.1991.55. PMID 2015735.
- ^ a b c d e f g h i j k l m n o p q r s t u v Saxon, L.; Hjemdahl, P.; Hiltunen, A. J.; Borg, S. (1997). “Effects of flumazenil in the treatment of benzodiazepine withdrawal - a double-blind pilot study”. Psychopharmacology 131 (2): 153–60. doi:10.1007/s002130050278. PMID 9201803.
- ^ Terao, T; Yoshimura, R; Terao, M; Abe, K (1992). “Depersonalization following nitrazepam withdrawal”. Biological Psychiatry 31 (2): 212–3. doi:10.1016/0006-3223(92)90209-I. PMID 1737083.
- ^ Lader, Malcolm (1994). “Anxiety or depression during withdrawal of hypnotic treatments”. Journal of Psychosomatic Research 38: 113–23; discussion 118–23. doi:10.1016/0022-3999(94)90142-2. PMID 7799243.
- ^ a b c d e Mintzer, M. Z.; Stoller, K. B.; Griffiths, R. R. (1999). “A controlled study of flumazenil-precipitated withdrawal in chronic low-dose benzodiazepine users”. Psychopharmacology 147 (2): 200–9. doi:10.1007/s002130051161. PMID 10591888.
- ^ Mendelson, WB; Weingartner, H; Greenblatt, DJ; Garnett, D; Gillin, JC (1982). “A clinical study of flurazepam”. Sleep 5 (4): 350–60. PMID 6761826.
- ^ Schöpf, J. (2008). “Withdrawal Phenomena after Long-term Administration of Benzodiazepines a Review of Recent Investigations”. Pharmacopsychiatry 16 (1): 1–8. doi:10.1055/s-2007-1017439. PMID 6131447.
- ^ a b Shader, RI; Greenblatt, DJ (1981). “The use of benzodiazepines in clinical practice”. British Journal of Clinical Pharmacology 11 Suppl 1 (Suppl 1): 5S–9S. PMC 1401641. PMID 6133535.
- ^ Mintzer, Miriam Z.; Griffiths, Roland R. (2004). “Flumazenil-precipitated withdrawal in healthy volunteers following repeated diazepam exposure”. Psychopharmacology 178 (2–3): 259–67. doi:10.1007/s00213-004-2009-1. PMID 15452683.
- ^ a b Loeb, P; Adnet, P; Boittiaux, P; Forget, AP; Mille, FX (1997). “Sevrage en benzodiazépines révélé par un syndrome douloureux abdominal pseudochirurgical [Benzodiazepine withdrawal masquerading as surgical abdominal syndrome]” (French). Annales Françaises d'Anesthésie et de Réanimation 16 (5): 521–2. doi:10.1016/S0750-7658(97)83345-X.
- ^ http://www.benzo.org.uk/manual/bzcha03.htm#16[要文献特定詳細情報]
- ^ a b c d e f Pelissolo, A; Bisserbe, JC (1994). “Dependence on benzodiazepines. Clinical and biological aspects”. L'Encephale 20 (2): 147–57. PMID 7914165.
- ^ Biswas, AK; Feldman, BL; Davis, DH; Zintz, EA (2005). “Myocardial ischemia as a result of severe benzodiazepine and opioid withdrawal”. Clinical toxicology (Philadelphia, Pa.) 43 (3): 207–9. PMID 15902797.
- ^ a b c d e Bismuth, C; Le Bellec, M; Dally, S; Lagier, G (1980). “Benzodiazepine physical dependence. 6 cases (author's transl)”. La Nouvelle presse medicale 9 (28): 1941–5. PMID 6106922.
- ^ Pecknold, J.C. (1993). “Discontinuation reactions to alprazolam in panic disorder”. Journal of Psychiatric Research 27: 155. doi:10.1016/0022-3956(93)90025-W.
- ^ Kliniska Färdigheter: Informationsutbytet Mellan Patient Och Läkare, LINDGREN, STEFAN, ISBN 91-44-37271-X (Swedish)[要ページ番号]
- ^ Drummond, Lynne M.; Matthews, Helen P. (1988). “SINGLE CASE STUDY Obsessive-Compulsive Disorder Occurring as a Complication in Benzodiazepine Withdrawal”. The Journal of Nervous and Mental Disease 176 (11): 688–91. doi:10.1097/00005053-198811000-00008. PMID 3183654.
- ^ Matthews, HP; Drummond, LM (1987). “Obsessive-compulsive disorder--a complication of benzodiazepine withdrawal”. The British journal of psychiatry 150: 272. PMID 3651695.
- ^ Pagel, J. F.; Parnes, Bennett L. (2001), “Medications for the Treatment of Sleep Disorders”, The Primary Care Companion to the Journal of Clinical Psychiatry 3 (3): 118–125, doi:10.4088/PCC.v03n0303, PMC 181172, PMID 15014609
- ^ Van Engelen, BG; Gimbrere, JS; Booy, LH (1993). “Benzodiazepine withdrawal reaction in two children following discontinuation of sedation with midazolam”. The Annals of pharmacotherapy 27 (5): 579–81. PMID 8347907.
- ^ a b Beeley, L (1991). “Benzodiazepines and tinnitus”. BMJ 302 (6790): 1465. doi:10.1136/bmj.302.6790.1465.
- ^ Mellor, CS; Jain, VK (1982). “Diazepam withdrawal syndrome: Its prolonged and changing nature”. Canadian Medical Association journal 127 (11): 1093–6. PMC 1862031. PMID 7139456.
- ^ Olajide, Dele; Lader, Malcolm (2009). “Depression following withdrawal from long-term benzodiazepine use: A report of four cases”. Psychological Medicine 14 (4): 937–40. doi:10.1017/S0033291700019899. PMID 6152745.
- ^ Rosebush, Patricia I.; Mazurek, Michael F. (1996). “Catatonia After Benzodiazepine Withdrawal”. Journal of Clinical Psychopharmacology 16 (4): 315–9. doi:10.1097/00004714-199608000-00007. PMID 8835707.
- ^ Deuschle, M.F.; Lederbogen, F (2001). “Benzodiazepine Withdrawal - Induced Catatonia”. Pharmacopsychiatry 34 (1): 41–2. doi:10.1055/s-2001-15188. PMID 11229621.
- ^ Kanemoto, Kousuke; Miyamoto, Toshio; Abe, Ryuji (1999). “Ictal catatonia as a manifestation of de novo absence status epilepticus following benzodiazepine withdrawal”. Seizure 8 (6): 364–6. doi:10.1053/seiz.1999.0309. PMID 10512781.
- ^ Uhlenhuth EH; Starcevic V, Qualls C, Antal EJ, Matuzas W, Javaid JI, Barnhill J (October 2006). “Abrupt discontinuation of alprazolam and cognitive style in patients with panic disorder: early effects on mood, performance, and vital signs”. J Clin Psychopharmacol 26 (5): 519–523. doi:10.1097/01.jcp.0000236653.85791.60. PMID 16974197.
- ^ Metten, Pamela; Crabbe, John C (1999). “Genetic Determinants of Severity of Acute Withdrawal from Diazepam in Mice”. Pharmacology Biochemistry and Behavior 63 (3): 473–9. doi:10.1016/S0091-3057(99)00017-9. PMID 10418790.
- ^ Haque, W; Watson, DJ; Bryant, SG (1990). “Death following suspected alprazolam withdrawal seizures: A case report”. Texas medicine 86 (1): 44–7. PMID 2300914.
- ^ Provini, F.; Cortelli, P.; Montagna, P.; Gambetti, P.; Lugaresi, E. (2008). “Fatal insomnia and agrypnia excitata: Sleep and the limbic system”. Revue Neurologique 164 (8–9): 692–700. doi:10.1016/j.neurol.2007.11.003. PMID 18805303.
- ^ a b Berezak, A.; Weber, M.; Hansmann, J.; Tulasne, P.A.; Laporte, B.; Ould Ouali, A. (1984). “Dépendance physique aux benzodiazépines dans un contexte traumatologique [Benzodiazepine physical dependence in traumatology]” (French). Annales Françaises d'Anesthésie et de Réanimation 3 (5): 383–4. doi:10.1016/S0750-7658(84)80078-7.
- ^ Keshavan, MS; Moodley, P; Eales, M; Joyce, E; Yeragani, VK (1988). “Delusional depression following benzodiazepine withdrawal”. Canadian journal of psychiatry 33 (7): 626–7. PMID 3197017.
- ^ Risse, SC; Whitters, A; Burke, J; Chen, S; Scurfield, RM; Raskind, MA (1990). “Severe withdrawal symptoms after discontinuation of alprazolam in eight patients with combat-induced posttraumatic stress disorder”. The Journal of clinical psychiatry 51 (5): 206–9. PMID 2335496.
- ^ Turkington, Douglas; Gill, Paul (1989). “Mania induced by lorazepam withdrawal: A report of two cases”. Journal of Affective Disorders 17 (1): 93–5. doi:10.1016/0165-0327(89)90028-1. PMID 2525581.
- ^ Lapierre, YD; Labelle, A (1987). “Manic-like reaction induced by lorazepam withdrawal”. Canadian journal of psychiatry 32 (8): 697–8. PMID 3690487.
- ^ Kawajiri, M; Ohyagi, Y; Furuya, H; Araki, T; Inoue, N; Esaki, S; Yamada, T; Kira, J (2002). “A patient with Parkinson's disease complicated by hypothyroidism who developed malignant syndrome after discontinuation of etizolam”. Rinsho shinkeigaku 42 (2): 136–9. PMID 12424963.
- ^ Strawn, Jeffrey; Keck Jr, PE; Caroff, SN (2007). “Neuroleptic Malignant Syndrome”. American Journal of Psychiatry 164 (6): 870–6. doi:10.1176/appi.ajp.164.6.870. PMID 17541044.
- ^ Khan, A; Joyce, P; Jones, AV (1980). “Benzodiazepine withdrawal syndromes”. The New Zealand medical journal 92 (665): 94–6. PMID 6107888.
- ^ Peh, LH; Mahendran, R (1989). “Psychiatric complications of Erimin abuse”. Singapore medical journal 30 (1): 72–3. PMID 2595393.
- ^ Fruensgaard, K. (1976). “Withdrawal Psychosis: A Study of 30 Consecutive Cases”. Acta Psychiatrica Scandinavica 53 (2): 105–18. doi:10.1111/j.1600-0447.1976.tb00065.x. PMID 3091.
- ^ Einarson, A; Selby, P; Koren, G (2001). “Abrupt discontinuation of psychotropic drugs during pregnancy: Fear of teratogenic risk and impact of counselling”. Journal of psychiatry & neuroscience 26 (1): 44–8. PMC 1408034. PMID 11212593.
- ^ Joughin, N.; Tata, P.; Collins, M.; Hooper, C.; Falkowski, J. (1991). “In-patient withdrawal from long-term benzodiazepine use”. Addiction 86 (4): 449–55. doi:10.1111/j.1360-0443.1991.tb03422.x. PMID 1675899.
- ^ Citrome, Leslie; Volavka, Jan (1999). “Violent Patients in the Emergency Setting”. Psychiatric Clinics of North America 22 (4): 789–801. doi:10.1016/S0193-953X(05)70126-X. PMID 10623971.
- ^ Vorma, H; Naukkarinen, Hh; Sarna, Sj; Kuoppasalmi, Ki (2005). “Predictors of benzodiazepine discontinuation in subjects manifesting complicated dependence.”. Substance use & misuse 40 (4): 499-510. doi:10.1081/JA-200052433. PMID 15830732.
- ^ Stephens DN (August 1995). “A glutamatergic hypothesis of drug dependence: extrapolations from benzodiazepine receptor ligands”. Behav Pharmacol 6 (5 And 6): 425-446. PMID 11224351.
- ^ Dunworth SJ, Mead AN, Stephens DN (April 2000). “Previous experience of withdrawal from chronic diazepam ameliorates the aversiveness of precipitated withdrawal and reduces withdrawal-induced c-fos expression in nucleus accumbens”. Eur. J. Neurosci. 12 (4): 1501-1508. doi:10.1046/j.1460-9568.2000.00036.x. PMID 10762378.
- ^ Rickels K, Schweizer E, Csanalosi I, Case WG, Chung H (May 1988). “Long-term treatment of anxiety and risk of withdrawal. Prospective comparison of clorazepate and buspirone”. Arch. Gen. Psychiatry 45 (5): 444-450. PMID 2895993.
- ^ mhGAP Intervention Guide for mental, neurological and substance use disorders in non-specialized health settings (Report). 世界保健機関. 2010. DRU. ISBN 9789241548069。
- ^ a b c Parr, Jannette M.; Kavanagh, David J.; Cahill, Lareina; Mitchell, Geoffrey; Mcd Young, Ross McD. (2009). “Effectiveness of current treatment approaches for benzodiazepine discontinuation: A meta-analysis”. Addiction 104 (1): 13–24. doi:10.1111/j.1360-0443.2008.02364.x. PMID 18983627.
- ^ Dou C, Rebane J, Bardal S (January 2018). “Interventions to improve benzodiazepine tapering success in the elderly: a systematic review”. Aging Ment Health: 1–6. doi:10.1080/13607863.2017.1423030. PMID 29336611.
- ^ Garfinkel, Doron; Zisapel, N; Wainstein, J; Laudon, M (1999). “Facilitation of Benzodiazepine Discontinuation by Melatonin: A New Clinical Approach”. Archives of Internal Medicine 159 (20): 2456–60. doi:10.1001/archinte.159.20.2456. PMID 10665894.
- ^ Nakao, Mutsuhiro; Takeuchi, Takeaki; Nomura, Kyoko; Teramoto, Tamio; Yano, Eiji (2006). “Clinical application of paroxetine for tapering benzodiazepine use in non-major-depressive outpatients visiting an internal medicine clinic”. Psychiatry and Clinical Neurosciences 60 (5): 605–10. doi:10.1111/j.1440-1819.2006.01565.x. PMID 16958945.
- ^ Rickels, K.; Schweizer, E.; Garcia España, F.; Case, G.; Demartinis, N.; Greenblatt, D. (1999). “Trazodone and valproate in patients discontinuing long-term benzodiazepine therapy: Effects on withdrawal symptoms and taper outcome”. Psychopharmacology 141 (1): 1–5. doi:10.1007/s002130050798. PMID 9952057.
- ^ a b Baandrup L, Ebdrup BH, Rasmussen JØ, Lindschou J, Gluud C, Glenthøj BY (March 2018). “Pharmacological interventions for benzodiazepine discontinuation in chronic benzodiazepine users”. Cochrane Database Syst Re: CD011481. doi:10.1002/14651858.CD011481.pub2. PMID 29543325.
- ^ a b c Lader, Malcolm; Tylee, Andre; Donoghue, John (2009). “Withdrawing Benzodiazepines in Primary Care”. CNS Drugs 23 (1): 19–34. doi:10.2165/0023210-200923010-00002. PMID 19062773.
- ^ Schweizer, Edward; Rickels, K; Case, WG; Greenblatt, DJ (1990). “Long-term Therapeutic Use of Benzodiazepines: II. Effects of Gradual Taper”. Archives of General Psychiatry 47 (10): 908–15. doi:10.1001/archpsyc.1990.01810220024003. PMID 2222130.
- ^ Fruensgaard, K (1977). “Withdrawal psychosis after drugs. Report of a consecutive material”. Ugeskrift for laeger 139 (29): 1719–22. PMID 898354.
- ^ Tagashira, Eijiro; Hiramori, Tameo; Urano, Tomoko; Nakao, Kenzo; Yanaura, Saizo (1981). “Enhancement of drug withdrawal convulsion by combinations of phenobarbital and antipsychotic agents”. The Japanese Journal of Pharmacology 31 (5): 689–99. doi:10.1254/jjp.31.689. PMID 6118452.
- ^ Bobolakis, Ioannis (2000). “Neuroleptic Malignant Syndrome After Antipsychotic Drug Administration During Benzodiazepine Withdrawal”. Journal of Clinical Psychopharmacology 20 (2): 281–3. doi:10.1097/00004714-200004000-00033. PMID 10770479.
- ^ Randall, Michael D; Neil, Karen E (February 2004). “5”. Disease management (1 ed.). Pharmaceutical Press. p. 62. ISBN 978-0-85369-523-3 2009年6月1日閲覧。
- ^ Ebadi, Manuchair (2007-10-23). “Alphabetical presentation of drugs”. Desk Reference for Clinical Pharmacology (2nd ed.). USA: CRC Press. p. 512. ISBN 978-1-4200-4743-1
- ^ Higgitt, A.; Fonagy, P.; Lader, M. (2009). “The natural history of tolerance to the benzodiazepines”. Psychological Medicine. Monograph Supplement 13: 1–55. doi:10.1017/S0264180100000412. PMID 2908516.
- ^ “Wellbutrin XL Prescribing Information” (PDF). GlaxoSmithKline (December 2008). 2009年3月26日時点のオリジナルよりアーカイブ。2010年1月16日閲覧。
- ^ Seale, Thomas W.; Carney, John M.; Rennert, Owen M.; Flux, Marinus; Skolnick, Phil (1987). “Coincidence of seizure susceptibility to caffeine and to the benzodiazepine inverse agonist, DMCM, in SWR and CBA inbred mice”. Pharmacology Biochemistry and Behavior 26 (2): 381–7. doi:10.1016/0091-3057(87)90133-X. PMID 3575358.
- ^ “FLUMAZENIL injection, solution [APP Pharmaceuticals, LLC]”. Daily Med (2012年8月23日). 2014年3月15日閲覧。
- ^ a b Denis, Cecile; Fatseas, Melina; Lavie, Estelle; Auriacombe, Marc (2006). “Pharmacological interventions for benzodiazepine mono-dependence management in outpatient settings”. In Denis, Cecile. Cochrane Database of Systematic Reviews. pp. CD005194. doi:10.1002/14651858.CD005194.pub2. PMID 16856084.
- ^ Gerra, G.; Zaimovic, A.; Giusti, F.; Moi, G.; Brewer, C. (2002). “Intravenous flumazenil versus oxazepam tapering in the treatment of benzodiazepine withdrawal: A randomized, placebo-controlled study”. Addiction Biology 7 (4): 385–95. doi:10.1080/1355621021000005973. PMID 14578014.
- ^ Little, H.J. (1991). “The benzodiazepines: Anxiolytic and withdrawal effects”. Neuropeptides 19: 11–4. doi:10.1016/0143-4179(91)90077-V. PMID 1679209.
- ^ Lader, M. H.; Morton, S. V. (1992). “A pilot study of the effects of flumazenil on symptoms persisting after benzodiazepine withdrawal”. Journal of Psychopharmacology 6 (3): 357–63. doi:10.1177/026988119200600303. PMID 22291380.
- ^ Roche USA (October 2007). “Romazicon” (PDF). Roche Pharmaceuticals USA. 2008年6月25日時点のオリジナルよりアーカイブ。2011年5月27日閲覧。
- ^ “Blocking the high: one man’s quixotic quest to cure addiction”. mosaicscience.com (2015年3月17日). 2017年2月19日閲覧。
- ^ McConnell, John Girvan (2008). “Benzodiazepine tolerance, dependency, and withdrawal syndromes and interactions with fluoroquinolone antimicrobials”. British Journal of General Practice 58 (550): 365–6. doi:10.3399/bjgp08X280317. PMC 2435654. PMID 18482496.
- ^ Unseld, E; Ziegler, G; Gemeinhardt, A; Janssen, U; Klotz, U (1990). “Possible interaction of fluoroquinolones with the benzodiazepine-GABAA- receptor complex”. British Journal of Clinical Pharmacology 30 (1): 63–70. doi:10.1111/j.1365-2125.1990.tb03744.x. PMC 1368276. PMID 2167717.
- ^ Sternbach, Harvey; State, Rosanne (1997). “Antibiotics: Neuropsychiatric Effects and Psychotropic Interactions”. Harvard Review of Psychiatry 5 (4): 214–26. doi:10.3109/10673229709000304. PMID 9427014.
- ^ Committee on Safety of Medicines; Medicines and Healthcare products Regulatory Agency (2008年). “Quinolones”. United Kingdom: British National Formulary. 2012年6月30日時点のオリジナルよりアーカイブ。2009年2月16日閲覧。(要登録)
- ^ Wong, PT (1993). “Interactions of indomethacin with central GABA systems”. Archives internationales de pharmacodynamie et de therapie 324: 5–16. PMID 8297186.
- ^ Delanty, Norman (November 2001). “Medication associated seizures”. Seizures: Medical Causes and Management. Humana Press. pp. 152–153. ISBN 0-89603-827-0
- ^ Green, M. A.; Halliwell, R. F. (1997). “Selective antagonism of the GABAAreceptor by ciprofloxacin and biphenylacetic acid”. British Journal of Pharmacology 122 (3): 584–90. doi:10.1038/sj.bjp.0701411. PMC 1564969. PMID 9351519.
- ^ Auta J, Costa E, Davis JM, Guidotti A (September 2005). “Imidazenil: an antagonist of the sedative but not the anticonvulsant action of diazepam”. Neuropharmacology 49 (3): 425-429. doi:10.1016/j.neuropharm.2005.04.005. PMID 15964602.
- ^ Sullivan, Mark; Toshima, Michelle; Lynn, Pamela; Roy-Byrne, Peter (1993). “Phenobarbital Versus Clonazepam for Sedative-Hypnotic Taper in Chronic Pain Patients: A Pilot Study”. Annals of Clinical Psychiatry 5 (2): 123–8. doi:10.3109/10401239309148974. PMID 8348204.
- ^ Dr Ray Baker. “Dr Ray Baker's Article on Addiction: Benzodiazepines in Particular”. 2009年2月14日閲覧。
- ^ Oulis, P.; Konstantakopoulos, G. (2010). “Pregabalin in the treatment of alcohol and benzodiazepines dependence.”. CNS Neurosci Ther 16 (1): 45–50. doi:10.1111/j.1755-5949.2009.00120.x. PMID 20070788.
- ^ Oulis, P.; Konstantakopoulos, G. (Jul 2012). “Efficacy and safety of pregabalin in the treatment of alcohol and benzodiazepine dependence.”. Expert Opin Investig Drugs 21 (7): 1019–29. doi:10.1517/13543784.2012.685651. PMID 22568872.
- ^ Zitman, F. G.; Couvée, JE (2001). “Chronic benzodiazepine use in general practice patients with depression: An evaluation of controlled treatment and taper-off: Report on behalf of the Dutch Chronic Benzodiazepine Working Group”. The British Journal of Psychiatry 178 (4): 317–24. doi:10.1192/bjp.178.4.317. PMID 11282810.
- ^ British National Formulary; Committee on Safety of Medicines. “Hypnotics and anxiolytics”. BNF.org. 2008年9月5日閲覧。
- ^ Tönne, U.; Hiltunen, A. J.; Vikander, B.; Engelbrektsson, K.; Bergman, H.; Bergman, I.; Leifman, H.; Borg, S. (1995). “Neuropsychological changes during steady-state drug use, withdrawal and abstinence in primary benzodiazepine-dependent patients”. Acta Psychiatrica Scandinavica 91 (5): 299–304. doi:10.1111/j.1600-0447.1995.tb09786.x. PMID 7639085.
- ^ Kan, CC; Mickers, FC; Barnhoorn, D (2006). “Short- and long-term results of a systematic benzodiazepine discontinuation programme for psychiatric patients”. Tijdschrift voor psychiatrie 48 (9): 683–93. PMID 17007474.
- ^ Jørgensen, VR (2009). “Benzodiazepine reduction does not imply an increased consumption of antidepressants. A survey of two medical practices”. Ugeskrift for laeger 171 (41): 2999–3003. PMID 19814928.
- ^ Lal R, Gupta S, Rao R, Kattimani S (2007). “Emergency management of substance overdose and withdrawal” (PDF). Substance Use Disorder. World Health Organisation. p. 82. オリジナルの2010年6月13日時点におけるアーカイブ。 2009年6月6日閲覧. "Generally, a longer-acting benzodiazepine such as chlordiazepoxide or diazepam is used and the initial dose titrated downward"
- ^ Noyes, Russell; Perry, Paul J.; Crowe, Raymond R.; Coryell, William H.; Clancy, John; Yamada, Thoru; Gabel, Janelle (1986). “Seizures Following the Withdrawal of Alprazolam”. The Journal of Nervous and Mental Disease 174 (1): 50–2. doi:10.1097/00005053-198601000-00009. PMID 2867122.
- ^ Noyes Jr, R; Clancy, J; Coryell, WH; Crowe, RR; Chaudhry, DR; Domingo, DV (1985). “A withdrawal syndrome after abrupt discontinuation of alprazolam”. The American Journal of Psychiatry 142 (1): 114–6. PMID 2857066.
- ^ Rickels, Karl; Schweizer, E; Case, WG; Greenblatt, DJ (1990). “Long-term Therapeutic Use of Benzodiazepines: I. Effects of Abrupt Discontinuation”. Archives of General Psychiatry 47 (10): 899–907. doi:10.1001/archpsyc.1990.01810220015002. PMID 2222129.
- ^ Neale, G; Smith, AJ (2007). “Self-harm and suicide associated with benzodiazepine usage”. The British journal of general practice 57 (538): 407–8. PMC 2047018. PMID 17504594.
- ^ Curran, H. V.; Bond, A.; O'Sullivan, G.; Bruce, M.; Marks, I.; Lelliot, P.; Shine, P.; Lader, M. (2009). “Memory functions, alprazolam and exposure therapy: A controlled longitudinal study of agoraphobia with panic disorder”. Psychological Medicine 24 (4): 969–76. doi:10.1017/S0033291700029056. PMID 7892364.
- ^ Busto, Usoa; Fornazzari, Luis; Naranjo, Claudio A. (1988). “Protracted Tinnitus after Discontinuation of Long-Term Therapeutic Use of Benzodiazepines”. Journal of Clinical Psychopharmacology 8 (5): 359–362. doi:10.1097/00004714-198810000-00010. PMID 2903182.
- ^ Higgitt, A.; Fonagy, P.; Toone, B.; Shine, P. (1990). “The prolonged benzodiazepine withdrawal syndrome: Anxiety or hysteria?”. Acta Psychiatrica Scandinavica 82 (2): 165–8. doi:10.1111/j.1600-0447.1990.tb01375.x. PMID 1978465.
- ^ Ashton CH (March 1995). “Protracted Withdrawal From Benzodiazepines: The Post-Withdrawal Syndrome”. Psychiatric Annals (benzo.org.uk) 25 (3): 174–179.
- ^ Barker, M; Greenwood, KM; Jackson, M; Crowe, SF (2004). “Persistence of cognitive effects after withdrawal from long-term benzodiazepine use: A meta-analysis”. Archives of Clinical Neuropsychology 19 (3): 437–54. doi:10.1016/S0887-6177(03)00096-9. PMID 15033227.
- ^ L. Saxon, S. Borg & A. J. Hiltunen (August 2010). “Reduction of aggression during benzodiazepine withdrawal: effects of flumazenil”. Pharmacology, biochemistry, and behavior 96 (2): 148–151. doi:10.1016/j.pbb.2010.04.023. PMID 20451546.
- ^ Hood HM, Metten P, Crabbe JC, Buck KJ (February 2006). “Fine mapping of a sedative-hypnotic drug withdrawal locus on mouse chromosome 11”. Genes, Brain and Behavior 5 (1): 1-10. doi:10.1111/j.1601-183X.2005.00122.x. PMID 16436183.
- ^ Baillargeon L, Landreville P, Verreault R, Beauchemin JP, Grégoire JP, Morin CM (November 2003). “Discontinuation of benzodiazepines among older insomniac adults treated with cognitive-behavioural therapy combined with gradual tapering: a randomized trial” (PDF). CMAJ 169 (10): 1015–1020. PMC 236226. PMID 14609970.
- ^ Salzman, Carl (2004-05-15). Clinical geriatric psychopharmacology (4th ed.). USA: Lippincott Williams & Wilkins. pp. 450–453. ISBN 978-0-7817-4380-8
- ^ 『重篤副作用疾患別対応マニュアル - 新生児薬物離脱症候群 (PDF)』(レポート)、厚生労働省、2010年3月。
参考文献
[編集]- 臨床ガイドライン
-
- 世界保健機関 (2009-09-31), Clinical Guidelines for Withdrawal Management and Treatment of Drug Dependence in Closed Settings, ISBN 978-92-9061-430-2
- WHO Programme on Substance Abuse (1996年11月). Rational use of benzodiazepines - Document no.WHO/PSA/96.11 (pdf) (Report). World Health Organization. OCLC 67091696. 2013年3月10日閲覧。
- コロンビア大学嗜癖物質乱用国立センター (2012-06). Addiction Medicine: Closing the Gap between Science and Practice
- 英国国立薬物乱用治療庁 (2007年). Drug misuse and dependence - UK guidelines on clinical management (PDF) (Report).
- Davidson B et al; NHS Grampian (2006年). Guidance for prescribing and withdrawal of benzodiazepines and hypnotics in general practice (PDF) (Report). 英国国民医薬品集. 2012年6月20日時点のオリジナル (PDF)よりアーカイブ。
- 英国精神薬理学会; AR Lingford-Hughes, S Welch, L Peters and DJ Nutt (July 2012). “BAP updated guidelines: evidence-based guidelines for the pharmacological management of substance abuse, harmful use, addiction and comorbidity: recommendations from BAP” (pdf). Journal of Psychopharmacology 26 (7): 899–952. doi:10.1177/0269881112444324. PMID 22628390. オリジナルの2012年12月3日時点におけるアーカイブ。.
- Professor Heather Ashton (2002), Benzodiazepines: How They Work and How to Withdraw
- ヘザー・アシュトン『ベンゾジアゼピン - それはどのように作用し、離脱するにはどうすればよいか』(pdf)Professor C H Ashton、2002年8月。、(邦訳は2012年8月19日に公開され、出典論文が省略されている)
- その他
-
- 英国精神薬理学会; Nutt, David; Baldwin, David; Aitchison, Katherine (2013). “Benzodiazepines: Risks and benefits. A reconsideration” (pdf). J Psychopharmacol 27 (11): Epub 2013 Sep 24. doi:10.1177/0269881113503509. PMID 24067791. オリジナルの2015年9月2日時点におけるアーカイブ。.
- 中川敦夫ら『向精神薬の処方実態に関する国内外の比較研究(平成22年度総括・分担研究報告書厚生労働科学研究費補助金厚生労働科学特別研究事業)』(pdf)2011年3月。
関連項目
[編集]外部リンク
[編集]- Benzodiazepine poisoning and withdrawal - UpToDate
- Benzodiazepine Information Coalition
- Benzodiazepine Tapering Strategies and Solutions 日本語訳 (2017) ベンゾジアゼピン離脱問題を扱うコミュニティのメディカルアドバイザリーボードでは、マイクロテーパリングでの微量づつ減薬する方法を考案している。
- ベンゾジアゼピン情報センター