胚中心
| 胚中心 | |
|---|---|
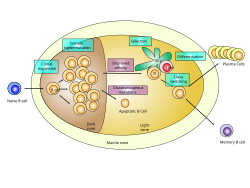 B細胞の増殖および発達段階を示すリンパ節の胚中心の模式図。 | |
| MeSH | D018858 |
| グレイ解剖学 | p.689 |
| 解剖学用語 | |
胚中心(はいちゅうしん、英: germinal centers or germinal centres、GC)または胚芽中心(はいがちゅうしん)は、二次リンパ系臓器(リンパ節、回腸パイエル板、脾臓など)のB細胞領域(濾胞; ろほう)内に形成される一過性の構造である[1]。ここでは正常な免疫応答の間に成熟したB細胞が活性化され、増殖、分化、抗体遺伝子の変異(より高い親和性を目的した体細胞超変異)が行われる。胚中心B細胞(BGC)のほとんどは、可染体マクロファージよって除去される[2]。B細胞は、T依存性抗原(胸腺依存性抗原)によって濾胞B細胞が活性化された後、動的に発達する。
胚中心内で、暗帯(dark zone)にあるB細胞は、急速で突然変異的な細胞分裂を行うため、中心芽細胞(centroblasts)と呼ばれる。これらのB細胞が増殖を停止して明帯(light zone)に移動すると、中心細胞(centrocytes)と呼ばれ、濾胞樹状細胞(FDC)の存在下で濾胞ヘルパーT(TFH)細胞による選択を受けるようになる。このように、胚中心はB細胞の体液性免疫応答において重要な役割を果たしており、抗原(感染病原体など)を効果的に認識する改良された抗体の産生に特化した親和性成熟B細胞の生成や、長寿形質細胞および耐久メモリーB細胞の産生で、中心的な工場としての機能を果たしている。
プロセス
[編集]- リンパ節内では、成熟した末梢性B細胞(濾胞(Fo)B細胞と呼ばれる)が、FDCから抗原を獲得し、濾胞間T細胞領域とB細胞領域を分ける境界(リンパ濾胞とも呼ばれる)で、同族のCD4+TFH細胞にその抗原を提示する。
- 数回の細胞分裂の後、B細胞は体細胞超変異を起こし、抗体をコードするDNAを変異させ、胚中心部に多様なクローンを産生する。これには、B細胞が産生する抗体の抗原認識表面をコードする領域に偏った疑似ランダム置換を伴う。この現象は、抗原認識後に親和性の高い抗体が産生および選択されるという親和性成熟のプロセスを明確に示している。
- 成熟したB細胞(中心芽細胞)は、未知の刺激を受けると暗帯から明帯に移動し、自らの細胞表面に編集したB細胞受容体(BCR)を発現し始め、この段階では中心細胞と呼ばれる。中心細胞は活性化アポトーシスの状態にあり、FDCおよびTFH細胞に由来する生存シグナルを求めて競合する。 胚中心選択と呼ばれるこの救済プロセスは、抗原に対する表面抗体の親和性に依存すると考えられている。このように、抗原に対する親和性がより高い表面抗体を与える突然変異をうまく獲得したB細胞は、親和性がより低いB細胞クローンや有害な突然変異を獲得したB細胞よりも生存の優位性を得ることができる。また、選択されなかったB細胞の変異体は、中心芽細胞として暗帯に周期的に再入することで、抗原への親和性を高めるためにさらに変異を獲得する機会が生まれる。T細胞との相互作用もまた、自己反応性胚中心B細胞の生成を妨げると考えられている[3]。
- 成熟したB細胞は、中心芽細胞-中心細胞間の循環の不明確な段階で、最終分化シグナルを受け取り、抗体産生形質細胞(大量の抗体を分泌する細胞)または、同じ抗原に再度接触した際に再活性化できるメモリーB細胞として胚中心を出る。選択されたB細胞は、中心細胞の変異分枝および選択の全サイクルを再開することもある。このようにして、適応免疫系は、部分的にこれらの胚中心反応を介して、時間の経過とともに徐々に抗原をよりよく認識できるようになる。
さまざまな段階での形態
[編集]胚中心の形態は非常に特異的であり、反応のさまざまな段階で特徴的な特性を示す。
- 反応の初期段階では、FDCのネットワークは増殖中のB細胞で完全に満たされている。
- その後、反応の4日目になると、胚中心は暗帯と明帯という2つの領域の分離を示す[4]。前者はまだ増殖と変異が優位なB細胞を含み、後者はB細胞が選択される領域である。
- これらの領域は、胚中心が発生してから10日後に解消され、約3週間後に消滅する。
医学的関連性
[編集]胚中心は適応免疫系の重要な構造であるため、その調整解除は、たとえば関節リウマチ、免疫不全、DLBCLやバーキットリンパ腫などの多くのリンパ腫などの多くの免疫疾患に関与している。
参照項目
[編集]- リンパ系
- 可染体マクロファージ - 主に胚中心に存在するマクロファージの一種で、さまざまな分解状態にある多の貪食されたアポトーシス細胞を含む。
- マントル層 - 胚中心を囲む小リンパ球の外輪
脚注
[編集]- ^ Natkunam, Yasodha (1 January 2007). “The Biology of the Germinal Center” (英語). Hematology 2007: 210–215. doi:10.1182/asheducation-2007.1.210. PMID 18024632.
- ^ Aguzzi A, Kranich J, Krautler NJ (2014). “Follicular dendritic cells: origin, phenotype, and function in health and disease”. Trends in Immunology 35 (3): 105-113. doi:10.1016/j.it.2013.11.001. PMID 24315719.
- ^ Thorbecke GJ, Amin AR, Tsiagbe VK (1994). “Biology of germinal centres in lymphoid tissue”. FASEB Journal 8 (11): 832–840. doi:10.1096/fasebj.8.11.8070632. PMID 8070632.
- ^ Meyer-Hermann ME (2002). “A Mathematical Model for the Germinal Centre Morphology and Affinity Maturation”. J. Theor. Biol. 216 (3): 273–300. arXiv:physics/0203021. Bibcode: 2002physics...3021M. doi:10.1006/jtbi.2002.2550. PMID 12183119.
外部リンク
[編集]- MedEd at Loyola Histo/practical/lymph/hp12-42.html - 胚中心の光学顕微鏡像