글리코실기전이효소
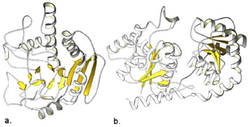
글리코실기전이효소(영어: glycosyltransferase, GTF, Gtf) (EC 2.4)는 천연 글리코사이드 결합을 형성시키는 반응을 촉매하는 효소이다. 글리코실전이효소, 글리코실트랜스퍼레이스라고도 한다. 글리코실트랜스퍼레이스는 활성화된 당뉴클레오타이드(글리코실기 공여체라고도 함)으로부터 친핵성 글리코실기 수용체 분자로 탄수화물 부분을 전달하는 반응을 촉매한다. 이러한 친핵성 글리코실기 수용체는 산소, 탄소, 질소 또는 황 기반일 수 있다.[1]
내용
[편집]글리코실기 전이의 결과는 탄수화물, 글리코사이드, 올리고당 또는 다당류가 될 수 있다. 일부 글리코실트랜스퍼레이스는 무기 인산염 또는 물로의 전이를 촉매한다. 글리코실기 전이는 또한 단백질 잔기, 일반적으로 O-연결된 당단백질을 제공하는 티로신, 세린 또는 트레오닌으로 또는 N-연결된 당단백질을 제공하는 아스파라긴으로 일어날 수 있다. 만노실기는 트립토판으로 이동하여 진핵생물에 비교적 풍부한 C-만노실 트립토판을 생성할 수 있다. 글리코실트랜스퍼레이스는 또한 지질을 수용체로 사용하여 당지질을 형성하고 진핵생물의 돌리콜 인산 또는 박테리아의 운데카 프레닐 포스페이트와 같은 지질 연결 당 인산 공여체를 사용할 수도 있다.
당뉴클레오티드 공여체를 사용하는 글리코실트랜스퍼레이스는 를루아르 효소(Leloir enzymes)로, 최초로 당뉴클레오티드를 발견하고 탄수화물 대사에 대한 연구로 1970년 노벨 화학상을 수상한 과학자 루이스 페데리코 를루아르의 이름에서 따왔다. 돌리콜 또는 폴리 프레놀 피로포스페이트와 같은 비뉴클레오타이드 공여체를 사용하는 글리코실트랜스퍼레이스는 비를루아르 글리코실트랜스퍼레이스이다.
포유동물은 글리코실트랜스퍼레이스에 대해 9개의 당뉴클레오티드 공여체만을 사용한다.[2] 이 9가지는 UDP-글루코스, UDP-갈락토스, UDP-GlcNAc, UDP-GalNAc, UDP-자일로스, UDP-글루쿠론산, GDP-만노스, GDP-푸코스 및 CMP-시알산이다. 이러한 공여체 분자의 인산염(들)은 일반적으로 망가니즈와 같은 2가 양이온에 의해 배위되지만 금속에 대해 독립적인 효소도 존재한다.
많은 글리코실트랜스퍼레이스는 단일 통과 막관통 단백질이며 일반적으로 골지체의 막에 고정되어 있다.[3]
원리
[편집]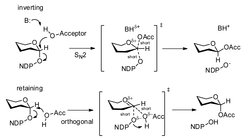
글리코실트랜스퍼레이스는 전달 동안 공여체의 아노머 결합의 입체화학이 유지(α→α) 또는 역전(α→β)되는지 여부에 따라 유지 또는 역전 효소로 분리될 수 있다. 반전 메커니즘은 간단하지만 입체화학을 반전시키기 위해 수용 원자로부터 단일 친핵성 침투가 필요하다.
유지 메커니즘에 대해서는 논쟁의 여지가 있지만 이중 치환 메커니즘(입체화학의 순 유지를 위해 아노머 탄소에 대해 두 개의 역전을 일으킬 수 있음) 또는 해리 메커니즘(일반적으로 SNi). 반전 효소와 유사한 직교 결합 메커니즘이 제안되었으며, 이는 비선형 각도(많은 결정 구조에서 관찰됨)에서 수용체로부터 단일 친핵성 공격만 요구하여 아노머 보유를 달성한다.[4]
반응 가역성
[편집]역전 글리코실트랜스퍼레이스에 의해 촉매되는 많은 반응의 가역성에 대한 최근의 발견은 이 분야의 패러다임 전환으로 작용했으며 당뉴클레오티드를 활성화된 공여체로 지정하는 것에 대한 질문을 제기한다.[5][6][7][8][9]
순서에 따른 분류
[편집]서열 기반 분류 방법은 관련 단백질에 대한 서열 정렬을 기반으로 단백질 기능에 대한 가설을 생성하는 강력한 방법임이 입증되었다. 탄수화물 활성 효소 데이터베이스는 90개 이상의 패밀리로 글리코실트랜스퍼레이스의 서열 기반 분류를 제시한다.[10] 동일한 3차원 접힘이 각 패밀리 내에서 발생할 것으로 예상된다.[11]
구조
[편집]글리코사이드 가수분해효소에 대해 관찰된 3D 구조의 다양성과 대조적으로, 글리코실트랜스퍼레이스는 훨씬 더 작은 범위의 구조를 가지고 있다.[12][13] 사실, 단백질 입체구조 분류 데이터베이스에 따르면, 글리코실트랜스퍼레이스에 대해 세 가지 다른 접힘만이 관찰되었다.[14] 매우 최근에, 펩티도글리칸의 NAG-NAM 폴리머 백본의 생합성에 관여하는 글리코실트랜스퍼레이스에 대해 새로운 글리코실트랜스퍼레이스 접힘이 확인되었다.[15]
저해제
[편집]많은 글리코실트랜스퍼레이스의 저해제가 알려져 있다. 이들 중 일부는 펩티도글리칸 글리코실트랜스퍼레이스의 저해제인 모에노마이신, 키틴 합성효소의 저해제인 니코마이신, 곰팡이 β-1,3-글루칸 합성효소의 저해제인 에키노칸딘과 같은 천연 제품이다. 일부 글리코실트랜스퍼레이스 저해제는 약물이나 항생제로 사용된다. 모에노마이신은 동물 사료에 성장 촉진제로 사용된다. Caspofungin은 echinocandins에서 개발되었으며 항진균제로 사용된다. 에탐부톨은 마이코박테리아 아라비노트랜스퍼라제 저해제이며 결핵 치료에 사용된다. Lufenuron은 곤충 키틴 합성의 저해제이며 동물의 벼룩을 통제하는 데 사용된다. 이미다졸륨 기반 글리코실트랜스퍼레이스의 합성 억제제는 항균제 및 방부제로 사용하도록 설계되었다.[16]
혈액형 결정 인자
[편집]ABO 혈액형은 신체에서 발현되는 글리코실트랜스퍼레이스의 유형에 따라 결정된다.
글리코실트랜스퍼레이스를 발현하는 ABO 유전자 좌위는 A, B 및 O의 세 가지 주요 대립형질을 갖는다.
- A 대립유전자는 α-N-아세틸갈락토사민을 H 항원의 D-갈락토스 말단에 결합시키는 1-3-N-아세틸갈락토사미닐트랜스퍼라제를 코딩하여 항원 A를 생성한다.
- B 대립유전자는 H 항원의 D-갈락토스 말단에 결합된 α-D-갈락토스를 연결하는 1-3-갈락토실트랜스퍼라제를 코딩하여 B 항원을 생성한다. O 대립 유전자의 경우 엑손 6은 효소 활성의 손실을 초래하는 결실을 포함한다.
- O 대립유전자는 위치 261에서 단일 뉴클레오티드인 구아닌이 결실되어 A 대립유전자와 약간 다르다. 결실은 프레임 이동을 유발하고 효소 활성이 결여된 거의 완전히 다른 단백질의 번역을 초래한다. 이것은 O 그룹의 경우 H 항원이 변하지 않고 남아있게 한다.
각 사람에게 존재하는 두 대립유전자에 의한 글리코실트랜스퍼레이스의 조합은 혈액형이 AB형, A형, B형 또는 O형인지 여부를 결정한다.
용도
[편집]글리코실트랜스퍼레이스는 특정 글리코컨쥬게이트의 표적 합성뿐만 아니라 약물 개발의 맥락에서 차등적으로 글리코실화된 약물, 생물학적 프로브 또는 천연 산물 라이브러리의 합성(lycorandomization으로 알려진 프로세스)에 널리 사용되었다.[17]
적합한 효소는 천연 공급원에서 분리하거나 재조합으로 생산할 수 있다. 대안으로, 내인성 글리코실 공여체를 사용하는 전체 세포 기반 시스템 또는 글리코실 공여체 합성을 위한 복제 및 발현 시스템을 포함하는 세포 기반 시스템이 개발되었다. 무세포 접근법에서, 당접합체 합성을 위한 글리코실트랜스퍼레이스의 대규모 적용은 다량의 글리코실 공여체에 대한 접근을 필요로 했다. 한편, 방출된 뉴클레오티드로부터 글리코실 공여체의 재합성을 허용하는 뉴클레오티드 재활용 시스템이 개발되었다. 뉴클레오티드 재활용 접근 방식은 부산물로 형성되는 뉴클레오티드의 양을 줄여 관심 대상인 글리코실트랜스퍼레이스(뉴클레오티드 부산물의 일반적으로 관찰되는 특징)에 유발되는 억제의 양을 줄이는 추가 이점이 있다.
같이 보기
[편집]각주
[편집]- ↑ Williams, GJ; Thorson, JS (2009). 《Natural product glycosyltransferases: properties and applications.》. Advances in Enzymology - and Related Areas of Molecular Biology 76. 55–119쪽. doi:10.1002/9780470392881.ch2. ISBN 9780470392881. PMID 18990828.
- ↑ 《Essentials of Glycobiology》 2판. Plainview, N.Y: Cold Spring Harbor Laboratory Press. 2008. ISBN 978-0-87969-770-9.
- ↑ Transferases in Membranome database.
- ↑ “Geometric Attributes of Retaining Glycosyltransferase Enzymes Favor an Orthogonal Mechanism”. 《PLOS ONE》 8 (8): e71077. August 2013. Bibcode:2013PLoSO...871077S. doi:10.1371/journal.pone.0071077. PMC 3731257. PMID 23936487.
- ↑ Zhang, C; Griffith, BR; Fu, Q; Albermann, C; Fu, X; Lee, IK; Li, L; Thorson, JS (2006년 9월 1일). “Exploiting the reversibility of natural product glycosyltransferase-catalyzed reactions.”. 《Science》 313 (5791): 1291–4. Bibcode:2006Sci...313.1291Z. doi:10.1126/science.1130028. PMID 16946071.
- ↑ Zhang, C; Albermann, C; Fu, X; Thorson, JS (2006년 12월 27일). “The in vitro characterization of the iterative avermectin glycosyltransferase AveBI reveals reaction reversibility and sugar nucleotide flexibility.”. 《Journal of the American Chemical Society》 128 (51): 16420–1. doi:10.1021/ja065950k. PMID 17177349.
- ↑ Zhang, C; Fu, Q; Albermann, C; Li, L; Thorson, JS (2007년 3월 5일). “The in vitro characterization of the erythronolide mycarosyltransferase EryBV and its utility in macrolide diversification.”. 《ChemBioChem》 8 (4): 385–90. doi:10.1002/cbic.200600509. PMID 17262863.
- ↑ Zhang, C; Moretti, R; Jiang, J; Thorson, JS (2008년 10월 13일). “The in vitro characterization of polyene glycosyltransferases AmphDI and NysDI.”. 《ChemBioChem》 9 (15): 2506–14. doi:10.1002/cbic.200800349. PMC 2947747. PMID 18798210.
- ↑ Gantt, RW; Peltier-Pain, P; Cournoyer, WJ; Thorson, JS (2011년 8월 21일). “Using simple donors to drive the equilibria of glycosyltransferase-catalyzed reactions.”. 《Nature Chemical Biology》 7 (10): 685–91. doi:10.1038/nchembio.638. PMC 3177962. PMID 21857660.
- ↑ CAZypedia Glycosyltransferases
- ↑ “CAZy Glycosyl Transferase”. 2009년 3월 23일에 원본 문서에서 보존된 문서. 2022년 3월 10일에 확인함.
- ↑ Singh, S; Phillips GN, Jr; Thorson, JS (October 2012). “The structural biology of enzymes involved in natural product glycosylation”. 《Natural Product Reports》 29 (10): 1201–37. doi:10.1039/c2np20039b. PMC 3627186. PMID 22688446.
- ↑ Chang, A; Singh, S; Phillips GN, Jr; Thorson, JS (December 2011). “Glycosyltransferase structural biology and its role in the design of catalysts for glycosylation”. 《Current Opinion in Biotechnology》 22 (6): 800–8. doi:10.1016/j.copbio.2011.04.013. PMC 3163058. PMID 21592771.
- ↑ SCOP: Structural Classification of Proteins
- ↑ “Structural insight into the transglycosylation step of bacterial cell-wall biosynthesis”. 《Science》 315 (5817): 1402–5. March 2007. Bibcode:2007Sci...315.1402L. doi:10.1126/science.1136611. PMID 17347437.
- ↑ Kocev, A; Melamed, J; Wang, S; Kong, X; Vlahakis, JZ; Xu, Y; Szarek, WA; Brockhausen, I (June 2020). "Inhibition of bacterial growth and galactosyltransferase activity of WbwC by α, ω-bis(3-alkyl-1H-imidazolium)alkane salts: Effect of varying carbon content". Bioorganic and Medicinal Chemistry. 28 (11): 115494. doi:10.1016/j.bmc.2020.115494. PMID 32312486.
- ↑ Gantt, RW; Peltier-Pain, P; Thorson, JS (October 2011). “Enzymatic methods for glyco(diversification/randomization) of drugs and small molecules.”. 《Natural Product Reports》 28 (11): 1811–53. doi:10.1039/c1np00045d. PMID 21901218.