Dihidrolipoil transasetilase
| DLAT | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Pengecam | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Alias | DLAT, DLTA, PDC-E2, PDCE2, dihydrolipoamide S-acetyltransferase, Dihydrolipoyl transacetylase, E2 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Pengecam-pengecam luaran | OMIM: 608770 MGI: 2385311 HomoloGene: 6814 GeneCards: DLAT | ||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Wikidata | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
Dihidrolipoil transasetilase (atau dihidrolipoamida asetiltransferase) ialah komponen enzim kompleks piruvat dehidrogenase multienzim. Kompleks piruvat dehidrogenase bertanggungjawab untuk langkah penyahkarboksilan piruvat yang menghubungkan glikolisis kepada kitaran asid sitrik. Ini melibatkan transformasi piruvat daripada glikolisis kepada asetil-KoA yang kemudiannya digunakan dalam kitaran asid sitrik untuk menjalankan respirasi sel.
Terdapat tiga komponen enzim yang berbeza dalam kompleks piruvat dehidrogenase. Piruvat dehidrogenase (EC 1.2.4.1) bertanggungjawab untuk pengoksidaan piruvat, dihidrolipoil transasetilase (enzim ini; EC 2.3.1.12) memindahkan kumpulan asetil kepada koenzim A (KoA), dan dihidrolipoil dehidrogenase (EC 1.8.1.4) menjana semula lipoamida. Oleh kerana dihidrolipoil transasetilase ialah enzim kedua daripada tiga komponen enzim yang mengambil bahagian dalam mekanisme tindak balas untuk penukaran piruvat kepada asetil KoA, ia kadangkala dirujuk sebagai E2.
Pada manusia, aktiviti enzimatik dihidrolipoil transasetilase berada dalam komponen kompleks piruvat dehidrogenase E2 (PDCE2) yang dikodkan oleh gen DLAT (dihidrolipoamida S-asetiltransferase).[4]
Nomenklatur
[sunting | sunting sumber]Nama sistematik kelas enzim ini ialah asetil-KoA:enzim N6-(dihidrolipoil)lisina S-asetiltransferase.
Struktur
[sunting | sunting sumber]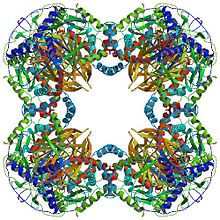
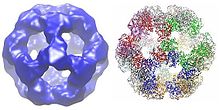
Semua dihidrolipoil transasetilase mempunyai struktur multidomain unik yang terdiri daripada (dari N hingga C): 3 domain lipoil, domain interaksi dan domain pemangkin (lihat seni bina domain di Pfam). Semua domain disambungkan oleh kawasan pemaut kerumitan rendah yang tidak teratur.
Bergantung kepada spesies, berbilang subunit enzim dihidrolipoil transasetilase boleh disusun bersama-sama ke dalam bentuk kiub atau dodekahedron. Struktur ini kemudiannya membentuk teras pemangkin kompleks piruvat dehidrogenase yang bukan sahaja memangkinkan tindak balas yang memindahkan kumpulan asetil kepada KoA, tetapi juga melaksanakan peranan struktur yang penting dalam mencipta seni bina kompleks keseluruhan.[6]
Kiub
[sunting | sunting sumber]Struktur teras kiub yang ada dalam spesies seperti Azotobacter vinelandii terdiri daripada 24 subunit jumlah.[7][8] Domain pemangkin dipasang menjadi trimer dengan tapak aktif terletak di antara muka subunit. Topologi tapak aktif trimer ini adalah sama dengan kloramfenikol asetiltransferase. Lapan daripada trimer ini kemudiannya disusun menjadi kiub terpotong berongga. Dua substrat utama, KoA dan lipoamida (Lip(SH)2), terdapat pada dua pintu masuk bertentangan bagi saluran sepanjang 30 Å yang berjalan di antara subunit, dan membentuk pusat pemangkin. KoA masuk dari dalam kiub, dan lipoamida pula masuk dari luar.[9]
Dodekahedron
[sunting | sunting sumber]Dalam kebanyakan spesies, termasuk bakteria seperti Geobacillus stearothermophilus dan Enterococcus faecalis[6] serta mamalia seperti manusia[10] dan lembu,[11] struktur teras dodekahedral terdiri daripada 60 subunit keseluruhan. Subunit disusun dalam set bertiga, serupa dengan trimer dalam bentuk teras kiub, dengan setiap set membentuk satu daripada 20 bucu dodekahedron.
Fungsi
[sunting | sunting sumber]
Dihidrolipoilltransasetilase mengambil bahagian dalam tindak balas penyahkarboksilan piruvat yang menghubungkan glikolisis kepada kitaran asid sitrik. Proses metabolik ini penting dalam respirasi sel—penukaran tenaga biokimia daripada nutrien kepada adenosina trifosfat (ATP) yang kemudiannya boleh digunakan untuk menjalankan pelbagai tindak balas biologi dalam sel. Pelbagai bahagian respirasi sel berlaku di bahagian sel yang berlainan. Dalam eukariot, glikolisis berlaku di dalam sitoplasma, penyahkarboksilan piruvat pula dalam mitokondria, kitaran asid sitrik dalam matriks mitokondria, dan fosforilasi oksidatif melalui rantai pengangkutan elektron di krista mitokondria. Oleh itu, kompleks piruvat dehidrogenase (mengandungi enzim dihidrolipoil transasetilase) ditemui dalam mitokondria eukariota (dan hanya dalam sitosol prokariot).
Mekanisme
[sunting | sunting sumber]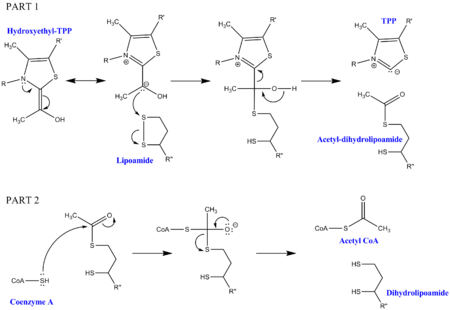
Penyahkarboksilan piruvat memerlukan beberapa kofaktor sebagai tambahan kepada enzim yang membentuk kompleks. Kofaktor pertama ialah tiamina pirofosfat (TPP) yang digunakan oleh piruvat dehidrogenase untuk mengoksidakan piruvat dan membentuk perantaraan hidroksietil-TPP. Perantaraan ini diambil oleh dihidrolipoil transasetilase, dan bertindak balas dengan kofaktor lipoamida kedua untuk menghasilkan perantaraan asetil-dihidrolipoil, melepaskan TPP dalam proses. Perantara kedua ini kemudiannya boleh diserang oleh sulfur nukleofilik yang melekat di Koenzim A, dan dihidrolipoamida dilepaskan. Ini menghasilkan pengeluaran asetil-KoA, matlamat akhir penyahkarboksilan. Dihidrolipoamida diambil oleh dihidrolipoil dehidrogenase, dan melalui kofaktor tambahan FAD dan NAD+, menjana semula lipoamida asal (dengan NADH sebagai produk sampingan berguna).
Kepentingan klinikal
[sunting | sunting sumber]Sirosis hempedu primer
[sunting | sunting sumber]Sirosis hempedu primer (PBC) ialah penyakit autoimun yang dicirikan oleh autoantibodi terhadap antigen mitokondria dan nukleus. Ini dipanggil antibodi antimitokondrion (AMA) dan antibodi antinukleus (ANA), masing-masing. Antibodi ini boleh dikesan dalam serum pesakit PBC, dan sangat berbeza berkaitan kekhususan epitop dari pesakit ke pesakit. Daripada antigen mitokondrion yang boleh menjana kereaktifan autoantibodi dalam pesakit PBC, subunit E2 kompleks piruvat dehidrogenase, dihidrolipoil transasetilase, ialah epitop yang paling biasa (antigen lain termasuk enzim kompleks dehidrogenase 2-oksoasid serta enzim kompleks piruvat dehidrogenase lain).[12] Bukti terkini telah mencadangkan bahawa peptida dalam tapak pemangkin mungkin menunjukkan epitop imunodominan yang diiktiraf oleh antibodi anti-PDC-E2 dalam pesakit PBC.[13] Terdapat juga bukti antibodi anti-PDC-E2 dalam pesakit hepatitis autoimun (AIH).[14]
Kekurangan piruvat dehidrogenase
[sunting | sunting sumber]Kekurangan piruvat dehidrogenase (PDH) ialah penyakit genetik yang mengakibatkan asidosis laktik serta disfungsi neurologi pada peringkat bayi dan awal kanak-kanak. Lazimnya, PDH merupakan hasil mutasi dalam gen berkaitan X bagi subunit E1 kompleks piruvat dehidrogenase. Walau bagaimanapun, terdapat beberapa kes yang jarang berlaku di mana pesakit dengan PDH sebenarnya terbit daripada mutasi dalam gen autosom untuk subunit E2. Pesakit-pesakit ini telah dilaporkan mempunyai simptom yang kurang teruk, dengan manifestasi penyakit yang paling ketara ialah distonia episodik, walaupun kedua-dua hipotonia dan ataksia juga hadir.[15]
Rujukan
[sunting | sunting sumber]- ^ a b c GRCh38: Ensembl release 89: ENSG00000150768 - Ensembl, May 2017
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Chromosome localization and RFLP analysis of PDC-E2: the major autoantigen of primary biliary cirrhosis". Autoimmunity. 14 (4): 335–40. 1993. doi:10.3109/08916939309079237. PMID 8102256.
- ^ "Crystallographic analysis of substrate binding and catalysis in dihydrolipoyl transacetylase (E2p)". Biochemistry. 32 (15): 3887–901. Apr 1993. doi:10.1021/bi00066a007. PMID 8471601.
- ^ a b c PDB: 1B5S; "Principles of quasi-equivalence and Euclidean geometry govern the assembly of cubic and dodecahedral cores of pyruvate dehydrogenase complexes". Proc. Natl. Acad. Sci. U.S.A. 96 (4): 1240–5. February 1999. Bibcode:1999PNAS...96.1240I. doi:10.1073/pnas.96.4.1240. PMC 15447. PMID 9990008.
- ^ "The pyruvate dehydrogenase multi-enzyme complex from Gram-negative bacteria". Biochimica et Biophysica Acta (BBA) - Protein Structure and Molecular Enzymology. 1385 (2): 353–66. Jun 1998. doi:10.1016/S0167-4838(98)00079-X. PMID 9655933.
- ^ "The quaternary structure of the dihydrolipoyl transacetylase component of the pyruvate dehydrogenase complex from Azotobacter vinelandii. A reconsideration". European Journal of Biochemistry. 179 (2): 287–92. Feb 1989. doi:10.1111/j.1432-1033.1989.tb14553.x. PMID 2917567.
- ^ "Atomic structure of the cubic core of the pyruvate dehydrogenase multienzyme complex". Science. 255 (5051): 1544–50. Mar 1992. Bibcode:1992Sci...255.1544M. doi:10.1126/science.1549782. PMID 1549782.
- ^ "Subunit and catalytic component stoichiometries of an in vitro reconstituted human pyruvate dehydrogenase complex". The Journal of Biological Chemistry. 284 (19): 13086–98. May 2009. doi:10.1074/jbc.M806563200. PMC 2676041. PMID 19240034.
- ^ "The remarkable structural and functional organization of the eukaryotic pyruvate dehydrogenase complexes". Proceedings of the National Academy of Sciences of the United States of America. 98 (26): 14802–7. Dec 2001. Bibcode:2001PNAS...9814802Z. doi:10.1073/pnas.011597698. PMC 64939. PMID 11752427.
- ^ "The peculiar autoimmunity of primary biliary cirrhosis". Immunological Reviews. 174: 226–37. Apr 2000. doi:10.1034/j.1600-0528.2002.017410.x. PMID 10807519. Diarkibkan daripada yang asal pada 2013-01-05.
- ^ "Catalytic domain of PDC-E2 contains epitopes recognized by antimitochondrial antibodies in primary biliary cirrhosis". World Journal of Gastroenterology. 16 (8): 973–81. Feb 2010. doi:10.3748/wjg.v16.i8.973. PMC 2828602. PMID 20180236.
- ^ "Long-term follow-up of antimitochondrial antibody-positive autoimmune hepatitis". Hepatology. 48 (2): 550–6. Aug 2008. doi:10.1002/hep.22380. PMID 18666262.
- ^ "Clinical and genetic spectrum of pyruvate dehydrogenase deficiency: dihydrolipoamide acetyltransferase (E2) deficiency". Annals of Neurology. 58 (2): 234–41. Aug 2005. doi:10.1002/ana.20550. PMID 16049940.
Pautan luar
[sunting | sunting sumber]- PDB: 1EAA, PDB: 1dpb
- Dihydrolipoyl+transacetylase dalam Tajuk Subjek Perubatan (MeSH) di Perpustakaan Perubatan Negara AS
- Gambaran maklumat struktur tersedia di PDB bagi UniProt: P10515 (Dihydrolipoyl transacetylase) di PDBe-KB.











