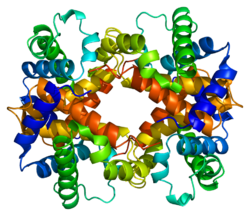
Subunit hemoglobin beta
Hemoglobin subunit beta (beta globin, β-globin) ialah sebuah protein globin yang dikodkan oleh gen HBB, dan bersama dengan globin alfa (HBA), membentuk bentuk hemoglobin yang paling biasa pada manusia dewasa, hemoglobin A (HbA).[4] Panjangnya ialah 147 asid amino dan mempunyai berat molekul 15,867 Da. HbA manusia dewasa normal ialah heterotetramer yang terdiri daripada dua rantai alfa dan dua rantai beta.
HBB dikodkan oleh gen HBB di kromosom manusia 11. Mutasi dalam gen menghasilkan beberapa varian protein yang dikaitkan dengan gangguan genetik seperti penyakit sel sabit dan talasemia beta serta ciri-ciri bermanfaat seperti ketahanan genetik terhadap malaria.[5][6] Sekurang-kurangnya 50 mutasi penyebab penyakit dalam gen ini telah ditemui.[7]
Lokus gen
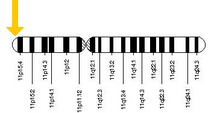
[sunting | sunting sumber]Protein HBB dihasilkan oleh gen HBB yang terletak dalam lokus multigen lokus β-globin di kromosom 11, khususnya pada kedudukan lengan pendek 15.4. Ekspresi globin beta dan globin jiran dalam lokus β-globin dikawal oleh kawasan kawalan lokus tunggal (LCR), elemen pengawalseliaan yang paling penting dalam lokus yang terletak di hulu gen globin.[8] Varian alel biasa ialah 1600 pasangan bes (bp) panjang dan mengandungi tiga ekson. Susunan gen dalam kelompok globin beta ialah 5' - epsilon - gama-G - gama-A - delta - beta - 3'.[4]
Interaksi
[sunting | sunting sumber]HBB berinteraksi dengan Hemoglobin alfa 1 (HBA1) untuk membentuk hemoglobin A, hemoglobin utama manusia dewasa.[9][10] Interaksi terlibat adalah ganda dua. Pertama, satu HBB dan satu HBA1 bergabung secara bukan kovalen untuk membentuk dimer. Selepas itu, dua dimer bergabung untuk membentuk tetramer lalu menjadi hemolglobin berfungsi.[11]
Gangguan genetik berkaitan
[sunting | sunting sumber]Talasemia beta
[sunting | sunting sumber]Talasemia beta ialah mutasi genetik yang diwarisi dalam satu (talasemia beta minor) atau kedua-duanya (talasemia beta major) alel globin beta di kromosom 11. Alel mutan dibahagikan kepada dua kumpulan: β0, di mana tiada β-globin berfungsi dihasilkan, dan β+, di mana sejumlah kecil protein β-globin normal dihasilkan. Talasemia beta minor berlaku apabila seseorang individu mewarisi satu alel beta normal dan satu alel beta abnormal (sama ada β0, atau β+). Talasemia beta minor mengakibatkan anemia mikrosit ringan yang selalunya tak bergejala atau boleh menyebabkan keletihan dan atau kulit pucat. Talasemia beta major berlaku apabila seseorang mewarisi dua alel abnormal. Ini boleh sama ada dua alel β+, dua alel β0, atau satu daripada setiap satu. Talasemia beta major ialah masalah perubatan yang teruk. Anemia yang teruk dapat dilihat bermula pada usia 6 bulan. Tanpa rawatan perubatan, kematian sering berlaku sebelum umur 12 tahun.[12] Talasemia beta major boleh dirawat dengan pemindahan darah sepanjang hayat atau pemindahan sumsum tulang.[13][14]
Menurut kajian baru-baru ini, mutasi hentian Gln40stop dalam gen HBB ialah punca biasa talasemia beta resesif autosom dalam kalangan orang Sardinia (hampir eksklusif di Sardinia). Pembawa mutasi ini menunjukkan bilangan sel darah merah yang dipertingkatkan. Mutasi yang sama juga dikaitkan dengan penurunan paras LDL serum dalam pembawa, dan disangka pengkaji bahawa ini disebabkan oleh keperluan kolesterol untuk menjana semula membran sel.[15]
Penyakit sel sabit
[sunting | sunting sumber]Lebih seribu varian HBB semulajadi telah ditemui. Jenis paling biasa ialah HbS yang menyebabkan penyakit sel sabit. HbS dihasilkan oleh mutasi titik dalam HBB di mana kodon GAG digantikan oleh GTG. Ini mengakibatkan penggantian asid glutamik hidrofilik dengan valina bersifat hidrofobik di kedudukan keenam (β6Glu→Val). Penggantian ini mewujudkan kawasan hidrofobik di luar protein yang melekat pada kawasan hidrofobik rantai beta molekul hemoglobin bersebelahan. Ini seterusnya menyebabkan penggumpalan molekul HbS menjadi gentian tegar, menyebabkan terbitan "sabit" keseluruhan sel darah merah dalam keadaan homozigot (HbS/HbS).[16] Alel homozigot telah menjadi salah satu faktor genetik yang paling membawa maut,[17] manakala pembawa heterozigot mutan (HbS/HbA) tahan terhadap malaria dan mengalami kesan minimum anemia.[18]
Hemoglobin C
[sunting | sunting sumber]Penyakit sel sabit berkait rapat dengan hemoglobin mutan lain yang dipanggil hemoglobin C (HbC) kerana ia boleh diwarisi bersama.[19] Mutasi HbC berada pada kedudukan yang sama dalam HbS, tetapi asid glutamat digantikan oleh lisina (β6Glu→Lys). Mutasi ini sangat lazim dalam populasi Afrika Barat. HbC menyediakan perlindungan hampir penuh terhadap Plasmodium falciparum dalam individu homozigot (CC) dan perlindungan sederhana dalam individu heterozigot (AC).[20] Ini menunjukkan bahawa HbC mempunyai pengaruh yang lebih kuat daripada HbS, dan diramalkan menggantikan HbS di kawasan endemik malaria.[21]
Hemoglobin E
[sunting | sunting sumber]Satu lagi mutasi titik dalam HBB, di mana asid glutamat digantikan dengan lisina di kedudukan 26 (β26Glu→Lys), membawa kepada pembentukan hemoglobin E (HbE).[22] HbE mempunyai persatuan α- dan β-globin yang sangat tidak stabil. Walaupun protein tidak stabil itu sendiri mempunyai kesan ringan, apabila ia diwarisi dengan ciri HbS dan talasemia, ia bertukar menjadi bentuk β-talasemia yang mengancam nyawa. Mutasi ini adalah agak baharu, menunjukkan bahawa ia terhasil daripada tekanan terpilih terhadap malaria Plasmodium falciparum yang teruk kerana alel heterozigot menghalang perkembangan malaria.[23]
Evolusi manusia
[sunting | sunting sumber]Malaria akibat Plasmodium falciparum ialah satu faktor terpilih utama dalam evolusi manusia.[6][24] Ia telah mempengaruhi mutasi dalam HBB di pelbagai peringkat yang mengakibatkan kewujudan banyak varian HBB. Sesetengah mutasi ini tidak secara langsung membawa maut dan sebaliknya memberikan ketahanan terhadap malaria, terutamanya di Afrika, di mana malaria adalah berleluasa.[25] Orang keturunan Afrika telah berkembang untuk mempunyai kadar HBB mutan yang lebih tinggi kerana individu heterozigot mempunyai sel darah merah yang berlainan bentuk lalu menghalang serangan daripada parasit malaria. Oleh itu, mutan HBB adalah sumber pemilihan positif di kawasan ini dan penting untuk kelangsungan hidup jangka panjang mereka.[5][26] Penanda pemilihan sedemikian penting untuk mengesan keturunan manusia dan pempelbagaian dari Afrika.[27]
Lihat juga
[sunting | sunting sumber]Rujukan
[sunting | sunting sumber]- ^ a b c GRCh38: Ensembl release 89: ENSG00000244734 - Ensembl, May 2017
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ a b "Entrez Gene: HBB hemoglobin, beta".
- ^ a b Sabeti, Pardis C (2008). "Natural selection: uncovering mechanisms of evolutionary adaptation to infectious disease". Nature Education. 1 (1): 13.
- ^ a b "How malaria has affected the human genome and what human genetics can teach us about malaria". The American Journal of Human Genetics. 77 (2): 171–192. 2005. doi:10.1086/432519. PMC 1224522. PMID 16001361.
- ^ "Refinement of evolutionary medicine predictions based on clinical evidence for the manifestations of Mendelian diseases". Scientific Reports. 9 (1): 18577. December 2019. Bibcode:2019NatSR...918577S. doi:10.1038/s41598-019-54976-4. PMC 6901466. PMID 31819097.
- ^ "The human beta-globin locus control region". Eur. J. Biochem. 269 (6): 1589–99. 2002. doi:10.1046/j.1432-1327.2002.02797.x. PMID 11895428.
- ^ "A human protein-protein interaction network: a resource for annotating the proteome". Cell. 122 (6): 957–968. 2005. doi:10.1016/j.cell.2005.08.029. PMID 16169070.
|hdl-access=requires|hdl=(bantuan) - ^ "Structure of human oxyhaemoglobin at 2.1 A resolution". J. Mol. Biol. ENGLAND. 171 (1): 31–59. 1983. doi:10.1016/S0022-2836(83)80313-1. ISSN 0022-2836. PMID 6644819.
- ^ "Hemoglobin Synthesis". harvard.edu. Harvard University. 2002. Dicapai pada 18 November 2014.
- ^ H. Franklin Bunn; Vijay G. Sankaran (2017). "8". Pathology of blood disorders. m/s. 927–933.
- ^ "Alpha and beta thalassemia". American Family Physician. 80 (4): 339–44. 2009. PMID 19678601.
- ^ "Beta thalassemia". Genetics Home Reference. U.S. National Library of Medicine. 11 November 2014. Dicapai pada 18 November 2014.
- ^ Sidore, C. (2015). "Genome sequencing elucidates Sardinian genetic architecture and augments association analyses for lipid and blood inflammatory markers". Nature Genetics. 47 (11): 1272–1281. doi:10.1038/ng.3368. PMC 4627508. PMID 26366554. Unknown parameter
|displayauthors=ignored (bantuan) - ^ "Hemoglobin variants: biochemical properties and clinical correlates". Cold Spring Harb Perspect Med. 3 (3): a011858. 2013. doi:10.1101/cshperspect.a011858. PMC 3579210. PMID 23388674.
- ^ "Global and regional mortality from 235 causes of death for 20 age groups in 1990 and 2010: a systematic analysis for the Global Burden of Disease Study 2010". Lancet. 380 (9859): 2095–128. 2012. doi:10.1016/S0140-6736(12)61728-0. PMID 23245604.
|hdl-access=requires|hdl=(bantuan) - ^ "Sickle cell anaemia and malaria". Mediterr J Hematol Infect Dis. 4 (1): e2012065. 2012. doi:10.4084/MJHID.2012.065. PMC 3499995. PMID 23170194.
- ^ "The distribution of haemoglobin C and its prevalence in newborns in Africa". Scientific Reports. 3 (1671): 1671. 2013. Bibcode:2013NatSR...3E1671P. doi:10.1038/srep01671. PMC 3628164. PMID 23591685.
- ^ "Haemoglobin C protects against clinical Plasmodium falciparum malaria". Nature. 414 (6861): 305–308. 2001. Bibcode:2001Natur.414..305M. doi:10.1038/35104556. PMID 11713529.
- ^ "Haemoglobin C and S in natural selection against Plasmodium falciparum malaria: a plethora or a single shared adaptive mechanism?". Parassitologia. 49 (4): 209–13. 2007. PMID 18689228.
- ^ "Hb E/beta-thalassaemia: a common & clinically diverse disorder". The Indian Journal of Medical Research. 134 (4): 522–531. 2011. PMC 3237252. PMID 22089616.
- ^ "Hemoglobin E: a balanced polymorphism protective against high parasitemias and thus severe P falciparum malaria". Blood. 100 (4): 1172–1176. 2002. doi:10.1182/blood.V100.4.1172.h81602001172_1172_1176. PMID 12149194.
- ^ "Genetics of susceptibility to Plasmodium falciparum: from classical malaria resistance genes towards genome-wide association studies". Parasite Immunology. 31 (5): 234–53. 2009. doi:10.1111/j.1365-3024.2009.01106.x. PMID 19388945.
- ^ "Genetic analysis of African populations: human evolution and complex disease". Nature Reviews Genetics. 3 (8): 611–21. 2002. doi:10.1038/nrg865. PMID 12154384.
- ^ "Human demographic history: refining the recent African origin model". Current Opinion in Genetics & Development. 12 (6): 675–682. 2002. doi:10.1016/S0959-437X(02)00350-7. PMID 12433581.
- ^ "African human diversity, origins and migrations". Current Opinion in Genetics & Development. 16 (6): 597–605. 2006. doi:10.1016/j.gde.2006.10.008. PMID 17056248.