Inhibitory odwrotnej transkryptazy
Inhibitory odwrotnej transkryptazy (RTIs) – grupa wielofunkcyjnych organicznych związków chemicznych, hamujących odwrotną transkryptazę oraz wirusową polimerazę DNA, niezbędnych w procesie replikacji ludzkiego wirusa niedoboru odporności oraz retrowirusów stosowanych w leczeniu zespołu nabytego niedoboru odporności (AIDS) oraz wirusowego zapalenia wątroby typu B (WZW typu B).
Inhibitory odwrotnej transkryptazy
[edytuj | edytuj kod]Inhibitory odwrotnej transkryptazy można podzielić na następujące grupy:
- nukleozydowe inhibitory odwrotnej transkryptazy (NARTIs, NRTIs)
- nukleotydowe inhibitory odwrotnej transkryptazy (NtARTIs, NtRTIs)
- nienukleozydowe inhibitory odwrotnej transkryptazy (NNRTIs)
- nukleozydowe inhibitory translokacji odwrotnej transkryptazy (NRTTIs)
- nienukleozydowe inhibitory translokacji odwrotnej transkryptazy (NNRTTIs)
- inhibitory portmanteau
Nukleozydowe inhibitory odwrotnej transkryptazy
[edytuj | edytuj kod]| Nazwa farmaceutyczna |
Skrót | Wzór chemiczny | Wskazanie | Nazwa preparatu |
Zastępowany nukleozyd |
Rejestracja w Polsce |
|---|---|---|---|---|---|---|
| abakawir[1] | ABC |  |
AIDS | Ziagen | dG | Tak |
| didanozyna[2] | ddI |  |
AIDS | Videx | dA | Nie |
| emtrycytabina[3] | FTC |  |
AIDS | Emtriva | dC | Tak |
| entekawir[4] | ETV |  |
WZWB | Baraclude | dG | Tak |
| lamiwudyna[5][6] | 3TC |  |
AIDS WZWB |
Zeffix | dC | Tak |
| stawudyna[7] | d4T |  |
AIDS | Zerit | T | Tak |
| zalcytabina[8] | ddC |  |
AIDS | Hivid | dC | Nie |
| zydowudyna[9] | AZT, ZVD |  |
AIDS | Retrovir | T | Tak |
Nukleotydowe inhibitory odwrotnej transkryptazy
[edytuj | edytuj kod]| Nazwa farmaceutyczna |
Skrót | Wzór chemiczny | Wskazanie | Nazwa preparatu |
Zastępowany nukleozyd |
Rejestracja w Polsce |
|---|---|---|---|---|---|---|
| adefowir[10] | ADF |  |
WZWB | Preveon Hepsera |
adenozyna | Tak |
| tenofowir[11] | TDF |  |
AIDS WZWB |
Truvada Atripla Viread |
adenozyna | Tak |
Nienukleozydowe inhibitory odwrotnej transkryptazy
[edytuj | edytuj kod]| Nazwa farmaceutyczna |
Skrót | Wzór chemiczny | Wskazanie | Nazwa preparatu |
Rejestracja w Polsce |
|---|---|---|---|---|---|
| efawirenz[12] | EFV |  |
AIDS | Sustiva | Tak |
| delawirdyna[13] | DLV |  |
AIDS | Viramune | Nie |
| dorawiryna[14] | ETR |  |
AIDS | Pifeltro | Tak |
| etrawiryna[15] | ETR | 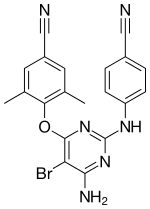 |
AIDS | Intelence | Tak |
| newirapina[16] | NVP | 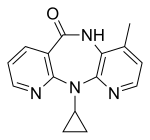 |
AIDS | Viramune | Tak |
| rylpiwiryna[17] | RLP |  |
AIDS | Edurant | Tak |
Nienukleozydowe inhibitory translokacji odwrotnej transkryptazy
[edytuj | edytuj kod]| Nazwa farmaceutyczna |
Skrót | Wzór chemiczny | Wskazanie | Nazwa preparatu |
Rejestracja w Polsce |
|---|---|---|---|---|---|
| elsulfawiryna[18] | EFV |  |
AIDS | Elpida | Nie |
Nowe grupy inhibitorów odwrotnej transkryptazy
[edytuj | edytuj kod]Aktualnie w badaniach klinicznych II fazy znajduje się pierwszy lek z nowej grupy nukleozydowych inhibitorów translokacji odwrotnej transkryptazy (NRTTIs) islatrawir (MK-8591)[19][20][21]. W fazie badań przedklinicznych znajdują się inhibitory portmanteau, które mają łączyć w jednej cząsteczce zdolność hamowania odwrotnej transkryptazy oraz integrazy[22].
Mechanizm działania biologicznego
[edytuj | edytuj kod]Po wniknięciu do wnętrza limfocyta przez receptor CD4 wirusowy jednoniciowy kwas rybonukleinowy (RNA) zostaje przepisany przez retrowirusowy enzym odwrotnej transkryptazy na dwuniciowy wirusowy kwas deoksyrybonukleinowy (DNA), który następnie zostaje wbudowany w jądrze komórkowym do DNA gospodarza[22].
Leki z tej grupy negatywnie wpływają na działanie odwrotnej transkryptazy retrowirusów, natomiast w znacznym mniejszym stopniu hamują komórkową polimerazę DNA[23]. Nukleozydowe i nukleotydowe inhibitory odwrotnej transkryptazy ulegają stopniowej fosforylacji do analogów nukleozydów, których wbudowanie do nowo tworzonego kwasu deoksyrybonukleinowego (DNA) powoduje jego zakończenie i przerwanie replikacji[23]. Natomiast leki z pozostałych grup wywierają bezpośredni wpływ na ten enzym[23][18].
Oporność na leki
[edytuj | edytuj kod]Oporność na inhibitory odwrotnej transkryptazy jest związana z mutacjami w obrębie wirusowego genomu i może występować zarówno w momencie rozpoznania zakażenia jak i pojawić się w trakcie leczenia[24].
Mutacje lekooporności można podzielić na[25]:
- warianty niekorzystnie wpływające na włączanie analogów nukleozydowych do łańcucha DNA (M184V, kompleks Q151M, K65R)
- mutacje związane z usuwaniem analogu nukleozydowego z łańcucha DNA (ang. thymidine analogue mutations) (M41L, D67N, K70R, L210W, T215Y, T215F)
- mutacje związane z opornością na leki nienukleozydowe (L100I, K103N, V106A, Y181C, Y188C, G190A, G190S)
Przypisy
[edytuj | edytuj kod]- ↑ ViiV Healthcare: Ziagen 300 mg tabletki powlekane Charakterystyka Produktu Leczniczego. Europejska Agencja Leków, 2014. [dostęp 2021-02-15].
- ↑ VIDEX (didanosine) [online], Agencja Żywności i Leków, 1999 [dostęp 2021-02-15].
- ↑ Gilead Sciences International: Emtriva 200 mg kapsułki twarde. Charakterystyka Produktu Leczniczego. Europejska Agencja Leków, 2008. [dostęp 2021-02-15].
- ↑ Bristol-Myers Squibb Pharma EEIG: Baraclude tabletki powlekane. Charakterystyka Produktu Leczniczego. Europejska Agencja Leków, 2011. [dostęp 2021-02-15].
- ↑ Lamiwudyna/Zydowudyna Mylan, 150 mg + 300 mg, tabletki powlekane – Charakterystyka Produktu Leczniczego. Centrum Systemów Informacyjnych Ochrony Zdrowia Rejestr Produktów Leczniczych. [dostęp 2021-02-15].
- ↑ Zeffix – Charakterystyka Produktu Leczniczego. GlaxoSmithKline. [dostęp 2021-02-15].
- ↑ Bristol-Myers Squibb: Zerit 15 mg kapsułki twarde Charakterystyka Produktu Leczniczego. Europejska Agencja Leków, 2006. [dostęp 2021-02-15].
- ↑ HIVID (zalcitabine) Tablets [online], Agencja Żywności i Leków, 2002 [dostęp 2021-02-15].
- ↑ Retrovir 250 mg – Charakterystyka Produktu Leczniczego. Centrum Systemów Informacyjnych Ochrony Zdrowia Rejestr Produktów Leczniczych. [dostęp 2021-02-15].
- ↑ Gilead Sciences: Hepsera 10 mg tabletki Charakterystyka Produktu Leczniczego. Europejska Agencja Leków, 2003. [dostęp 2021-02-15].
- ↑ Gilead Sciences: Viread 123 mg tabletki powlekane Charakterystyka Produktu Leczniczego. Europejska Agencja Leków, 2011. [dostęp 2021-02-15].
- ↑ Bristol-Myers Squibb Pharma EEIG: Sustiva kapsułki twarde. Charakterystyka Produktu Leczniczego. Europejska Agencja Leków, 2014. [dostęp 2021-02-15].
- ↑ Rescriptor (delavirdine mesylate) Tablets [online], Agencja Żywności i Leków, 2012 [dostęp 2021-02-15].
- ↑ Merck Sharp & Dohme: Pifeltro 100 mg tabletki powlekane. Charakterystyka Produktu Leczniczego. Europejska Agencja Leków. [dostęp 2021-02-15].
- ↑ Janssen-Cilag: Intelence tabletki. Charakterystyka Produktu Leczniczego. Europejska Agencja Leków, 2018. [dostęp 2021-02-15].
- ↑ Boehringer Ingelheim: Viramune 200 mg tabletki. Charakterystyka Produktu Leczniczego. Europejska Agencja Leków, 2012. [dostęp 2021-02-15].
- ↑ Janssen-Cilag: Edurant 25 mg, tabletki powlekane. Charakterystyka Produktu Leczniczego. Europejska Agencja Leków, 2011. [dostęp 2021-02-15].
- ↑ a b Zaina T. Al-Salama, Elsulfavirine: First Global Approval, „Drugs”, 77 (16), 2017, s. 1811–1816, DOI: 10.1007/s40265-017-0820-3, ISSN 1179-1950, PMID: 28940154 [dostęp 2021-02-22].
- ↑ Weronika Rymer: Dwulekowa terapia zakażenia HIV – doniesienia z konferencji IAS w Meksyku. Medycyna Praktyczna, 2019. [dostęp 2021-02-22].
- ↑ Martin Markowitz, Jay A. Grobler, Islatravir for the treatment and prevention of infection with the human immunodeficiency virus type 1, „Current opinion in HIV and AIDS”, 15 (1), 2020, s. 27–32, DOI: 10.1097/COH.0000000000000599, ISSN 1746-6318, PMID: 31658118 [dostęp 2021-02-22] (ang.).
- ↑ Mary C. Cambou, Raphael J. Landovitz, Novel Antiretroviral Agents, „Current HIV/AIDS reports”, 17 (2), 2020, s. 118–124, DOI: 10.1007/s11904-020-00486-2, ISSN 1548-3576, PMID: 32052271, PMCID: PMC7357992 [dostęp 2021-02-22] (ang.).
- ↑ a b Muhammad Shoaib Ali Gill, Sharifah Syed Hassan, Nafees Ahemad, Evolution of HIV-1 reverse transcriptase and integrase dual inhibitors: Recent advances and developments, „European Journal of Medicinal Chemistry”, 179, 2019, s. 423–448, DOI: 10.1016/j.ejmech.2019.06.058, ISSN 1768-3254, PMID: 31265935 [dostęp 2021-03-13] (ang.).
- ↑ a b c Alfred Zejc, Maria Gorczyca: Chemia leków. Warszawa: PZWL, 2008, s. 715–719. ISBN 978-83-200-3652-7.
- ↑ Kalyan Das, Eddy Arnold, HIV-1 reverse transcriptase and antiviral drug resistance. Part 1, „Current Opinion in Virology”, 3 (2), 2013, s. 111–118, DOI: 10.1016/j.coviro.2013.03.012, PMID: 23602471, PMCID: PMC4097814 [dostęp 2021-03-14] (ang.).
- ↑ Miłosz Parczewski, Lekooporność u osób z zakażeniem HIV-1, „Forum Zakażeń”, 4 (5), 2013, s. 317–323, DOI: 10.15374/fz2013054 [dostęp 2021-03-14].