Acetato de ferro(III)
| Acetato de ferro(III) Alerta sobre risco à saúde[1] | |
|---|---|
| |
| Nome IUPAC | iron(III) acetate |
| Outros nomes | basic iron(III) acetate |
| Identificadores | |
| Número CAS | |
| Propriedades | |
| Fórmula molecular | FeOH(C2H3O2)2 |
| Massa molar | 233 g/mol |
| Aparência | brownish-red amorphous powder |
| Solubilidade em água | insoluble |
| Solubilidade | soluble in ethanol |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
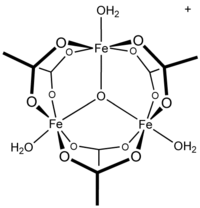
Acetato de ferro (III) ou acetato férrico, comumente conhecido como acetato de ferro básico, é um composto químico com a fórmula [Fe3O(OAc)6(H2O)3]OAc (OAc é CH3CO2-). É um sal, com um ânion acetato e o cátion triangular [Fe3O(OAc)6(H2O)3]+..[2] Cada metal no cátion é ligado a seis átomos de oxigênio, incluindo um óxido triplamente ligado no meio do triângulo equilátero. As águas de ligação podem ser substituidas por outras bases de Lewis, tal como a piridina.

Redução destas species affords the derivados de valência mista que contém um centro ferroso (ferro (II)) em adição a dois centros férricos (ferro (III)).
Em geral o acetato estabiliza estruturas multimetálicas. Outros exemplos incluem o acetato de cromo (II), acetato de cobre (II) e o acetato básico de berílio.[3]
Outros acetatos básicos
[editar | editar código-fonte]Outros metais dão estruturas análogas: cromo, rutênio, vanádio, e ródio. Adicionalmente, substâncias similares com metais mistos são conhecidos tais como o composto de carga neutra [Fe2CoO(OAc)6(H2O)3].[4]
Referências
- ↑ Lide, David R. (1998). Handbook of Chemistry and Physics 87 ed. Boca Raton, FL: CRC Press. pp. 4–63. ISBN 0849305942
- ↑ Figgis, B. N.; Robertson, G. B. “Crystal-Molecular Structure and Magnetic Properties of Cr3(CH3.COO)6OCl.5H2O” Nature 1965, volume 205, pages 694-5. doi:10.1038/205694a0
- ↑ Holleman, A. F.; Wiberg, E. "Inorganic Chemistry" Academic Press: San Diego, 2001. ISBN 0-12-352651-5.
- ↑ Blake, A. B. Yavari, A.; Hatfield, W. E.; Sethulekshmi, C. N. “Magnetic and Spectroscopic Properties of Some Heterotrinuclear Basic Acetates of Chromium(III), Iron(III), and Divalent Metal Ions” Journal of the Chemical Society, Dalton Transactions, 1985, pages 2509 - 2520. doi:10.1039/DT9850002509.