Esfíncter urinário artificial
| Esfíncter urinário artificial | |||
|---|---|---|---|
| |||
Um esfíncter urinário artificial (AUS) é um dispositivo implantado para tratar incontinência urinária de esforço moderada ou severa, mais comumente em homens. O AUS foi desenvolvido para complementar a função do esfíncter urinário natural que restringe o fluxo de urina para fora da bexiga.
Descrição
[editar | editar código-fonte]Existem dois tipos de esfíncteres urinários artificiais:
- O esfíncter urinário artificial de três componentes: manguito de controle, bomba e balão. O manguito de controle é colocado ao redor da uretra; a bomba é inserida no escroto, e o balão é implantado no espaço retropúbico - entre a bexiga e a veia ilíaca. A pressão do circuito hidráulico é gerado pelo balão a partoir do espaço retropúbico[1][2]
- O esfíncter urinário artificial com mola (2 componentes): manguito de controle e bomba.[3][4] O manguito de controle é colocado ao redor da uretra, e a bomba é inserida dentro do escroto. A pressão do circuito hidráulico é gerada pela mola na bomba. A pressão no espaço retropúbico não influencia esse tipo de esfíncter.
O fator comum entre os AUS disponíveis é a constrição mecânica através de um controle inflável preenchido com uma solução salina estéril, e implantada ao redor da uretra que mantém o lúmen uretral fechado devido à pressão produzida dentro do aparelho, e um controle externo acessível, colocado entre as duas camadas de pele do escroto (bolsa subdartos) que permite ao usuário para aliviar a constrição manualmente, e permitir a micção.
História
[editar | editar código-fonte]
Frederic Foley foi o primeiro a descrever um esfíncter urinário artificial externo, desenvolvido para tratar incontinência urinária, publicada em 1947.[5] Em 1972, F. Brantley Scott e seus colegas da Faculdade de Medicina de Baylor desenvolveram o precursor do esfíncter urinário artificial contemporâneo.[6][7] O primeiro modelo de AUS a entrar no mercado foi o AMS 800 (Boston Scientific, Marlborough, MA), que foi desenvolvido 50 anos atrás.[8][9] É um implante de três componentes com um controle posicionado ao redor da uretra, uma bomba inserida no escroto, e um reservatório gerador de pressão posicionado na pélvis, que vem com um kit para preparar e encher antes da implantação.[10]
Outro modelo de AUS é o ZSI 375 (Zephyr Surgical Implants, Genebra, Suíça), apresentado em 2008.[11] É um aparelho inteiro com duas partes, um controle e uma bomba com mola integrada, que vem como uma única peça, pré-conectada e pré-preenchida.[1][12] Não há componente abdominal no ZSI 375 que junto com sua configuração pronta para implantar reduz o tempo de operação.[13] Além disso, evitando incisão abdominal previne cicatrizes pós-operatória na área retroperitoneal, assim, evitando a dissecação dos tecidos retroperitoneais, o ZSI 375 evita complicações cirúrgicas.[14][15]
Outra vantagem do ZSI 375 é a possibilidade de aumentar ou diminuir dentro do aparelho depois da implantação para encontrar a continência ideal para a satisfação do paciente. Estes ajustes ajudam a manter o controle de continência no caso de atrofia na uretra ou retenção urinária no pós-implantação. Os ajustes de pressão podem ser feitos através da adição ou remoção da solução salina através de uma seringa no escroto. Até 2019, mais de 4500 unidades do esfíncter urinário artificial do ZSI 375 foram implantados no mundo inteiro.[13][16][17]
Os dois modelos são preenchidos com solução salina dentro do sistema que é utilizado para gerar pressão e comprimir a uretra (para prevenir vazamentos da urina). O controle uretral é esvaziado manualmente através de uma bomba controlada manualmente, que fica no escroto, permitindo que o paciente esvazie a bexiga. O controle da uretra então reinfla automaticamente e o paciente torna-se continente novamente.[1][18]
A lista inclui modelos AUS disponíveis no mercado em 2020:
| Produtos | Companhia | País de origem | Introduzido em | Projeto | Pré-conectado e pré-carregado | Entrega de pressão | Pressão ajustável |
|---|---|---|---|---|---|---|---|
| AMS 800 | Boston Scientific (anteriormente American Medical Systems) | Estados Unidos da America | 1988 | 3 componentes: manguito, bomba, reservatório | Não | Reservatório flexível inserido no assoalho pélvico | Não |
| ZSI 375 | Zephyr Surgical Implants | Suíça | 2008 | 2 componentes: manguito, bomba | sim | Mola de aço inoxidável dentro da unidade da bomba inserida no escroto | sim |


Uso médico
[editar | editar código-fonte]A incontinência de estresse causada pela deficiência no esfíncter intrínseco é a indicação mais comum da implantação do esfíncter urinário artificial.[9] A Associação Europeia de Urologia recomenda o implante para tratamento de incontinência de estresse severa para moderada em homens.[19] Adicionalmente, apesar das novas opções de tratamento, o esfíncter urinário artificial é o padrão ouro para o manejo cirúrgico, tanto para incontinência de estresse em homens, e incontinência desenvolvida pela complicação cirúrgica de uma prostatectomia, cistectomia, ou ressecção transuretral da próstata.[3][4][8]
Existem vários relatos de casos publicados na literatura sobre implante de AUS em crianças por incontinência secundária resultante de lesão uretral traumática.[20][21]
Existem dados limitados sobre o uso de AUS em mulheres, e nem todos os produtos disponíveis no mercado são projetados para uso em mulheres.[22][23] A Associação Europeia de Urologia fornece uma recomendação fraca sobre o uso de AUS em mulheres, afirmando que, embora a cura seja possível, o risco de complicações é alto.[19] No entanto, o AUS tem sido utilizado como último recurso no tratamento da incontinência urinária em mulheres devido a causas congênitas e secundárias a doenças neurológicas.[22]
Resultados
[editar | editar código-fonte]Taxa de sucesso
[editar | editar código-fonte]
Numerosos estudos foram publicados sobre os resultados de pacientes submetidos à colocação artificial de esfíncter urinário. A taxa de sucesso, geralmente definida como alcançar continência total (sem uso de frauda) ou social (uso de ≤1 frauda por dia) com o dispositivo implantado, varia de 61% a 100% na literatura.[4] A melhoria da qualidade de vida também foi considerada um sucesso, mesmo que mais de uma fralda ao dia fosse necessário. Foi relatado em 78% com acompanhamento de três anos[24] e acima de 72% com 5 a 7 anos de acompanhamento.[25] Em uma revisão sistemática recente, a taxa de sucesso foi relatada em 79%, com período de acompanhamento variando de 5 meses a 16 anos.[26] Um estudo comparativo entre pacientes implantados com diferentes modelos de esfíncter urinário artificial e alcançou continência social não mostrou diferença entre dois grupos em relação aos testes urodinâmicos, como taxa de fluxo, pressão uretral, etc.[2]
Satisfação
[editar | editar código-fonte]Em diferentes estudos com seguimento médio de mais de 6 anos,[27][28] pelo menos 73% dos homens com esfíncter urinário artificial implantado estavam satisfeitos ou muito satisfeitos com o dispositivo e 10-23% relataram insatisfação. Em períodos mais curtos de acompanhamento (2-4 anos), as taxas de satisfação alcançaram mais de 90%.[4][26][27] Em outro estudo com acompanhamento médio de mais de 7 anos, a taxa de satisfação geral mediu 3,9 em uma escala de 0 a 5.[27] A taxa de satisfação parece não ser afetada desfavoravelmente nos pacientes após a radioterapia.[29] A satisfação inicial com a taxa de continência é relatada como melhorada ajustando a pressão dentro do implante com o modelo ZSI 375.[23]
Pesquisas realizadas com pacientes submetidos ao procedimento constataram que mais de 90% recomendariam o procedimento a um amigo ou parente com o mesmo problema e mais de 90% seriam submetidos ao implante novamente.[30][31] Junto com isso, 14% dos pacientes relataram melhora na atividade sexual.[31]
A qualidade de vida após a implantação do AUS demonstrou melhorar significativamente em vários estudos usando várias ferramentas de dimensionamento.[7][27] E a qualidade de vida parece não ser afetada negativamente pelas reintervenções, desde que o dispositivo continue funcionando após a revisão.
Reoperação
[editar | editar código-fonte]Na maior série disponível que avaliou 1082 pacientes submetidos à colocação primária de AUS, a sobrevida do dispositivo em 5 anos foi de 74%, o que é consistente com os resultados relatados na literatura, variando de 59% a 79%.[32] Notavelmente, em todas as séries, ao longo do tempo, alguns pacientes precisaram passar por uma cirurgia repetida para incontinência urinária recorrente ou infecção do dispositivo. Em uma análise conjunta dos estudos disponíveis, a taxa de reintervenção (por qualquer causa) foi de aproximadamente 26%.[23] É importante ressaltar que alguns estudos demonstraram que os cirurgiões que realizam esse procedimento com mais frequência (cirurgiões de alto volume) têm melhores resultados em comparação com aqueles que o fazem com menos frequência.[23] De fato, nesta série, as taxas reoperativas diminuíram cerca de 50% quando os cirurgiões chegaram ao seu 200º caso, enfatizando a necessidade de pacientes em potencial procurarem cirurgiões de alto volume para melhorar suas chances de sucesso.[23]
Complicações
[editar | editar código-fonte]Possíveis riscos decorrentes da implantação do AUS incluem:[1]
- a lesão da uretra ou da bexiga durante a colocação AUS;
- dificuldades de esvaziamento da bexiga exigindo cateterismo;
- incontinência urinária persistente;
- infecções do aparelho levando a remoção,
- incontinência recorrente devido a falha do dispositivo ou atrofia dos tecidos uretrais; nesse caso, outras cirurgias podem ser realizadas para remover o dispositivo antigo e colocar um novo.
A taxa geral de complicações relatadas em homens é de 37%.[33] As complicações pós-operatórias mais comuns são:
- falha mecânica (8-21%),
- erosão uretral (4-15%),
- infecção (1-14%) e
- atrofia uretral (4-10%).
Outras complicações menos frequentes são hematoma, estenose uretral, fístula urinária.[34] Falhas mecânicas e complicações não mecânicas podem levar à revisão cirúrgica em 8-45% e 7-17% dos casos, respectivamente. As taxas gerais de explantação de dispositivos em homens são de 16 a 20%.[35]
Acompanhamento
[editar | editar código-fonte]Depois da alta
[editar | editar código-fonte]As relações sexuais devem ser evitadas nas primeiras 6 semanas depois do procedimento para permitir a cicatrização.[36] Atividades físicas que aplicam pressão na cicatriz, como andar a cavalo e de bicicleta também devem ser evitadas por no mínimo 6 semanas. Os pacientes podem ter prescrição de um apoio escrotal para ser utilizado 1 semana após o procedimento.[37]
Cuidados contínuos
[editar | editar código-fonte]Para aqueles que tiveram um AUS colocado, é importante que eles informem seus médicos antes de qualquer tentativa de colocação do cateter uretral, na tentativa de minimizar o risco de danos ao seu AUS.[38] A desativação do aparelho durante as noites podem ser recomendadas aos pacientes, especialmente aqueles que relatam secura durante a noite, para minimizar os riscos de atrofia da uretra.[36][39]
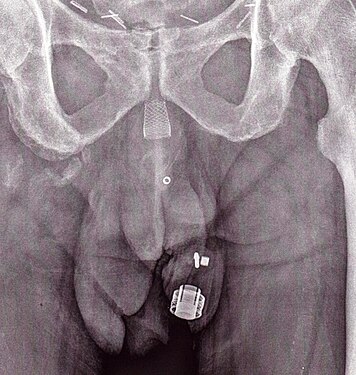
Galeria de Imagens
[editar | editar código-fonte]-
Tomografia computadorizada (reconstrução coronal) mostrando um AMS 800 em uma mulher.
-
Uma imagem de raio X de um ZSI 375 implantado. O aparelho está desativado - a mole está comprimida abaixo do topo do cilinder. O paciente está continente.
-
Uma radiografia x de um ZSI 375. O aparelho se encontra ativado - a mola é descomprimida no topo do cilindro. O paciente está continente.
-
Um GIF mostrando como o manguito de controle periuretral do esfíncter urinário artificial constringe a uretra.
Veja também
[editar | editar código-fonte]- Incontinencia urinaria
- Incontinência de esforço
- Prostatectomia
- Ressecção transuretral da próstata
- Esfíncter uretral interno
- Uretra
- Zephyr Surgical Implants
Referências
[editar | editar código-fonte]- ↑ a b c d Vakalopoulos, Ioannis; Kampantais, Spyridon; Laskaridis, Leonidas; Chachopoulos, Vasileios; Koptsis, Michail; Toutziaris, Chrysovalantis (2012). «New Artificial Urinary Sphincter Devices in the Treatment of Male Iatrogenic Incontinence». Advances in Urology. 2012. ISSN 1687-6369. PMC 3332164
 . PMID 22567002. doi:10.1155/2012/439372
. PMID 22567002. doi:10.1155/2012/439372
- ↑ a b Ripert, Thomas; Pierrevelcin, Jean (21 de setembro de 2017). «Comparative study of urodynamic tests after AMS 800 and ZSI 375 insertion». Urologia Journal (em inglês). 85 (1): 15–18. ISSN 0391-5603. doi:10.5301/uj.5000271
- ↑ a b Bauer, Ricarda M.; Gozzi, Christian; Hübner, Wilhelm; Nitti, Victor W.; Novara, Giacomo; Peterson, Andrew; Sandhu, Jaspreet S.; Stief, Christian G. (1 de junho de 2011). «Contemporary Management of Postprostatectomy Incontinence». European Urology (em inglês). 59 (6): 985–996. ISSN 0302-2838. doi:10.1016/j.eururo.2011.03.020
- ↑ a b c d Cordon, Billy H; Singla, Nirmish; Singla, Ajay K (4 de julho de 2016). «Artificial urinary sphincters for male stress urinary incontinence: current perspectives». Medical Devices (Auckland, N.Z.). 9: 175–183. ISSN 1179-1470. PMC 4938139
 . PMID 27445509. doi:10.2147/MDER.S93637
. PMID 27445509. doi:10.2147/MDER.S93637
- ↑ Foley, Frederic E. B. (1 de outubro de 1947). «An Artificial Sphincter: A New Device and Operation for Control of Enuresis and Urinary Incontinence11Read at annual meeting, American Urological Association, Cincinnati, O., July 26, 1946 and the Urological Section of the American Medical Association, San Francisco, Calif., July 6, 1946.». The Journal of Urology (em inglês). 58 (4): 250–259. ISSN 0022-5347. doi:10.1016/S0022-5347(17)69552-1
- ↑ Scott, F. Brantley; Bradley, William E.; Timm, Gerald W. (1 de julho de 1974). «Treatment of Urinary Incontinence By An Implantable Prosthetic Urinary Sphincter». The Journal of Urology (em inglês). 112 (1): 75–80. ISSN 0022-5347. doi:10.1016/S0022-5347(17)59647-0
- ↑ a b Yafi, Faysal A.; Powers, Mary K.; Zurawin, Jonathan; Hellstrom, Wayne J. G. (1 de abril de 2016). «Contemporary Review of Artificial Urinary Sphincters for Male Stress Urinary Incontinence». Sexual Medicine Reviews (em inglês). 4 (2): 157–166. ISSN 2050-0521. doi:10.1016/j.sxmr.2015.11.004
- ↑ a b Suarez, Oscar A.; McCammon, Kurt A. (1 de junho de 2016). «The Artificial Urinary Sphincter in the Management of Incontinence». Urology (em inglês). 92: 14–19. ISSN 0090-4295. doi:10.1016/j.urology.2016.01.016
- ↑ a b Scott F. Brantley; Bradley William E.; Timm Gerald W. (1 de julho de 1974). «Treatment of Urinary Incontinence By An Implantable Prosthetic Urinary Sphincter». Journal of Urology. 112 (1): 75–80. doi:10.1016/S0022-5347(17)59647-0
- ↑ Boston Scientific Corporation. «AMS 800™ Urinary Control System For Male Patients: Oerating Room Manual» (PDF)
- ↑ Zephyr Surgical Implants (November 2019). «ARTIFICIAL URINARY SPHINCTER ZSI 375» (PDF)
- ↑ Ostrowski, Ireneusz; Golabek, Tomasz; Ciechan, Janusz; Śledź, Emil; Przydacz, Mikolaj; Dyś, Wojciech; Blewniewski, Mariusz; von Heyden, Burkhard; Pottek, Tobias (2019). «Preliminary outcomes of the European multicentre experience with the ZSI 375 artificial urinary sphincter for treatment of stress urinary incontinence in men». Central European Journal of Urology. 72 (3): 263–269. ISSN 2080-4806. PMC 6830485
 . PMID 31720028. doi:10.5173/ceju.2019.1920
. PMID 31720028. doi:10.5173/ceju.2019.1920
- ↑ a b Ostrowski, Ireneusz; Ciechan, Janusz; Sledz, Emil; Dys, Wojciech; Golabek, Tomasz; Chłosta, Piotr L. (2018). «Four-year follow-up on a Zephyr Surgical Implants 375 artificial urinary sphincter for male urinary incontinence from one urological centre in Poland». Central European Journal of Urology. 71 (3): 320–325. ISSN 2080-4806. PMC 6202622
 . PMID 30386654. doi:10.5173/ceju.2018.1704
. PMID 30386654. doi:10.5173/ceju.2018.1704
- ↑ «The Surgical Learning Curve for Artificial Urinary Sphincter Procedures Compared to Typical Surgeon Experience». European Urology. 60: 1285–1290. PMID 21665357. doi:10.1016/j.eururo.2011.05.048
- ↑ «ZSI 375 artificial urinary sphincter for male urinary incontinence: a preliminary study». BJU International. 111: E202-E206. PMID 22937774. doi:10.1111/j.1464-410X.2012.11468.x
- ↑ «EFFICACY OF THE ARTIFICIAL URINARY SPHINCTER ZSI 375 FOR TREATMENT OF POST-RADICAL PROSTATECTOMY INCONTINENCE IN PATIENTS WITH INTRINSIC SPHINCTER DEFICIENCY: A PRELIMINARY STUDY». European Medical Journal. 2: 22–26
- ↑ Ostrowski, Ireneusz; Blewniewski, Mariusz; Neugart, Frank; von Heyden, Burkhard; Selvaggio, Oscar; Iori, Francesco; Foley, Steeve; Fernández Arjona, Manuel; Carvajal Obando, Alejandro (29 de maio de 2017). «Multicentre Experience with ZSI 375 Artificial Urinary Sphincter for the Treatment of Stress Urinary Incontinence in Men». Urologia Journal (em inglês). 84 (3): 148–152. ISSN 0391-5603. doi:10.5301/uj.5000246
- ↑ Chung, Eric (2017). «Contemporary surgical devices for male stress urinary incontinence: a review of technological advances in current continence surgery». Translational Andrology and Urology. 6 (Suppl 2): S112–S121. ISSN 2223-4691. PMC 5522789
 . PMID 28791230. doi:10.21037/tau.2017.04.12
. PMID 28791230. doi:10.21037/tau.2017.04.12
- ↑ a b Burkhard, F.C.; Bosch, J.L.H.R.; Cruz, F.; Lemack, G.E.; Nambiar, A.K.; Thiruchelvam, N.; Tubaro, A. (2018). «EAU Guidelines on Urinary Incontinence in Adults» (PDF). European Association of Urology.
- ↑ «Long-term continence outcomes after immediate repair of pediatric bladder neck lacerations extending into the urethra». The Journal of Urology. 178: 1816–1818. PMID 17707005. doi:10.1016/j.juro.2007.05.094
- ↑ «Single piece artificial urinary sphincter for secondary incontinence following successful repair of post traumatic urethral injury». Journal of Indian Association of Pediatric Surgeons. 18: 152–154. PMID 24347870. doi:10.4103/0971-9261.121120
- ↑ a b «The Current Role of the Artificial Urinary Sphincter in Male and Female Urinary Incontinence». The World Journal of Men's Health. 31: 21–30. PMID 23658862. doi:10.5534/wjmh.2013.31.1.21
- ↑ a b c d e Sandhu (2011). «The Surgical Learning Curve for Artificial Urinary Sphincter Procedures Compared to Typical Surgeon Experience». European Urology. 60: 1285–1290. PMC 3646622
 . PMID 21665357. doi:10.1016/j.eururo.2011.05.048
. PMID 21665357. doi:10.1016/j.eururo.2011.05.048
- ↑ «Multicentre Experience with ZSI 375 Artificial Urinary Sphincter for the Treatment of Stress Urinary Incontinence in Men». Urologia Journal. 84: 148–152. PMID 28574143. doi:10.5301/uj.5000246
- ↑ «Urinary Artificial Sphincter ZSI 375 for Treatment of Stress Urinary Incontinence in Men: 5 and 7 Years Follow-Up Report». Urologia Journal. 84: 263–266. PMID 28525665. doi:10.5301/uj.5000243
- ↑ a b «The Artificial Urinary Sphincter After a Quarter of a Century: A Critical Systematic Review of Its Use in Male Non-neurogenic Incontinence». European Urology. 63: 681–689. PMID 23219375. doi:10.1016/j.eururo.2012.11.034
- ↑ a b c d «Artificial Urinary Sphincter: Long-Term Results and Patient Satisfaction». Advances in Urology. 2012: 1–4. PMID 22536227. doi:10.1155/2012/835290
- ↑ «A state-of-the-art review on the evolution of urinary sphincter devices for the treatment of post-prostatectomy urinary incontinence: Past, present and future innovations». Journal of Medical Engineering & Technology. 38: 328–332. PMID 24936961. doi:10.3109/03091902.2014.899400
- ↑ «The artificial urinary sphincter is the treatment of choice for post–radical prostatectomy incontinence». Canadian Urological Association Journal. 2. 536 páginas. PMID 18953453. doi:10.5489/cuaj.924
- ↑ Viers (2016). «Long-Term Quality of Life and Functional Outcomes among Primary and Secondary Artificial Urinary Sphincter Implantations in Men with Stress Urinary Incontinence». The Journal of Urology. 196: 838–843. PMID 26997310. doi:10.1016/j.juro.2016.03.076
- ↑ a b «Post-Prostatectomy incontinence and the Artificial Urinary Sphincter: A Long-Term Study of Patient Satisfaction and Criteria for Success». Journal of Urology. 156: 1975–1980. PMID 8911369. doi:10.1016/S0022-5347(01)65408-9
- ↑ Linder (2015). «Long-term Outcomes Following Artificial Urinary Sphincter Placement: An Analysis of 1082 Cases at Mayo Clinic». Urology. 86: 602–607. PMID 26135815. doi:10.1016/j.urology.2015.05.029
- ↑ «The current role of the artificial urinary sphincter for the treatment of urinary incontinence». Journal of Urology. 174: 418–424. PMID 23658862. doi:10.1097/01.ju.0000165345.11199.98
- ↑ «The Current Role of the Artificial Urinary Sphincter in Male and Female Urinary Incontinence». The World Journal of Men's Health. 31: 21–30. PMID 23658862. doi:10.5534/wjmh.2013.31.1.21
- ↑ «Artificial sphincter». Current Opinion in Urology. 23: 520–527. PMID 24080811. doi:10.1097/01.MOU.0000434591.02823.d0
- ↑ a b «Urinary Sphincter Replacement (Discharge Care) - What You Need to Know» (em inglês)
- ↑ Memorial Sloan Kettering Cancer Center. «"About Your Artificial Urinary Sphincter | Memorial Sloan Kettering Cancer Center"». www.mskcc.org
- ↑ Agarwal (2016). «Artificial urinary sphincter urethral erosions: Temporal patterns, management, and incidence of preventable erosions». Indian Journal of Urology. 0: 26–29. PMC 5264188
 . PMID 28197026. doi:10.4103/0970-1591.195758
. PMID 28197026. doi:10.4103/0970-1591.195758
- ↑ Elliott, Daniel S.; Barrett, David M.; Gohma, Mohamed; Boone, Timothy B. (1 de junho de 2001). «Does nocturnal deactivation of the artificial urinary sphincter lessen the risk of urethral atrophy?». Urology (em inglês). 57 (6): 1051–1054. ISSN 0090-4295. doi:10.1016/S0090-4295(01)00963-3