Exostoses múltiplas hereditárias
| Hereditary multiple osteochondromas | |
|---|---|
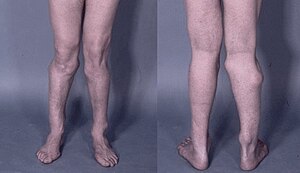
| Photograph of the legs of a 26-year-old male showing multiple lumps leading to deformity. | |
| Especialidade | genética médica |
| Classificação e recursos externos | |
| CID-10 | Q78.6 |
| OMIM | 133700, 600209, 133701 |
| DiseasesDB | 33342 |
| MeSH | D005097 |
Osteocondromas múltiplos hereditários (HMO, hereditary multiple osteochondromas), também conhecidos como exostoses múltiplas hereditárias, é uma doença caracterizada pelo desenvolvimento de múltiplas massas osteocartilaginosas benignas (exostoses) nas extremidades dos ossos longos dos membros inferiores, como fêmures e tíbias, e dos membros superiores, como os úmeros e os ossos do antebraço. Eles também podem ser conhecidos como osteocondromas, osteocondromatose (osteochondromatosis) ou exostoses cartilaginosas múltiplas. Também podem ocorrer em ossos chatos, como o osso pélvico e a escápula.
A distribuição e o número dessas exostoses mostram uma grande diversidade entre os indivíduos afetados pela doença. Elas geralmente se apresentam durante a infância e a grande maioria dos indivíduos afetados manifesta-se clinicamente quando atingem a adolescência.[1][2] Uma pequena porcentagem dos afetados também corre o risco de desenvolver sarcomas como resultado de mutação maligna. A incidência de exostoses múltiplas hereditárias é de cerca de 1 em 50.000 indivíduos.[3]
Osteocondromas múltiplos hereditários é o termo preferido usado pela Organização Mundial da Saúde.
Apresentação
[editar | editar código-fonte]O primeiro sintoma notado pode ser um nódulo perceptível em relação a uma extremidade. Além disso, podem surgir múltiplas deformidades, chamadas deformidades do plano coronal à volta dos joelhos, tornozelos, ombros, cotovelos e punhos. Por exemplo, joelho em valgo (joelhos tortos), tornozelo valgo, arqueamento e encurtamento ulnar e subluxação da cabeça do rádio são tipo de deformidades encontradas. A maior parte dos indivíduos afetados apresenta osteocondromas clinicamente manifestados ao redor do joelho. Além de que, o envolvimento do antebraço no osteocondroma múltiplo hereditário ser considerável.[1][4] Ademais, pode ocorrer baixa estatura, normalmente desproporcional. Tais manifestações geralmente resultam da interrupção do crescimento fisário, especialmente porque os osteocondromas usualmente surgem nas extremidades da metáfase proximal dos ossos longos nas proximidades da epífise.[1][4]
Osteocondromas intrarticulares do quadril podem induzir limitação da extensão de movimentos, dores articulares e displasia acetabular.[2] Da mesma forma, pode ocorrer dor nas articulações em outros locais e compressão neurovascular. A incapacidade funcional em relação às atividades da vida diária também pode ser uma característica presente na vida dos indivíduos afetados pela doença. A dor da deformidade da coluna ou o comprometimento neurológico geralmente levantam a suspeita de envolvimento das vértebras.[3]
Dores
[editar | editar código-fonte]De acordo com relatos de pacientes, a grande maioria deles sente dor e cerca de metade sente dor generalizada. Pacientes que tiveram complicações relacionadas ao HME tiveram cinco vezes mais chances de sentirem dores, enquanto aqueles que fizeram cirurgia tiveram 3,8 mais chances de sentirem dores. Não foram encontradas diferenças entre homens e mulheres em relação às dores, cirurgias ou complicações relacionadas ao osteocondroma múltiplo hereditário.[5]
Possível relação com autismo
[editar | editar código-fonte]Alguns pais de crianças com a doença observaram problemas sociais semelhantes ao transtorno do espectro autismo em seus filhos. Para explorar e entender essas observações mais profundamente, um estudo realizado em 2012 no Sanford-Burnham Medical Research Institute usou uma cobaia de rato com HME para observar a função cognitiva. Os resultados indicaram que os ratos mutantes possuíam três características autistas: deficiência social, dificuldade na vocalização e comportamento repetitivo.[6]
Genética
[editar | editar código-fonte]Osteocondromas múltiplos hereditários é uma doença, por nome, hereditária e autossômica dominante. O que significa que o paciente possui uma chance de 50% de transmitir a doença para os seus filhos.
A maioria dos indivíduos afetados tem um pai ou mãe que também tem a doença, enquanto, aproximadamente 10 a 20% possui a doença devido uma mutação espontânea e se tornam a primeira pessoa da família a serem afetados.
Até agora, os osteocondromas múltiplos hereditários (HME) tem sido associados a mutações em três genes:
- EXT1 que mapeia para o cromossomo 8q24.1[7]
- EXT2 que mapeia para 11p13[8]
- EXT3 que mapeia para o braço curto do cromossomo 19 (embora sua localização exata ainda não tenha sido determinada com precisão) [9]
As mutações nesses genes comumente levam à síntese de uma proteína EXT truncada que não funciona normalmente. Sabe-se que as proteínas EXT são enzimas importantes na síntese do sulfato de heparano; contudo, o mecanismo exato por qual a síntese alterada de sulfato de heparano pode trazer o crescimento ósseo anormal relacionado ao osteocondroma múltiplo hereditário não é certo. Acredita-se que a proliferação e diferenciação normais dos condrócitos possam ser atingidas, levando a um crescimento ósseo anormal que ocasionaria na doença.[10][11] Uma vez que os genes HME estão envolvidos na síntese de um glicano (heparan sulfato), a doença pode ser considerado um distúrbio congênito da glicosilação de acordo com a nova nomenclatura CDG (doença congênita de glicosilação) sugerida em 2009.[12]
Para os pacientes com a doença que estão pensando em constituir família, há testes genéticos pré-implantação e diagnóstico pré-natal disponíveis para determinar se o feto herdou ou não a doença. O osteocondroma múltiplo hereditário tem uma penetrância de 96%, o que significa que, se o gene afetado for realmente passado para a criança, ela terá 96% de realmente manifestar a doença e 4% de chance de ter a doença, mas nunca a manifestar. O valor dessa penetrância de 96% vem de somente um estudo.[13] Outros estudos observaram penetrância incompleta e variável, mas não calcularam a porcentagem da penetrância.[14] Em ambos os estudos mencionados, os indivíduos assintomáticos portadores do gene com defeito eram predominantemente do sexo feminino, levando à consideração de que a penetrância incompleta é mais provável de ser apresentada em mulheres. De fato, outros trabalhos mostraram que pacientes do sexo masculino tendem a ter uma doença pior do que mulheres, assim como que o número de exostoses em membros familiares afetados pode variar muito.[15] A possibilidade de que as mulheres sejam severamente afetadas também existe e não é descartada. A gravidade dos sintomas varia entre os indivíduos afetados, mesmo que estejam na mesma família.
É mais provável que os sintomas da doença sejam graves ou severos se a mutação ocorrer no gene EXT1 em vez de EXT2 ou EXT3 ; EXT1 também é o gene mais comumente afetado em pacientes com esse distúrbio.[15]
Fisiopatologia
[editar | editar código-fonte]A fisiopatologia das osteocondromas múltiplas hereditárias é caracterizada pelo crescimento de tumores ósseos benignos cobertos por cartilagem em torno de áreas de crescimento ósseo ativo, particularmente a metáfise dos ossos longos. Geralmente, cinco ou seis exostoses são encontradas em membros superiores e inferiores. As áreas mais comuns são: [16]
Esse distúrbio pode levar ao encurtamento e arqueamento dos ossos; levando aos indivíduos afetados terem baixa estatura, geralmente. Dependendo da sua localização, as exostoses podem causar tais problemas: dor ou dormência por compressão nervosa, comprometimento vascular, desigualdade no comprimento dos membros, irritação de tendões e músculos, deformidade de Madelung,[17] bem como limitação da amplitude de movimento nas articulações que eles invadirem. Uma pessoa com osteocondromas múltiplos hereditários têm um risco aumentado de desenvolver uma forma rara de câncer ósseo chamado condrossarcoma quando chegar a fase adulta.[17] Problemas podem ocorrer mais tardiamente na vida e podem incluir ossos fracos e danos nos nervos.[18][19][20] A taxa relatada de transformações malignas pode variar de 0,57% [13] a 8,3% das pessoas com a doença.[21] Alguns autores relatam uma associação entre osteocondromas múltiplos hereditários e a presença de pseudoaneurismas poplíteos.[22]
Diagnóstico
[editar | editar código-fonte]O diagnóstico de osteocondromas múltiplos hereditários é baseado em uma correlação exata entre as características clínicas acima citadas e as características radiográficas. O histórico familiar pode fornecer um guia importantíssimo para o diagnóstico. Os exames são complementados por testes para os dois genes nos quais as variantes patogênicas são conhecidas por causar a doença, ou seja, os genes EXT1 e EXT2. Uma combinação da análise da sequência e a análise de deleção de todas as regiões codificantes de EXT1 e EXT2 detecta variantes patogênicas em 70 a 95% dos indivíduos afetados.[3][4]
A marca do diagnóstico radiográfico é a presença de osteocondromas nas extremidades metafisárias dos ossos longos, nos quais o córtex e a medula do osteocondroma configuram uma extensão contínua do osso hospedeiro. Essa imagem é facilmente vista em radiografias dos joelhos ou de áreas afetadas.[3][1]
Tratamento
[editar | editar código-fonte]As indicações para intervenção cirúrgica em indivíduos com osteocondromas múltiplos hereditários permanecem incertas e chegam a variar muito na literatura médica. Geralmente, o tratamento cirúrgico da doença inclui um ou mais dos seguintes procedimentos: excisão do osteocondroma; alongamento ósseo gradual ou agudo, tal qual o alongamento da ulna; osteotomias corretivas; hemiepifisiodese temporária para corrigir deformidades articulares angulares, como hemiepifisiodese do rádio distal e hemiepifisiodese da tíbia distal medial.[1][3] Todavia, há pouca evidência para apoiar a prática ortopédica pediátrica em andamento em osteocondromas múltiplos hereditários. O que quer dizer que revisões sistemáticas recentes encontraram evidências insuficientes para provar que o tratamento cirúrgico contínuo dos osteocondromas múltiplos hereditários melhora imensamente a função ou para provar que os mesmos afetam a qualidade de vida das crianças afetadas.[1][2]
Para aumentar a quantidade de evidências na literatura médica, algumas recomendações foram mostradas. Uma das ideias em alta é a construção de estudos prospectivos bem desenhados, que possam vir a fornecer uma associação mais clara entre procedimentos cirúrgicos, características dos pacientes e os resultados. Caso contrário, continuar seguindo os desenhos de estudo atuais continuará a levantar mais perguntas do que respostas, não ajudando a melhorar e progredir em relação ao tratamento da doença.[1][2]
A artroplastia total do quadril tem sido usada para remediar as osteocondromas múltiplas hereditárias graves e dolorosas da articulação do quadril. A artroplastia total do quadril em indivíduos com a doença é desafiadora devido à distorção da anatomia e às repetidas cirurgias realizadas para tratar queixas relacionadas à exostose.[23]
Epidemiologia
[editar | editar código-fonte]As osteocondromas múltiplas hereditárias são estimadas para ocorrerem em 1 em 50.000 pessoas.[16][20]
Referências
[editar | editar código-fonte]- ↑ a b c d e f g EL-Sobky, TA; Samir, S; Atiyya, AN; Mahmoud, S; Aly, AS; Soliman, R (21 de março de 2018). «Current paediatric orthopaedic practice in hereditary multiple osteochondromas of the forearm: a systematic review.». Sicot-J. 4. 10 páginas. PMC 5863686
 . PMID 29565244. doi:10.1051/sicotj/2018002
. PMID 29565244. doi:10.1051/sicotj/2018002
- ↑ a b c d Makhdom, AM; Jiang, F; Hamdy, RC; Benaroch, TE; Lavigne, M; Saran, N (20 de maio de 2014). «Hip joint osteochondroma: systematic review of the literature and report of three further cases.». Advances in Orthopedics. 2014. 180254 páginas. PMC 4054980
 . PMID 24963411. doi:10.1155/2014/180254
. PMID 24963411. doi:10.1155/2014/180254
- ↑ a b c d e Wuyts, W; Schmale, GA; Chansky, HA; et al. (21 de novembro de 2013). «Hereditary Multiple Osteochondromas.». University of Washington, Seattle. GeneReviews. PMID 20301413. Consultado em 24 de março de 2018
- ↑ a b c Alvarez, CM; De Vera, MA; Heslip, TR; Casey, B (setembro de 2007). «Evaluation of the anatomic burden of patients with hereditary multiple exostoses.». Clin Orthop Relat Res. 462: 73–79. PMID 17589361. doi:10.1097/BLO.0b013e3181334b51
- ↑ Darilek S, Wicklund C, Novy D, Scott A, Gambello M, Johnston D, Hecht J (maio de 2005). «Hereditary multiple exostosis and pain». Journal of Pediatric Orthopedy. 25 (3): 369–76. PMID 15832158. doi:10.1097/01.bpo.0000150813.18673.ad
- ↑ Irie F, Badie-Mahdavi H, Yamaguchi Y (março de 2012). «Autism-like socio-communicative deficits and stereotypies in mice lacking heparan sulfate». Proceedings of the National Academy of Sciences of the United States of America. 109 (13): 5052–6. Bibcode:2012PNAS..109.5052I. PMC 3323986
 . PMID 22411800. doi:10.1073/pnas.1117881109
. PMID 22411800. doi:10.1073/pnas.1117881109
- ↑ Cook A, Raskind W, Blanton SH, Pauli RM, Gregg RG, Francomano CA, Puffenberger E, Conrad EU, Schmale G, Schellenberg G (1993). «Genetic heterogeneity in families with hereditary multiple exostoses». American Journal of Human Genetics. 53 (1): 71–9. PMC 1682231
 . PMID 8317501
. PMID 8317501
- ↑ Wu YQ, Heutink P, de Vries BB, Sandkuijl LA, van den Ouweland AM, Niermeijer MF, Galjaard H, Reyniers E, Willems PJ, Halley DJ (1994). «Assignment of a second locus for multiple exostoses to the pericentromeric region of chromosome 11». Human Molecular Genetics. 3 (1): 167–71. PMID 8162019. doi:10.1093/hmg/3.1.167
- ↑ Le Merrer M, Legeai-Mallet L, Jeannin PM, Horsthemke B, Schinzel A, Plauchu H, Toutain A, Achard F, Munnich A, Maroteaux P (1994). «A gene for hereditary multiple exostoses maps to chromosome 19p». Human Molecular Genetics. 3 (5): 717–22. CiteSeerX 10.1.1.1028.5356
 . PMID 8081357. doi:10.1093/hmg/3.5.717
. PMID 8081357. doi:10.1093/hmg/3.5.717
- ↑ Zak BM, Crawford BE, Esko JD (2002). «Hereditary multiple exostoses and heparan sulfate polymerization». Biochimica et Biophysica Acta (BBA) - General Subjects. 1573 (3): 346–55. PMID 12417417. doi:10.1016/S0304-4165(02)00402-6
- ↑ Stieber JR, Dormans JP (2005). «Manifestations of hereditary multiple exostoses». The Journal of the American Academy of Orthopaedic Surgeons. 13 (2): 110–20. PMID 15850368. doi:10.5435/00124635-200503000-00004
- ↑ Jaeken J, Hennet T, Matthijs G, Freeze HH (2009). «CDG nomenclature: time for a change!». Biochim. Biophys. Acta. 1792 (9): 825–6. PMC 3917312
 . PMID 19765534. doi:10.1016/j.bbadis.2009.08.005
. PMID 19765534. doi:10.1016/j.bbadis.2009.08.005
- ↑ a b Legeai-Mallet L, Munnich A, Maroteaux P, Le Merrer M (julho de 1997). «Incomplete penetrance and expressivity skewing in hereditary multiple exostoses». Clinical Genetics. 52 (1): 12–6. PMID 9272707. doi:10.1111/j.1399-0004.1997.tb02508.x
- ↑ Faiyaz-Ul-Haque M, Ahmad W, Zaidi SH, et al. (agosto de 2004). «Novel mutations in the EXT1 gene in two consanguineous families affected with multiple hereditary exostoses (familial osteochondromatosis)». Clinical Genetics. 66 (2): 144–51. PMID 15253765. doi:10.1111/j.1399-0004.2004.00275.x
- ↑ a b Porter DE, Lonie L, Fraser M, et al. (setembro de 2004). «Severity of disease and risk of malignant change in hereditary multiple exostoses. A genotype-phenotype study». The Journal of Bone and Joint Surgery. British Volume. 86 (7): 1041–6. PMID 15446535. doi:10.1302/0301-620x.86b7.14815
|hdl-access=requer|hdl=(ajuda) - ↑ a b Turek's orthopaedics principles and their application 6th ed. Philadelphia: Lippincott Williams & Wilkins. 2005. 263 páginas. ISBN 9780781742986
- ↑ a b Davies, A. Mark; Pettersson, Holger (2002). Pettersson; Ostensen, eds. Radiography of the Musculoskeletal System (PDF). Geneva: World Health Organization. pp. 177, 189. ISBN 978-92-4-154555-6
- ↑ CANNON JF (1954). «Hereditary multiple exostoses». American Journal of Human Genetics. 6 (4): 419–25. PMC 1716573
 . PMID 14349947
. PMID 14349947
- ↑ McBride WZ (setembro de 1988). «Hereditary multiple exostoses». American Family Physician. 38 (3): 191–2. PMID 3046271
- ↑ a b Schmale GA, Conrad EU, Raskind WH (julho de 1994). «The natural history of hereditary multiple exostoses». The Journal of Bone and Joint Surgery. American Volume. 76 (7): 986–92. PMID 8027127. doi:10.2106/00004623-199407000-00005. Cópia arquivada em 20 de setembro de 2014
- ↑ Kivioja A, Ervasti H, Kinnunen J, Kaitila I, Wolf M, Böhling T (março de 2000). «Chondrosarcoma in a family with multiple hereditary exostoses». The Journal of Bone and Joint Surgery. British Volume. 82 (2): 261–6. PMID 10755438. doi:10.1302/0301-620X.82B2.0820261

- ↑ Parada Duarte O, Arambula Neira J, Castillo Herazo V, Oviedo Lara M, López Polanco A, Durán Omaña A, Herrera Ortiz AF. Popliteal artery pseudoaneurysm caused by non–penetrating trauma in a patient with hereditary multiple osteochondromatosis. Radiology Case Reports.2021;17(1):185-189. https://doi.org/10.1016/j.radcr.2021.10.025
- ↑ Vaishya, R; Swami, S; Vijay, V; Vaish, A (5 de janeiro de 2015). «Bilateral total hip arthroplasty in a young man with hereditary multiple exostoses.». BMJ Case Rep. 2015: bcr2014207853. PMC 4289752
 . PMID 25564594. doi:10.1136/bcr-2014-207853
. PMID 25564594. doi:10.1136/bcr-2014-207853