História da evolução molecular
| Parte de uma série sobre |
| Evolução |
|---|
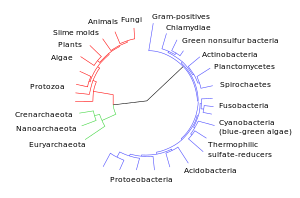 Diagrama da divergência dos grupos taxonómicos modernos em relação aos seus ancestrais comuns. |
|
Tópicos fundamentais |
A história da evolução molecular começa no início do século XX com a "bioquímica comparada", mas o campo da evolução molecular só se tornou independente durante as décadas de 1960 e 70, seguindo o aparecimento da biologia molecular e da descoberta das bases genéticas da evolução. O advento da sequenciação de proteínas permitiu que biólogos moleculares criassem comparação de proteínas à base de filogenias, e de usar as diferenças entre sequências homólogas como um relógio molecular para estimar o tempo decorrido desde o último ancestral comum. No fim da década de 60, a teoria neutral da evolução molecular forneceu a base teórica para o relógio molecular, embora tanto o relógio como a teoria neutral fossem controversas, uma vez que a maioria dos biólogos evolutivos se mantivessem fieis ao panseleccionismo, com a seleção natural como a única causa importante de mudanças evolutivas. Depois dos anos 70, a sequenciação de ácidos nucleicos permitiu que a evolução molecular chegasse para além das proteínas até sequências altamente conservadas de RNA ribossomal, a fundação para a reconceitualização do princípio da história da vida.
Primeiros tempos
[editar | editar código-fonte]Antes do surgimento da biologia molecular nas décadas de 1950 e 1960, alguns biólogos tinham explorado a possibilidade de usar diferenças bioquímicas entre espécies para estudar evolução. Ao longo do século 20, avanços científicos significativos revelaram como a evolução ocorre a nível molecular, envolvendo principalmente mudanças no DNA, proteínas e outros componentes celulares. Alfred Sturtevant previu a existência de inversões cromossômicas em 1921 e junto com Dobzhansky construiu uma das primeiras filogenias moleculares em 17 estirpes de Drosophila pseudoobscura a partir da acumulação de inversões cromossômicas observadas por hibridação de cromossomos politénicos.[1] Ernest Baldwin trabalhou extensivamente em bioquímica comparativa começando na década de 1930, e Marcel Florkin foi pioneiro de técnicas para a construção de filogenias baseadas em caracteres moleculares e bioquímicos na década de 1940. Contudo, só na década de 1950 é que biólogos desenvolveram técnicas para produzir dados bioquímicos para o estudo quantitativo de evolução molecular.[2]
Descobertas significativas (Décadas de 1950 e 1960)
[editar | editar código-fonte]Em 1953, James Watson e Francis Crick, com a ajuda de dados de Rosalind Franklin e Maurice Wilkins, descobriram a estrutura do DNA (ácido desoxirribonucleico), um passo fundamental para a compreensão da evolução molecular. O DNA foi identificado como o material genético responsável pela hereditariedade e pelas variações que surgem ao longo do tempo nas populações.[3]
A primeira investigação de sistemática molecular baseou-se em ensaios imunológicos e "fingerprinting" proteíco. Alan Boyden, expandindo métodos imunológicos de G. H. F. Nuttall, desenvolveu novas técnicas começando em 1954, e no início da década de 60 Curtis Williams e Morris Goodman usaram comparações imunológicas para estudar a filogenia dos primatas. Outros, como Linus Pauling e os seus estudantes, aplicaram uma combinação de eletroforese e cromatografia em papel recentemente desenvolvida para criar padrões bi-dimensionais de proteínas submetidas a digestão parcial por enzimas digestivas, permitindo comparações finas entre proteínas homólogas.[4]
Durante as décadas seguintes, cientistas como Marshall Nirenberg e Heinrich Matthaei decifram o código genético, que determina como as sequências de DNA são traduzidas em proteínas. Isso permitiu compreender como a informação genética é copiada e transmitida, e como as variações podem ocorrer.[5]
Avanços posteriores (1970-1980)
[editar | editar código-fonte]Em 1970 foram descobertas as enzimas de restrição em estudos com a Haemophilius influenzae, permitindo aos cientistas o corte do DNA e a sua transferência entre organismos. Foi uma das mais importantes descobertas na história da genética molecular. Essas enzimas são proteínas que atuam como "corte" de DNA em locais específicos, de acordo com sequências de bases nitrogenadas. As enzimas de restrição são fundamentais para a clonagem de genes e para muitas técnicas de manipulação do DNA.[6] Na mesma década, a teoria da evolução de Charles Darwin, que se baseia em variações e seleção natural, foi combinada com a biologia molecular. Essa combinação resultou na teoria da "síntese molecular", que afirmou que as mutações no DNA e a recombinação genética são as principais fontes de variação genética, e essas variações são selecionadas ao longo do tempo com base na adaptação ao ambiente. As mutações podem ser causadas por diversos fatores, como radiação ou erros na replicação do DNA. A seleção natural age sobre essas mutações, favorecendo aquelas que conferem uma vantagem adaptativa.[7] Theodosius Dobzhansky foi um dos pioneiros dessa integração entre a evolução darwiniana e a genética molecular.[8]
Em 1977 , Frederick Sanger, Walter Gilbert e Allan Maxam sequenciaram o DNA pela primeira vez. Assim foi descrito um novo método para determinar sequências de nucleotídeos em DNA, conhecido como método Sanger, o qual faz uso dos análogos 2',3'-didesoxi e arabinonucleosídeos dos trifosfatos de desoxirribonucleosídeos (DNTP’s), que atuam como inibidores específicos de terminação de cadeia para a DNA polimerase.[9] Essa técnica foi aplicada para sequenciar o genoma do bacteriófago Phi-X174 o primeiro genoma completamente sequenciado.[10] O método Sanger permitiu o mapeamento de genes e a comparação das sequências de DNA entre diferentes organismos. Isso revelou a diversidade genética e como ela se relaciona com a evolução.
Werner Arber, Daniel Nathans, Hamilton O. Smith receberam o Prêmio Nobel de Fisiologia ou Medicina em 1978 pela descoberta das enzimas de restrição e suas aplicações na genética molecular.[11] Outra descoberta importante para os estudos da evolução molecular foi a reação de polimerização em cadeia (en:PCR) por Kary Banks Mullis em 1983, o que proporcionou amplificar o DNA com facilidade.[12] Na sequência, a genética de populações aplicou os princípios da evolução molecular à biologia de populações. Os estudos de como as mutações se propagam em uma população, e como a seleção natural e a deriva genética afetam as frequências alélicas, foram cruciais para compreender a evolução a nível molecular.[13] Em 1993, Kary Mullis foi reconhecido com o Prêmio Nobel de Química devido a esta descoberta.[14]
Evolução molecular e bioinformática (1990-presente)
[editar | editar código-fonte]O sequenciamento completo do genoma de organismos possibilitou a análise da evolução molecular de forma revolucionária. O Projeto Genoma Humano, iniciado na década de 1990 marcou impacto significativo ao comparar genomas de diferentes espécies, os cientistas passaram a traçar as relações evolutivas entre elas.[15] A análise de genomas, conhecida como genômica é uma ferramenta-chave para compreender processos biológicos fundamentais, variabilidade genética e doenças. Com o uso de genômica comparativa é possível traçar relações entre espécies e identificar elementos conservados no genoma. A evolução molecular não ocorre apenas em nível de DNA, mas também em nível de proteínas, onde pequenas mudanças podem afetar a função e, assim, a adaptação e sobrevivência dos organismos. A análise das proteínas, conhecida como proteômica, incluindo suas estruturas e funções, também avançou significativamente. A proteômica é essencial para compreender os produtos da expressão gênica, os mecanismos moleculares das células e a adaptação de organismos. Para gerenciar, analisar e interpretar a enorme quantidade de dados gerados pela genômica e proteômica é utilizada a bioinformática. Esse campo interdisciplinar utiliza algoritmos, bancos de dados e ferramentas computacionais para resolver problemas biológicos, como o alinhamento de sequências, predição de estruturas proteicas e análise funcional de genes.[16]
Nos anos 1990 e 2000, o desenvolvimento da bioinformática acelerou a capacidade de analisar grandes volumes de dados genômicos, tornando a construção de árvores filogenéticas mais precisa e detalhada.[17][18] O uso de algoritmos de bioinformática tem facilitado a análise de grandes volumes de dados genéticos, revelando detalhes sobre como as espécies se diversificaram ao longo do tempo.[19][20]
O futuro da evolução molecular
[editar | editar código-fonte]Pesquisas mais recentes permitem observar como as populações de organismos evoluem em tempo real, especialmente em laboratórios, onde mutações podem ser induzidas e observadas.[21] Isso oferece uma visão mais dinâmica e precisa da evolução molecular.
A descoberta do sistema CRISPR-Cas como ferramenta de edição genética,[22] tornou possível modificar o DNA de forma altamente específica e eficiente. Essa tecnologia não apenas amplia a capacidade de estudar a evolução molecular em tempo real, mas também permite realizar seleções evolutivas dirigidas, acelerando o entendimento dos mecanismos genéticos subjacentes à adaptação e à variação. As aplicações recentes, como CRISPR-Cas9 evolutivo,[23] possibilitam simular e testar cenários evolutivos no laboratório, impulsionando áreas como a genética de populações, a biotecnologia e a engenharia de organismos.
Referências
- ↑ Dobzhansky, Th; Sturtevant, A H (1 de janeiro de 1938). «INVERSIONS IN THE CHROMOSOMES OF DROSOPHILA PSEUDOOBSCURA». Genetics (1): 28–64. ISSN 1943-2631. doi:10.1093/genetics/23.1.28. Consultado em 30 de janeiro de 2025
- ↑ Zuckerkandl, Emile (novembro de 1987). «On the molecular evolutionary clock». Journal of Molecular Evolution (1-2): 34–46. ISSN 0022-2844. doi:10.1007/bf02111280. Consultado em 30 de janeiro de 2025
- ↑ Watson, J. D.; Crick, F. H. C. (25 de abril de 1953). «Molecular Structure of Nucleic Acids: A Structure for Deoxyribose Nucleic Acid». Nature (em inglês) (4356): 737–738. ISSN 0028-0836. doi:10.1038/171737a0. Consultado em 30 de janeiro de 2025
- ↑ ZUCKERKANDL, EMILE; PAULING, LINUS (1965). «Evolutionary Divergence and Convergence in Proteins». Elsevier: 97–166. ISBN 978-1-4832-2734-4. Consultado em 30 de janeiro de 2025
- ↑ Nirenberg, Marshall W.; Matthaei, J. Heinrich (outubro de 1961). «The dependence of cell-free protein synthesis in E. coli upon naturally occurring or synthetic polyribonucleotides». Proceedings of the National Academy of Sciences (em inglês) (10): 1588–1602. ISSN 0027-8424. PMC PMC223178
 Verifique
Verifique |pmc=(ajuda). PMID 14479932. doi:10.1073/pnas.47.10.1588. Consultado em 30 de janeiro de 2025 - ↑ Smith, Hamilton O.; Welcox, K.W. (julho de 1970). «A Restriction enzyme from Hemophilus influenzae». Journal of Molecular Biology (2): 379–391. ISSN 0022-2836. doi:10.1016/0022-2836(70)90149-x. Consultado em 30 de janeiro de 2025
- ↑ Harrison, G. Ainsworth (janeiro de 1972). «Genetics of the Evolutionary Process. By Theodosius Dobzhansky. Pp. 505. (Columbia University Press, New York and London, 1970). Price £4.95.». Journal of Biosocial Science (1): 137–140. ISSN 0021-9320. doi:10.1017/s0021932000008403. Consultado em 30 de janeiro de 2025
- ↑ Mayr, Ernst; Dobzhansky, Theodosius; Ayala, Francisco; Stebbins, G. Ledyard; Valentine, James W. (dezembro de 1977). «An Almost Comprehensive Survey of Evolution». Evolution (4). 913 páginas. ISSN 0014-3820. doi:10.2307/2407458. Consultado em 30 de janeiro de 2025
- ↑ Sanger, F.; Nicklen, S.; Coulson, A. R. (dezembro de 1977). «DNA sequencing with chain-terminating inhibitors». Proceedings of the National Academy of Sciences (12): 5463–5467. ISSN 0027-8424. doi:10.1073/pnas.74.12.5463. Consultado em 30 de janeiro de 2025
- ↑ Sanger, F.; Air, G. M.; Barrell, B. G.; Brown, N. L.; Coulson, A. R.; Fiddes, J. C.; Hutchison, C. A.; Slocombe, P. M.; Smith, M. (fevereiro de 1977). «Nucleotide sequence of bacteriophage φX174 DNA». Nature (5596): 687–695. ISSN 0028-0836. doi:10.1038/265687a0. Consultado em 30 de janeiro de 2025
- ↑ MEITES, J. (6 de janeiro de 1978). «Nobel Prize in Physiology or Medicine». Science (4324): 7–7. ISSN 0036-8075. doi:10.1126/science.199.4324.7. Consultado em 30 de janeiro de 2025
- ↑ Mullis, Kary B.; Faloona, Fred A. (1987). «[21] Specific synthesis of DNA in vitro via a polymerase-catalyzed chain reaction». Elsevier: 335–350. ISBN 978-0-12-182056-5. Consultado em 30 de janeiro de 2025
- ↑ Ninio, Jacques (7 de maio de 1984). «The Neutral Theory of Molecular Evolution». FEBS Letters (1): 210–211. ISSN 0014-5793. doi:10.1016/0014-5793(84)81411-8. Consultado em 30 de janeiro de 2025
- ↑ ТЮТЮННИК В, М. (28 de outubro de 2024). «ЛАУРЕАТЫ НОБЕЛЕВСКИХ ПРЕМИЙ - ЧЛЕНЫ КОРОЛЕВСКОЙ ШВЕДСКОЙ АКАДЕМИИ НАУК». История науки и техники (10). ISSN 1813-100X. doi:10.25791/intstg.10.2024.1504. Consultado em 30 de janeiro de 2025
- ↑ International Human Genome Sequencing Consortium; Whitehead Institute for Biomedical Research, Center for Genome Research:; Lander, Eric S.; Linton, Lauren M.; Birren, Bruce; Nusbaum, Chad; Zody, Michael C.; Baldwin, Jennifer; Devon, Keri (15 de fevereiro de 2001). «Initial sequencing and analysis of the human genome». Nature (em inglês) (6822): 860–921. ISSN 0028-0836. doi:10.1038/35057062. Consultado em 30 de janeiro de 2025
- ↑ Gregerson, Robert G.; Lindblom, Tim H. (janeiro de 2008). «A Unique Textbook for Teaching Courses in Bioinformatics [review of Discovering Genomics, Proteomics, and Bioinformatics, 2nd ed. (Cummings, B.; 2006)]». Computing in Science & Engineering (1): 7–8. ISSN 1521-9615. doi:10.1109/mcse.2008.3. Consultado em 30 de janeiro de 2025
- ↑ Altschul, S. (1 de setembro de 1997). «Gapped BLAST and PSI-BLAST: a new generation of protein database search programs». Nucleic Acids Research (17): 3389–3402. PMC PMC146917
 Verifique
Verifique |pmc=(ajuda). PMID 9254694. doi:10.1093/nar/25.17.3389. Consultado em 30 de janeiro de 2025 - ↑ Penny, David (1 de agosto de 2004). «Inferring Phylogenies.—Joseph Felsenstein. 2003. Sinauer Associates, Sunderland, Massachusetts.». Systematic Biology (4): 669–670. ISSN 1076-836X. doi:10.1080/10635150490468530. Consultado em 30 de janeiro de 2025
- ↑ Ronquist, Fredrik; Huelsenbeck, John P. (12 de agosto de 2003). «MrBayes 3: Bayesian phylogenetic inference under mixed models». Bioinformatics (em inglês) (12): 1572–1574. ISSN 1367-4811. doi:10.1093/bioinformatics/btg180. Consultado em 30 de janeiro de 2025
- ↑ Tamura, K.; Dudley, J.; Nei, M.; Kumar, S. (18 de abril de 2007). «MEGA4: Molecular Evolutionary Genetics Analysis (MEGA) Software Version 4.0». Molecular Biology and Evolution (8): 1596–1599. ISSN 0737-4038. doi:10.1093/molbev/msm092. Consultado em 30 de janeiro de 2025
- ↑ Barrick, Jeffrey E.; Yu, Dong Su; Yoon, Sung Ho; Jeong, Haeyoung; Oh, Tae Kwang; Schneider, Dominique; Lenski, Richard E.; Kim, Jihyun F. (outubro de 2009). «Genome evolution and adaptation in a long-term experiment with Escherichia coli». Nature (em inglês) (7268): 1243–1247. ISSN 0028-0836. doi:10.1038/nature08480. Consultado em 30 de janeiro de 2025
- ↑ Jinek, Martin; Chylinski, Krzysztof; Fonfara, Ines; Hauer, Michael; Doudna, Jennifer A.; Charpentier, Emmanuelle (17 de agosto de 2012). «A Programmable Dual-RNA–Guided DNA Endonuclease in Adaptive Bacterial Immunity». Science (em inglês) (6096): 816–821. ISSN 0036-8075. PMC PMC6286148
 Verifique
Verifique |pmc=(ajuda). PMID 22745249. doi:10.1126/science.1225829. Consultado em 30 de janeiro de 2025 - ↑ Shalem, Ophir; Sanjana, Neville E.; Hartenian, Ella; Shi, Xi; Scott, David A.; Mikkelsen, Tarjei S.; Heckl, Dirk; Ebert, Benjamin L.; Root, David E. (3 de janeiro de 2014). «Genome-Scale CRISPR-Cas9 Knockout Screening in Human Cells». Science (em inglês) (6166): 84–87. ISSN 0036-8075. PMC PMC4089965
 Verifique
Verifique |pmc=(ajuda). PMID 24336571. doi:10.1126/science.1247005. Consultado em 30 de janeiro de 2025