Heparan-sulfat

.
Heparan-sulfat (HS) je linearni polisaharid koji se nalazi u svim životinjskim tkivima.[1] Javlja se kao proteoglikan (HSPG, tj. Heparan-sulfat proteoglikan) u kojem su dva ili tri HS lanca vezana u neposrednoj blizini površine ćelije ili vanćelijskog matriksa proteina.[2][3] U ovom obliku se HS vezuje za različite proteinske ligande, uključujući Wnt,[4][5] i reguliše širok spektar bioloških aktivnosti, uključujući razvojne procese, angiogenezu, koagulaciju krvi, ukidajući aktivnost odvajanja GrB (granzim B),[6] i tumorske metastaze. Također se pokazalo da HS služi kao ćelijski receptor za brojne viruse, uključujući respiratorni sincicijski virus.[7] Jedna studija sugerira da ćelijski heparan-sulfat ima ulogu u infekciji SARS-CoV-2, posebno kada se virus veže s ACE2.[8]
Proteoglikani
[uredi | uredi izvor]Glavni HSPG-ovi ćelijske membrane su transmembranski sindekani i glikozilfosfatidilinozitoli (GPI) usidreni glipikani.[9][10] Drugi manji oblici membranskog HSPG-a uključuju betaglikan[11] i V-3 izoformu CD44 prisutnu na keratinocitima i aktiviranim monocitima.[12]
U vanćelijskom matriksu, posebno baznim membranama i fraktonima, multi-domenski perlekan, agrin i kolagena XVIII proteini jedrae su glavni tipovi koje nose HS.
Struktura i razlike od heparina
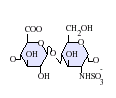
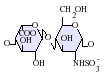
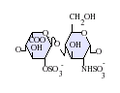
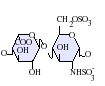
[uredi | uredi izvor]Heparan-sulfat je član glikozaminoglikanske porodice ugljikohidrata i veoma je blisko povezan po strukturi sa heparinom. Heparin, poznat kao antikoagulans, je visoko sulfatirani oblik HS koji se, za razliku od HS, uglavnom nalazi u sekretornim granulama mastocita.[13] Oba se sastoje od varijabilno sulfatirane ponavljajuće disaharidne jedinice. Glavne disaharidne jedinice koje se javljaju u heparan-sulfatu i heparinu prikazane su u nastavku.
Najčešća disaharidna jedinica u heparanasulfatu sastoji se od glukuronske kiseline (GlcA) povezane sa N-acetilglukozaminom (GlcNAc), obično čini oko 50% ukupne disaharidne jedinice. Uporedite ovo sa heparinom, gde IdoA(2S)-GlcNS(6S) čini 85% heparina iz goveđih pluća i oko 75% heparina iz svinjske crijevne sluzokože. Problemi nastaju prilikom definiranja hibridnih GAG-ova koji sadrže i strukture slične 'heparinu' i 'HS-like'. Predloženo je da GAG treba da se kvalifikuje kao heparin samo ako njegov sadržaj N-sulfatnih grupa uveliko premašuje N-acetilne grupe, a koncentracija O-sulfatnih grupa premašuje onu N-sulfatnih.[14]
Dolje nisu prikazani rijetki disaharidi koji sadrže 3-O-sulfat glukozamin (GlcNS(3S,6S) ili slobodnu amino grupu (GlcNH3+). U fiziološkim uslovima esterske i amidne sulfatne grupe se deprotoniraju i privlače pozitivno nabijene kontraione da formiraju so. Smatra se da u tom obliku HS postoji na površini ćelije.
-
GlcA-GlcNAc
-
GlcA-GlcNS
-
IdoA-GlcNS
-
IdoA(2S)-GlcNS
-
IdoA-GlcNS(6S)
-
IdoA(2S)-GlcNS(6S)
Skraćenice
[uredi | uredi izvor]- GlcA = β-D-glukuronska kiselina
- IdoA = α-L-iduronska kiselina
- IdoA(2S) = 2-O-sulfo-α-L-iduronska kiselina
- GlcNAc = 2-deoksi-2-acetamido-α-D-glukopiranozil
- GlcNS = 2-deoksi-2-sulfamido-α-D-glukopiranozil
- GlcNS(6S) = 2-deoksi-2-sulfamido-α-D-glukopiranozil-6-O-sulfat
Biosinteza
[uredi | uredi izvor]Mnogo različitih tipova ćelija proizvodi HS lance sa mnogo različitih primarnih struktura. Stoga postoji velika varijabilnost u načinu na koji se sintetiziraju HS lanci, stvarajući strukturnu raznolikost obuhvaćenu pojmom "heparanom" - koji definira cijeli niz primarnih struktura koje proizvodi određena ćelija, tkivo ili organizam.[15] Međutim, od suštinskog značaja za formiranje HS bez obzira na primarnu sekvencu je niz biosintetskih enzima. Ovi enzimi se sastoje od više glikoziltransferaza, sulfotransferaza i epimeraza. Ti isti enzimi takođe sintetišu heparin.
1980-ih, Jeffrey Esko je bio prvi koji je izolirao i karakterizirao mutante životinjskih ćelija izmijenjene u sklopu heparan-sulfata.[16] Mnogi od ovih enzima su sada pročišćeni, molekulski klonirani i obrasci njihove ekspresije su proučavani. Iz ovog i ranog rada na osnovnim fazama biosinteze HS/heparina koristeći sistem bez ćelija mastocitoma miša, mnogo se zna o redoslijedu enzimskih reakcija i specifičnosti.[17]
Iniciranje lanca
[uredi | uredi izvor]
Sinteza HS započinje prijenosom ksiloze sa UDP-ksiloze pomoću ksiloziltransferaza (XT) na specifične serinske ostatke unutar proteinskog jezgra. Spajanje dva galaktozna (Gal) ostatka galaktoziltransferazama I i II (GalTI i GalTII) i glukuronske kiseline (GlcA) pomoću glukuronoziltransferaze I (GlcATI) dovršava formiranje tetrasaharidnog prajmera O-vezanog za serin jezgarnih proteina: βGlcUA-(1→3)-βGal-(1→3)-βGal-(1→4)-βXyl-O-Ser.
Smatra se da se vezivanje ksiloze za jezgarni protein javlja u endoplazmatskom retikulumu (ER) sa daljim sastavljanjem regiona veze i ostatka lanca koji se javlja u Golgijevom aparatu.
Putevi biosinteze HS/heparina ili hondroitin-sulfat (CS) i dermatan-sulfat (DS) se razlikuju nakon formiranja ove zajedničke strukture tetrasaharidne veze. Sljedeći enzim koji djeluje, GlcNAcT-I ili GalNAcT-I, usmjerava sintezu, bilo na HS/heparin ili CS/DS.
Elongacija lanca
[uredi | uredi izvor]Nakon vezivanja prvog N-acetilglukozaminskog (GlcNAc) ostatka, produženje tetrasakridnog linkera nastavlja se postupnim dodavanjem GlcA i GlcNAc ostataka. Oni se prenose sa svojih odgovarajućih UDP-šećernih nukleotida. Ovo se provodi pomoću jednog ili više srodnih enzima čiji su geni članovi porodice egzostoznih gena (EXT) tumorskih supresora.
Mutacije na EXT1-3 genskim lokusima kod ljudi dovode do nesposobnosti ćelija da proizvode HS i do razvoja bolesti multiple nasljedne egzostoze (MHE). MHE karakteriziraju tumori prekriveni hrskavicom, poznati kao osteohondromi ili egzostoze, koji se prvenstveno razvijaju na dugim kostima oboljelih osoba od ranog djetinjstva do puberteta.[18]
Modifikacija lanca
[uredi | uredi izvor][Kako se HS lanac polimerizira, on prolazi kroz niz reakcija modifikacije koje provode četiri klase sulfotransferaza i epimeraza. Dostupnost donora sulfata PAPS je ključna za aktivnost sulfotransferaza.[19][20]
N-deacetilacija/N-sulfacija
[uredi | uredi izvor]Prva modifikacija polimera je N-deacetilacija/N-sulfatacija GlcNAc ostataka u GlcNS. Ovo je preduslov za sve naknadne modifikacione reakcije, a provodi ga jedan ili više članova porodice od četiri enzima GlcNAc N-deacetilaze/N-sulfotransferaze (NDST). U ranim studijama je pokazano da modificirajući enzimi mogu prepoznati i djelovati na bilo koji N-acetilirani ostatak u polimeru koji se formira.[21] Stoga bi se modifikacija GlcNAc ostataka trebala dogoditi nasumično u cijelom lancu. Međutim, u HS, N-sulfirani ostaci su uglavnom grupirani zajedno i razdvojeni regijama N-acetilacije gdje GlcNAc ostaje nemodificiran.
Postoje četiri izoforme NDST (NDST1–4). Aktivnosti N-deacetilaze i N-sulfotransferaze prisutne su u svim NDST-izoformama, ali se značajno razlikuju u svojim enzimskim aktivnostima.[22]
Generiranje GlcNH2
[uredi | uredi izvor]Zbog toga što se N-deacetilaza i N-sulfotransferaza provode istim enzimom, N-sulfatacija je normalno čvrsto povezana sa N-acetilacijom. Ostaci GlcNH2 koji su rezultat očiglednog razdvajanja dvije aktivnosti pronađeni su u heparinu i nekim vrstama HS.[23]
Epimerizacija i 2-O-sulfatacija
[uredi | uredi izvor]Epimerizaciju katalizira jedan enzim, GlcA C5 epimeraza ili heparosan-N-sulfat-glukuronat 5-epimeraza (EC 5.1.3.17). Ovaj enzim epimerizuje GlcA u iduronsku kiselinu (IdoA). Prepoznavanje supstrata zahteva da ostatak GlcN vezan za neredukcionu stranu potencijalne GlcA mete bude N-sulfat. Uronozil-2-O-sulfotransferaza (2OST) sulfatira rezultirajuće ostatke IdoA.
6-O-sulfacija
[uredi | uredi izvor]Identificirane su tri glukozaminil 6-O-transferaze (6OSTs) koje rezultiraju stvaranjem GlcNS(6S), pored sulfatnog ili nesulfatnog IdoA. GlcNAc(6S) se također nalazi u zrelim HS lancima.
3-O-sulfacija
[uredi | uredi izvor]Do sada je poznato da sedam glukozaminil 3-O-sulfotransferaza (3OSTs, HS3STs) postoji kod sisara (osam kod zebrica).[24][25] Enzimi 3OST stvaraju brojne moguće 3-O-sulfatne disaharide, uključujući GlcA-GlcNS(3S±6S) (modificiran putem HS3ST1 i HS3ST5), IdoA(2S)-GlcNH2(3S±6S) (modificirano prema HS3ST3A1, HS3ST3B1, HS3ST5 i HS3ST6) i GlcA/IdoA(2S)-GlcNS( 3S) (izmijenjeno od strane HS3ST2 i HS3ST4).[26][27][28][29] Kao i kod svih drugih HS sulfotransferaza, 3OST koriste 3'-fosfoadenozin-5'-fosfosulfat (PAPS) kao donatora sulfata. Uprkos tome što su najveća porodica enzima za modifikaciju HS, 3OST proizvode najrjeđu HS modifikaciju, 3-O-sulfataciju specifičnih ostataka glukozamina u C3-OH ostatku.[30]
3OST su podijeljeni u dvije funkcionalne potkategorije, one koje stvaraju antitrombin III mjesto vezanja (HS3ST1 i HS3ST5) i one koje stvaraju herpes simplex virus 1 glikoprotein D ( HSV-1 gD) mjesto vezanja (HS3ST2, HS3ST3A1, HS3ST3B1, HS3ST4, HS3ST5 i HS3ST6).[26][27][28][29][31][32][33][34][35][36][37] Kako su 3OST najveća porodica enzima za modifikaciju HS i njihovo djelovanje ograničava brzinu, specifično za supstrat i proizvodi rijetke modifikacije, pretpostavlja se da 3OST modificirani HS ima važnu regulatornu ulogu u biološkim procesima.[29][32] Pokazalo se da 3-O-sulfatacija može poboljšati vezivanje Wnt za glipikan i može igrati ulogu u regulaciji Wnt kod raka.[5][10]
Vezivanje liganda
[uredi | uredi izvor]Heparan-sulfat se veže sa velikim brojem vanćelijskih proteina. Oni se često zajednički nazivaju "heparin interaktom" ili "heparin-vezujući proteini", jer su izolovani afinitetnom hromatografijom na srodnom polisaharidnom heparinu, iako je termin "heparan sulfat interaktom" ispravniji. Funkcije proteina koji vežu heparan-sulfat kreću se od komponenti vanćelijskog matriksa, do enzima i faktora koagulacije, te većine faktora rasta, citokina, hemokina i morfogena.[38] Laboratorija dr. Mitchella Hoa na NCI-u izolovala je ljudsko monoklonsko antitijelo HS20 s visokim afinitetom za heparan-sulfat, putem displeja faga.[39] Antitijelo vezuje heparan-sulfat, a ne hondroitin sulfat.[5] Vezivanje HS20 za heparan-sulfat zahteva sulfatizaciju i na poziciji C2 i na poziciji C6. HS20 blokira vezivanje Wnt na heparan-sulfat[5] i također inhibira infektivni ulazak patogenog JC poliom virusa.[40]
Interferon-γ
[uredi | uredi izvor]Vezujući region za receptor na površini ćelije, Interferon-γ preklapa se sa HS vezujućim regionom, blizu C-terminala proteina. Vezivanje HS blokira mjesto vezanja receptora i kao rezultat toga, kompleksi protein-HS su neaktivni.[41]
Wnt
[uredi | uredi izvor]Glipikan-3 (GPC3) stupa u interakciju sa Wnt i ukrućenom strukturom, kako bi formirao kompleks i pokreće nizvodnu signalizaciju.[4][10] Eksperimentalno je utvrđeno da Wnt prepoznaje motiv heparan-sulfata na GPC3, koji sadrži IdoA2S i GlcNS6S, i da 3-O-sulfatacija u GlcNS6S3S pojačava vezivanje Wnt za glipikan.[5] Također se proučavaju svojstva vezivanja HS brojnih drugih proteina:
- Antitrombin III
- Faktori rasta fibroblasta
- Faktor rasta hepatocita
- Interleukin-8
- Faktor rasta vaskularnog endotela
- Wnt/Beskrilnost
- Endostatin
Analog heparan sulfata
[uredi | uredi izvor]Smatra se da analozi heparan-sulfata pokazuju identična svojstva kao i heparan-sulfat, osim što su stabilni u proteolitskom okruženju kao što je rana.[42][43] Budući da se heparan-sulfat u hroničnim ranama razgrađuje heparanazom, analozi se vezuju samo za mjesta na kojima nema prirodnog heparan-sulfata i ne mogu ga razgraditi nijedne poznate heparanaze i glikanaze. Također, funkcija analoga heparan-sulfata je ista kao i heparan-sulfata, štiteći različite proteinske ligande, kao što su faktori rasta i citokini. Držeći ih na mjestu, za proliferaciju tkivo može koristiti različite proteinske ligande.
Reference
[uredi | uredi izvor]- ^ Medeiros GF, Mendes A, Castro RA, Baú EC, Nader HB, Dietrich CP (juli 2000). "Distribution of sulfated glycosaminoglycans in the animal kingdom: widespread occurrence of heparin-like compounds in invertebrates". Biochimica et Biophysica Acta (BBA) - General Subjects. 1475 (3): 287–94. doi:10.1016/S0304-4165(00)00079-9. PMID 10913828.
- ^ Gallagher JT, Lyon M (2000). "Molecular structure of Heparan Sulfate and interactions with growth factors and morphogens". u Iozzo MV (ured.). Proteoglycans: structure, biology and molecular interactions. New York, New York: Marcel Dekker Inc. str. 27–59.
- ^ Iozzo RV (1998). "Matrix proteoglycans: from molecular design to cellular function". Annual Review of Biochemistry. 67: 609–52. doi:10.1146/annurev.biochem.67.1.609. PMID 9759499. S2CID 14638091.
- ^ a b Gao W, Kim H, Feng M, Phung Y, Xavier CP, Rubin JS, Ho M (august 2014). "Inactivation of Wnt signaling by a human antibody that recognizes the heparan sulfate chains of glypican-3 for liver cancer therapy". Hepatology. 60 (2): 576–87. doi:10.1002/hep.26996. PMC 4083010. PMID 24492943.
- ^ a b c d e Gao W, Xu Y, Liu J, Ho M (maj 2016). "Epitope mapping by a Wnt-blocking antibody: evidence of the Wnt binding domain in heparan sulfate". Scientific Reports. 6: 26245. Bibcode:2016NatSR...626245G. doi:10.1038/srep26245. PMC 4869111. PMID 27185050.
- ^ Buzza MS, Zamurs L, Sun J, Bird CH, Smith AI, Trapani JA, et al. (juni 2005). "Extracellular matrix remodeling by human granzyme B via cleavage of vitronectin, fibronectin, and laminin". The Journal of Biological Chemistry. 280 (25): 23549–58. doi:10.1074/jbc.M412001200. PMID 15843372.
- ^ Hallak LK, Spillmann D, Collins PL, Peeples ME (novembar 2000). "Glycosaminoglycan sulfation requirements for respiratory syncytial virus infection". Journal of Virology. 74 (22): 10508–13. doi:10.1128/JVI.74.22.10508-10513.2000. PMC 110925. PMID 11044095.
- ^ Clausen TM, Sandoval DR, Spliid CB, Pihl J, Perrett HR, Painter CD, et al. (14. 9. 2020). "SARS-CoV-2 Infection Depends on Cellular Heparan Sulfate and ACE2". The Journal of Cell. 183 (4): 1043–1057.e15. doi:10.1016/j.cell.2020.09.033. PMC 7489987. PMID 32970989.
- ^ Ho M, Kim H (februar 2011). "Glypican-3: a new target for cancer immunotherapy". European Journal of Cancer. 47 (3): 333–8. doi:10.1016/j.ejca.2010.10.024. PMC 3031711. PMID 21112773.
- ^ a b c Li N, Gao W, Zhang YF, Ho M (novembar 2018). "Glypicans as Cancer Therapeutic Targets". Trends in Cancer. 4 (11): 741–754. doi:10.1016/j.trecan.2018.09.004. PMC 6209326. PMID 30352677.
- ^ Andres JL, DeFalcis D, Noda M, Massagué J (mart 1992). "Binding of two growth factor families to separate domains of the proteoglycan betaglycan". The Journal of Biological Chemistry. 267 (9): 5927–30. doi:10.1016/S0021-9258(18)42643-9. PMID 1556106.
- ^ Jackson DG, Bell JI, Dickinson R, Timans J, Shields J, Whittle N (februar 1995). "Proteoglycan forms of the lymphocyte homing receptor CD44 are alternatively spliced variants containing the v3 exon". The Journal of Cell Biology. 128 (4): 673–85. doi:10.1083/jcb.128.4.673. PMC 2199896. PMID 7532175.
- ^ Sarrazin S, Lamanna WC, Esko JD (juli 2011). "Heparan Sulfate Proteoglycans". Cold Spring Harb Perspect Biol. 3 (7): a004952. doi:10.1101/cshperspect.a004952. PMC 3119907. PMID 21690215.
- ^ Gallagher JT, Walker A (septembar 1985). "Molecular distinctions between heparan sulphate and heparin. Analysis of sulphation patterns indicates that heparan sulphate and heparin are separate families of N-sulphated polysaccharides". The Biochemical Journal. 230 (3): 665–74. doi:10.1042/bj2300665. PMC 1152670. PMID 2933029.
- ^ Turnbull J, Powell A, Guimond S (februar 2001). "Heparan sulfate: decoding a dynamic multifunctional cell regulator". Trends in Cell Biology. 11 (2): 75–82. doi:10.1016/s0962-8924(00)01897-3. PMID 11166215.
- ^ Esko JD, Stewart TE, Taylor WH (maj 1985). "Animal cell mutants defective in glycosaminoglycan biosynthesis". Proceedings of the National Academy of Sciences of the United States of America. 82 (10): 3197–201. Bibcode:1985PNAS...82.3197E. doi:10.1073/pnas.82.10.3197. PMC 397742. PMID 3858816.
- ^ Lindahl U, Kusche-Gullberg M, Kjellén L (septembar 1998). "Regulated diversity of heparan sulfate". The Journal of Biological Chemistry. 273 (39): 24979–82. doi:10.1074/jbc.273.39.24979. PMID 9737951.
- ^ Beltrami G, Ristori G, Scoccianti G, Tamburini A, Capanna R (2016). "Hereditary Multiple Exostoses: a review of clinical appearance and metabolic pattern". Clinical Cases in Mineral and Bone Metabolism. 13 (2): 110–118. doi:10.11138/ccmbm/2016.13.2.110. PMC 5119707. PMID 27920806.
- ^ Silbert JE (novembar 1967). "Biosynthesis of heparin. 3. Formation of a sulfated glycosaminoglycan with a microsomal preparation from mast cell tumors". The Journal of Biological Chemistry. 242 (21): 5146–52. doi:10.1016/S0021-9258(18)99487-1. PMID 4228675.
- ^ Carlsson P, Presto J, Spillmann D, Lindahl U, Kjellén L (juli 2008). "Heparin/heparan sulfate biosynthesis: processive formation of N-sulfated domains". The Journal of Biological Chemistry. 283 (29): 20008–14. doi:10.1074/jbc.M801652200. PMID 18487608.
- ^ Höök M, Lindahl U, Hallén A, Bäckström G (august 1975). "Biosynthesis of heparin. Studies on the microsomal sulfation process". The Journal of Biological Chemistry. 250 (15): 6065–71. doi:10.1016/S0021-9258(19)41159-9. PMID 807579.
- ^ Aikawa J, Grobe K, Tsujimoto M, Esko JD (februar 2001). "Multiple isozymes of heparan sulfate/heparin GlcNAc N-deacetylase/GlcN N-sulfotransferase. Structure and activity of the fourth member, NDST4". The Journal of Biological Chemistry. 276 (8): 5876–82. doi:10.1074/jbc.M009606200. PMID 11087757.
- ^ Toida T, Yoshida H, Toyoda H, Koshiishi I, Imanari T, Hileman RE, et al. (mart 1997). "Structural differences and the presence of unsubstituted amino groups in heparan sulphates from different tissues and species". The Biochemical Journal. 322 ( Pt 2) (Pt 2): 499–506. doi:10.1042/bj3220499. PMC 1218218. PMID 9065769.
- ^ Cadwallader AB, Yost HJ (februar 2007). "Combinatorial expression patterns of heparan sulfate sulfotransferases in zebrafish: III. 2-O-sulfotransferase and C5-epimerases". Developmental Dynamics. 236 (2): 581–6. doi:10.1002/dvdy.21051. PMID 17195182. S2CID 38249813.
- ^ Xu D, Tiwari V, Xia G, Clement C, Shukla D, Liu J (januar 2005). "Characterization of heparan sulphate 3-O-sulphotransferase isoform 6 and its role in assisting the entry of herpes simplex virus type 1". The Biochemical Journal. 385 (Pt 2): 451–9. doi:10.1042/BJ20040908. PMC 1134716. PMID 15303968.
- ^ a b Shukla D, Liu J, Blaiklock P, Shworak NW, Bai X, Esko JD, et al. (oktobar 1999). "A novel role for 3-O-sulfated heparan sulfate in herpes simplex virus 1 entry". Cell. 99 (1): 13–22. doi:10.1016/s0092-8674(00)80058-6. PMID 10520990. S2CID 14139940.
- ^ a b Xia G, Chen J, Tiwari V, Ju W, Li JP, Malmstrom A, et al. (oktobar 2002). "Heparan sulfate 3-O-sulfotransferase isoform 5 generates both an antithrombin-binding site and an entry receptor for herpes simplex virus, type 1". The Journal of Biological Chemistry. 277 (40): 37912–9. doi:10.1074/jbc.m204209200. PMID 12138164.
- ^ a b Xu D, Tiwari V, Xia G, Clement C, Shukla D, Liu J (januar 2005). "Characterization of heparan sulphate 3-O-sulphotransferase isoform 6 and its role in assisting the entry of herpes simplex virus type 1". The Biochemical Journal. 385 (Pt 2): 451–9. doi:10.1042/bj20040908. PMC 1134716. PMID 15303968.
- ^ a b c Lawrence R, Yabe T, Hajmohammadi S, Rhodes J, McNeely M, Liu J, et al. (juli 2007). "The principal neuronal gD-type 3-O-sulfotransferases and their products in central and peripheral nervous system tissues". Matrix Biology. 26 (6): 442–55. doi:10.1016/j.matbio.2007.03.002. PMC 1993827. PMID 17482450.
- ^ Shworak NW, HajMohammadi S, de Agostini AI, Rosenberg RD (2003). "Mice deficient in heparan sulfate 3-O-sulfotransferase-1: normal hemostasis with unexpected perinatal phenotypes". Glycoconjugate Journal. 19 (4–5): 355–61. doi:10.1023/a:1025377206600. PMID 12975616. S2CID 21853086.
- ^ Liu J, Shworak NW, Fritze LM, Edelberg JM, Rosenberg RD (oktobar 1996). "Purification of heparan sulfate D-glucosaminyl 3-O-sulfotransferase". The Journal of Biological Chemistry. 271 (43): 27072–82. doi:10.1074/jbc.271.43.27072. PMID 8900198.
- ^ a b Shworak NW, Liu J, Fritze LM, Schwartz JJ, Zhang L, Logeart D, Rosenberg RD (oktobar 1997). "Molecular cloning and expression of mouse and human cDNAs encoding heparan sulfate D-glucosaminyl 3-O-sulfotransferase". The Journal of Biological Chemistry. 272 (44): 28008–19. doi:10.1074/jbc.272.44.28008. PMID 9346953.
- ^ Shworak NW, Liu J, Petros LM, Zhang L, Kobayashi M, Copeland NG, et al. (februar 1999). "Multiple isoforms of heparan sulfate D-glucosaminyl 3-O-sulfotransferase. Isolation, characterization, and expression of human cdnas and identification of distinct genomic loci". The Journal of Biological Chemistry. 274 (8): 5170–84. doi:10.1074/jbc.274.8.5170. PMID 9988767.
- ^ Chen J, Duncan MB, Carrick K, Pope RM, Liu J (novembar 2003). "Biosynthesis of 3-O-sulfated heparan sulfate: unique substrate specificity of heparan sulfate 3-O-sulfotransferase isoform 5". Glycobiology. 13 (11): 785–94. doi:10.1093/glycob/cwg101. PMID 12907690.
- ^ Duncan MB, Chen J, Krise JP, Liu J (mart 2004). "The biosynthesis of anticoagulant heparan sulfate by the heparan sulfate 3-O-sulfotransferase isoform 5". Biochimica et Biophysica Acta (BBA) - General Subjects. 1671 (1–3): 34–43. doi:10.1016/j.bbagen.2003.12.010. PMID 15026143.
- ^ Chen J, Liu J (septembar 2005). "Characterization of the structure of antithrombin-binding heparan sulfate generated by heparan sulfate 3-O-sulfotransferase 5". Biochimica et Biophysica Acta (BBA) - General Subjects. 1725 (2): 190–200. doi:10.1016/j.bbagen.2005.06.012. PMID 16099108.
- ^ Girardin EP, Hajmohammadi S, Birmele B, Helisch A, Shworak NW, de Agostini AI (novembar 2005). "Synthesis of anticoagulantly active heparan sulfate proteoglycans by glomerular epithelial cells involves multiple 3-O-sulfotransferase isoforms and a limiting precursor pool". The Journal of Biological Chemistry. 280 (45): 38059–70. doi:10.1074/jbc.m507997200. PMID 16107334.
- ^ Ori A, Wilkinson MC, Fernig DG (maj 2008). "The heparanome and regulation of cell function: structures, functions and challenges". Frontiers in Bioscience. 13 (13): 4309–38. doi:10.2741/3007. PMID 18508513.
- ^ Kim H, Ho M (novembar 2018). "Isolation of Antibodies to Heparan Sulfate on Glypicans by Phage Display". Current Protocols in Protein Science. 94 (1): e66. doi:10.1002/cpps.66. PMC 6205898. PMID 30091851.
- ^ Geoghegan EM, Pastrana DV, Schowalter RM, Ray U, Gao W, Ho M, et al. (oktobar 2017). "Infectious Entry and Neutralization of Pathogenic JC Polyomaviruses". Cell Reports. 21 (5): 1169–1179. doi:10.1016/j.celrep.2017.10.027. PMC 5687836. PMID 29091757.
- ^ Sadir R, Forest E, Lortat-Jacob H (maj 1998). "The heparan sulfate binding sequence of interferon-gamma increased the on rate of the interferon-gamma-interferon-gamma receptor complex formation". The Journal of Biological Chemistry. 273 (18): 10919–25. doi:10.1074/jbc.273.18.10919. PMID 9556569.
- ^ Tong M, Tuk B, Hekking IM, Vermeij M, Barritault D, van Neck JW (2009). "Stimulated neovascularization, inflammation resolution and collagen maturation in healing rat cutaneous wounds by a heparan sulfate glycosaminoglycan mimetic, OTR4120". Wound Repair and Regeneration. 17 (6): 840–52. doi:10.1111/j.1524-475X.2009.00548.x. PMID 19903305. S2CID 17262546.
- ^ Tong M, Tuk B, Hekking IM, Pleumeekers MM, Boldewijn MB, Hovius SE, van Neck JW (2011). "Heparan sulfate glycosaminoglycan mimetic improves pressure ulcer healing in a rat model of cutaneous ischemia-reperfusion injury". Wound Repair and Regeneration. 19 (4): 505–14. doi:10.1111/j.1524-475X.2011.00704.x. PMID 21649786. S2CID 7380997.