Aeromonas hydrophila
 | |
| Dades | |
|---|---|
| Tinció de Gram | gramnegatiu |
| Taxonomia | |
| Regne | Pseudomonadati |
| Fílum | Pseudomonadota |
| Classe | Gammaproteobacteria |
| Ordre | Aeromonadales |
| Família | Aeromonadaceae |
| Gènere | Aeromonas |
| Espècie | Aeromonas hydrophila * (Chester, 1901)
|
| Nomenclatura | |
| Sinònims |
|
Aeromonas hydrophila és una de les 27 espècies que formen part del gènere Aeromonas.[1] Es tracta d'un bacil eubacteri heteròtrof gramnegatiu mesòfil i es considera un patogen emergent responsable de diverses infeccions en humans, inclús pot ser patogen d’animals aquàtics, concretament en peixos.[2] Està àmpliament distribuït en ambients aquàtics,[3] com en aigües residuals o aigua potable.
Característiques
[modifica]Aeromonas hydrophila és un bacil patogen aquàtic gramnegatiu, oxidasa positiu, anaerobi facultatiu, oportunista i mesòfil, ja que creix a una temperatura de 35-37 °C, però s'ha observat que pot créixer en un marge ampli de temperatures i condicions ambientals.[4] Aeromonas hydrophila produeix factors de virulència, com ara hemolisines, adhesines, enterotoxines o fosfolipases.[5] Aquests bacteris son mòtils degut a un flagel polar. No formen estructures de resistència, per tant, no formen espores.[6] Pot créixer òptimament en pH d'entre 5,5 i 9.
Pot ser un colonitzador habitual del tracte gastrointestinal dels humans, causant malalties infeccioses. Els patògens son capaços d’expressar flagels laterals que els permet moure’s en ambients viscosos. Aquests flagels no només son útils pel moviment, sinó que també poden contribuir a la formació de biofilms.[7]
Aeromonas hydrophila també s'ha relacionat amb la mort de peixos d'arreu del món, provocant enormes pèrdues econòmiques.[4]
Aïllament
[modifica]Aeromonas hydrophila pot créixer al laboratori en molts medis de cultiu, ja que pot créixer en una àmplia gamma de medis de cultiu, inclosos medis selectius per a l'aïllament de bacteris entèrics. Normalment s’utilitza el medi cefsulodina-triclosan-novobiocina (CIN), un medi on poden créixer tan Yersinia enterocolitica com diverses espècies d'Aeromonas. També es pot cultivar sobre medis d'agar sang i és útil per distingir les espècies d'Aeromonas d’altres microorganismes que creixen en el medi, ja que es pot ferla prova de la citocrom oxidasa a partir del cultiu. En aquest medi de cultiu es podrà apreciar la capacitat hemolítica del bacteri, ja que es podrà observar una β-hemòlisi, és a dir, la capacitat de ruptura dels eritròcits, una característica distintiva útil, però no exclusiva.[8]
En els cultius, Aeromonas hydrophila es pot confondre amb espècies del gènere Vibrio. Es poden distingir per la capacitat de créixer en medis amb una alta o molt baixa concentració de sals: A hydrophila mai creix en condicions molt salines, però sí que ho pot fer en concentracions molt baixes de sal, entre un 0% i 4% de clorur de sodi (NaCl).[8]
Patogènesi
[modifica]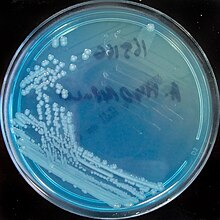
Aeromonas hydrophila és considerat un patogen primari i oportunista d’animals aquàtics i terrestres, incloent-hi humans. Té un rang molt ampli d'hostes com poden ser amfibis, ocells, peixos, rèptils o mamífers.[9] Aquesta espècie és un important agent causant de malalties en peixos d’aigua dolça i ambients càlids, provocant una septicèmia hemorràgica similar a la que causen altres bacteris gramnegatius i causant una significativa pèrdua econòmica. En humans, la manifestació clínica de la infecció per aquest patogen va des de gastroenteritis fins a infeccions extraintestinals com ara infeccions de la pell, meningitis o septicèmia. Malgrat l'augment de la recerca, el coneixement que hi ha sobre el mecanisme emprat per A. hydrophila en el desenvolupament de la septicèmia encara és limitat. Per causar septicèmia, els bacteris han d’evadir la resposta immunitària innata i mantenir un cert nivell de bacterièmia.[10][3]
S’ha suggerit que hi ha molts productes extracel·lulars que contribueixen a la patogènesi, com ara β-hemolisines, aerolisines, lipases extracel·lulars, enterotoxines citolítiques, toxines hemolítiques, proteases extracel·lulars o adhesines. La majoria d’hemolisines produïdes per aquest bacteri estan relacionades amb l'aerolisina i l'hemolisina HlyA-like de Vibrio cholerae. S’ha hipotetitzat que totes les toxines son similars en estructura molecular a l'aerolisina.[10][3]
Factors de patogenicitat
[modifica]Els brots d'Aeromonas hydrophila es donen quan hi ha canvis de susceptibilitat per part dels hostes degut a canvis en el medi extern. Els factors de patogenicitat produïts són principalment citotoxines i hemolisines.
El microorganisme creix òptimament a temperatures de 28 °C, fet que s’ha observat en aïllats ambientals, mentre que en aïllats clínics creix a temperatures òptimes més elevades, i que a partir de 37 °C comença a produir factors de virulència. La producció de factors de patogenicitat també està regulada per la percepció de quòrum, que també influeix en la densitat cel·lular. S'ha observat que molts factors de virulència venen codificats en el propi cromosoma del bacteri, però hi pot haver factors de virulència codificats en plasmidis i transposons que poden ser un problema pel fet que aquests poden ser transmesos a altres microorganismes que no els tinguin.[5]
La patogènesi de A. hydrophila és complexa i multifactorial, implicant antígens-O, càpsules, lipopolisacàrids, capa S, flagels i el sistema d'unió del ferro, incloent tots els productes extracel·lulars. Els seus flagels també actuen com a factors de patogenicitat. Hi ha una expressió constitutiva del flagel polar, anomenat Pof, que permet a les cèl·lules nedar en ambients aquàtics o líquids. També pot contribuir en la fixació inicial a l'epiteli gastrointestinal. Alhora, s'activarà l'expressió d'un flagel lateral, anomenat Laf, que actua com a superfície de contacte i generador de viscositat; d'aquesta manera permet el moviment d'eixamenament (swarming en anglès) en superfícies sòlides. Paral·lelament, pot augmentar l'adhesió de la cèl·lula, la formació de biofilms i la colonització a llarg termini.[4]
També s’ha parlat d'una regulació dels factors de patogenicitat mitjançant conversió lisogènica, tot i així no hi ha informació empírica per corroborar aquest fet.[11]
Sistemes de secreció
[modifica]- El sistema de secreció de tipus II està molt conservat i es troba en tots els membres coneguts d’A. hydrophila i és el que secreta el factor de patogenicitat més potent de tots, l'enterotoxina citotòxica aerolisina (en anglès s'anomena aerolysin-related citotoxic enterotoxin). A més d’aquesta toxina, el microorganisme secreta altres factors de patogenicitat com altres aerolisines, amilases, DNAses i proteases.[11]
- El sistema de secreció de tipus III es troba principalment en aïllats clínics, actua com una agulla que injecta els factors de patogenicitat en l'hoste, és un factor de virulència molt important en diferents espècies de Aeromonas spp, per tant es pot utilitzar com a vacuna desactivant una de les subunitats del sistema.[11]
- El sistema de secreció de tipus VI actua com la cua d’un bacteriòfag i permet la injecció dels factors de patogenicitat en la cèl·lula hoste, està format per proteïnes tipus VrgG i Hcp que actuen com a proteïnes estructurals o com a antimicrobianes formadores de porus un cop han estat secretades.[11]
Patogènesi en humans
[modifica]Gastroenteritis
[modifica]L'enteritis associada a Aeromonas és un fenomen estès per tot el món i que afecta persones de qualsevol edat. S’observa principalment en persones sanes, encara que també es pot donar en aquelles que pateixen algun tipus de trastorn immunitari, com els pacients de VIH.[4]
És una malaltia lleu i autolimitada. Es pot presentar de cinc diferents formes: enteritis no significativa, enteritis més greu acompanyada de sang a la femta, com una síndrome intestinal crònica o subaguda, com una malaltia semblant al còlera o en associació la diarrea del viatger. La més comuna és la no significativa, en la qual es produeix una diarrea líquida.[4]
Poden causar episodis de gastroenteritis: la ruta d’infecció és via oral, és a dir, per ingestió d'aliments o aigua contaminats. Un cop ha entrat en l'organisme, haurà de fer front a l'ambient àcid de l'estómac i ha de trobar el lloc adient per començar a créixer. També haurà de lluitar contra els microorganismes autòctons (microbiota intestinal). Hi ha d’haver molts gens i factors de virulència implicats en la supervivència d'Aeromonas; no obstant, només se n’han estudiat uns quants.[4]
L'esquema d’infecció pot ser el següent: hi ha una locomoció dirigida per arribar al lloc idoni on proliferarà. A continuació, el patogen es fixa a l'epiteli gastrointestinal i forma un biofilm, d’aquesta forma colonitza la zona. Finalment s’elaboren els factors de virulència, culminant en la infecció. En tot aquest procés intervenen diversos factors de patogenicitat, entre els quals els flagels polars i els flagels laterals.[4]
Una via potencial per la qual Aeromonas pot resistir el pH tan baix és una resposta àcid-tolerant similar a la que tenen alguns patògens entèrics com Salmonella enterica i Escherichia coli.
Per competir amb la microbiota local del tracte gastrointestinal elabora uns subproductes, resultat del metabolisme i uns compostos semblants a la bacteriocina.[4] Un cop s’ha establert en el tracte gastrointestinal, pot causar diarrea mitjançant l'elaboració de molècules enterotoxigèniques, o bé, a través de la invasió de l'epiteli, causant disenteria o colitis. La toxina millor caracteritzada probablement és la β-hemolisina, també anomenada aerolisina de Bernheimer, la qual és formadora de porus i es troba en més del 75 per cent de les espècies d'A. hydrophila.[4]
Hi pot haver diverses complicacions de les enteritis causades per A. hydrophila com ara episodis greus de colitis o disenteria. A partir de la colitis es poden desenvolupar afeccions cròniques com colitis ulcerosa o pancolitis, les quals en alguns casos requereixen d'una resecció quirúrgica a més dels antiinflamatoris per afavorir la recuperació total. Un cas fulminant és el de gastroenteritis necrotitzant segmentària, que està associada amb danys tissulars greus, septicèmia i disfunció multiorgànica. Malgrat això, la complicació més greu és la de la síndrome hemolíticourèmica.[4]
Infeccions cutànies
[modifica]També causa infeccions a la pell que fàcilment poden portar al xoc sèptic o a la mort, la infecció comença quan l’hoste entra en contacte amb aigua infectada, la presència de traumatismes a la pell facilita l'entrada del microorganisme, la infecció té tendència a ser polimicrobiana. Les infeccions per aquest microorganisme solen donar-se després de tsunamis o inundacions.[12]
La infecció és més comuna en homes, amb una relació de 3:1 i la malaltia es manifesta inicialment com una cel·lulitis que forma abcessos, posteriorment es dona l'aparició d’ampolles. La infecció es pot complicar i donar mionecrosi, cel·lulitis crepitant i ectima gangrenós. Aquests quadres clínics desemboquen en sèpsia, xoc tòxic, pèrdua de l'extremitat o la mort.[12]
L'anomenada aerolisina causa danys tissulars. La infecció només es dona quan un d’aquests productors de toxines entra per una ferida de la pell. Les ferides cutànies, cel·lulitis i altres símptomes poden anar acompanyats de febre, edema o eritema, el quadre simptomatològic varia segons l'eficiència del sistema immune de l’infectat.[12]
Septicèmia
[modifica]La malaltia invasiva per excel·lència associada a Aeromonas hydrophila és la septicèmia. Es pot classificar segons quatre aspectes: basant-se en la població afectada, a partir dels factors de risc; pels esdeveniments que han provocat la malaltia, i pels modes d'adquisició.[4] La majoria de casos de septicèmia per A. hydrophila es donen en persones que es troben greument immunocompromeses. Els casos en individus sans son inusuals i solen estar associats a traumatismes. Si s'exclouen els traumatismes, la majoria de casos d'aquesta malaltia en persones sanes es dona en la població de la tercera edat.[13] Les persones immunocompromeses que tenen major risc de patir septicèmia són les que pateixen trastorns mieloproliferatius o malalties hepàtiques cròniques.[4]
Els símptomes més comuns inclouen febre, icterícia, dolor abdominal, xoc sèptic i dispnea. La diarrea pot ocórrer en un petit percentatge de casos.[4]
Quan es produeix una septicèmia polimicrobiana, A. hydrophila normalment va acompanyada d'Escherichia coli, Klebsiella pneumoniae i Staphylococcus aureus.[4]
D'altres
[modifica]S'ha observat que Aeromonas hydrophila també és causant de les següents infeccions i malalties:
Infeccions intraabdominals
[modifica]El terme «infecció intraabdominal» normalment és sinònim de peritonitis. En realitat, però, aquestes infeccions comprenen també pancreatitis, colangitis aguda i abscessos hepàtics així com peritonitis. La freqüència de peritonitis associada a Aeromonas és molt major en el sud-est d'Àsia que la que s’observa en els Estats Units i Europa. Normalment es donen en homes de mitjana edat que pateixen altres malalties o complicacions.[4]
La peritonitis és la inflamació del peritoneu, la membrana serosa de la cavitat abdominal. Es pot trobar de tres formes: peritonitis bacteriana espontània, extensió directa de l'intestí (perforació intestinal) i diàlisi peritoneal ambulatòria crònica.
També es poden classificar segons si son primàries o secundàries. La forma més estranya és la peritonitis primària, que resulta de la disseminació de la infecció des de la sang o la limfa fins al peritoneu, mentre que la peritonitis secundària es dona per la disseminació d'una infecció provinent del tracte gastrointestinal. En el cas de peritonitis bacteriana espontània, A. hydrophila és el tercer gramnegatiu més freqüent que es troba en Korea i Taiwan. Aeromonas hydrophila és el patogen més freqüent associat a peritonitis en el sud-est d'Àsia.[4]
La peritonitis primària es dona en persones amb malalties al fetge i normalment van acompanyades amb una bacterièmia en el 50 per cent dels casos. Les peritonitis secundàries es donen en persones amb malalties associades a cuidats personals, les peritonitis secundàries normalment són polimicrobianes, es veu la presència d’altres bacils gramnegatius com ara Escherichia coli o Klebsiella pneumoniae. En contraposició, la peritonitis primària és monomicrobiana i més perillosa que la secundària, amb un 23 per cent de mortalitat, mentre que la secundària causa un 15 per cent de mortalitat.[4]
Infeccions dels sistemes hepatobiliars i pancreàtics
[modifica]La colangitis supurant aguda és una de les complicacions mèdiques més comuna associada a les malalties hepatobiliars causades per Aeromonas hydrophila, normalment és una infecció mixta associada a enterobacteris, enterococs o Pseudomonas aeruginosa, la presència d’aquests microorganismes dona a entendre que l’origen d’aquesta malaltia és gastrointestinal.[4]
Els pacients que pateixen aquesta malaltia presenten un quadre simptomatològic similar: colangiocarcinoma, carcinoma pancreàtic i estenosi biliar no maligna. Els trasplantaments de fetge actuen com a factor de predisposició a patir aquesta malaltia. Altres factors com ara intervencions quirúrgiques o immunodepressió faciliten que es doni aquesta malaltia.[4]
Infeccions del tracte respiratori
[modifica]La pneumònia causada per A. hydrohila es diagnostica fent cultius d'esput purulent de pacients amb pneumònia. La infecció respiratòria per A. hydrophila s’investiga quan a l'esput no es detecta la presència de cap microorganisme comú causant de pneumònia. Un cop ha crescut la colònia es poden fer diverses proves bioquímiques per corroborar la presència del microorganisme. La simptomatologia consisteix en febre, refredat, tos, dolor pectoral i dispnea, no hi ha cap símptoma que sigui diferent dels causats pels microorganismes causants de pneumònia més comuns.
Les proves que es realitzen per corroborar la presència d’aquest microorganisme són la tinció de gram, on observaríem una tinció pròpia d'un gramnegatiu i la prova de l'oxidasa, que és positiva. Tot i això, després de fer el cultiu del bacteri s’ha de fer una rèplica en cultiu amb sang, s’utilitza com a mètode de comprovació.[14]
La pneumònia causada per A. hydrophila és una malaltia molt poc freqüent, només en el 8% de les persones ingressades amb pneumònia trobem que aquesta ha estat causada per A. hydrophila. També s’ha de dir que tenint en compte que A. hydrophila és un patogen oportunista aquesta malaltia es sol donar a països del sud-est asiàtic i a persones amb més de 60 anys.[15]
Infeccions de l'ull
[modifica]A. hydrophila pot provocar des d'endoftalamitis fins queratitis i ulceració corneal. Normalment s'entra en contacte amb el patogen a través de les lents de contacte o lentilles.
Diagnòstic
[modifica]Es busca aquest microorganisme quan es troba un pacient amb infeccions a la pell que ha estat en contacte amb aigua que podria estar contaminada amb aquest patogen. També es pot buscar aquest microorganisme en cas que el pacient mostri mossegades d’amfibis, rèptils o peixos.
Es prenen mostres de l'exsudat de les ferides i s’envien al laboratori per fer-les créixer en els medis esmentats anteriorment. És important fer un antibiograma, ja que aquest microorganisme sol afectar persones immunodeprimides i necessitem trobar els antibiòtics més eficients per eliminar-la de l’organisme.
Es poden realitzar proves bioquímiques, donat que A. hydrophila és capaç de descarboxilar la lisina, utilitzar àcid urocànic i DL-lactat. També pot fermentar L-arabinosa, D-ramnosa, lactosa, sacarosa, mannitol, D-sorbitol i glucosa produint gas. Es podria realitzar la prova d'hidròlisi de l'esculina i l'arbutina, així com la producció d'elastasa. D'aquesta forma s'aconsegueix diferenciar A. hydrophila d'altres espècies d'Aeromonas.[4]
També es pot fer una identificació molecular. La tècnica més usada és la detecció i seqüenciació del gen de l'RNA ribosòmic 16S, no obstant no és gaire eficaç donat el gran mosaic evolutiu d'Aeromonas, conseqüència dels polimorfismes de nucleòtids que s'han detectat en els operons rrn que codifiquen aquests gens.[4]
Resistències als antibiòtics i tractament
[modifica]Tant l'aparició de resistències als antibiòtics així com el seu origen en el medi ambient són rellevants per a la salut humana per la creixent importància de les malalties transmeses per zoonosi i per la necessitat de saber les resistències d’organismes patògens emergents.[16] L'increment de les resistències a antibiòtics per part d'A. hydrophila comença a ser una preocupació per la salut pública.[5] Les Aeromonas tenen la característica de ser resistents a tota la família de penicil·lines i a l'ampicil·lina, entre d'altres.[16] A més a més, A.hydrophila sol sintetitzar una β-lactamasa, això fa que el tractament emprat no sigui el mateix que s’utilitza en altres espècies del mateix gènere. En aquest cas s’utilitza un tractament amb aminoglicòsids i cefalosporines de segona i tercera generació. Els patrons de sensibilitat als antibiòtics són útils com a característiques fenotípiques per a la identificació d’espècies d'Aeromonas, especialment per als aïllats clínics.[16]
Quan es donen quadres simptomatològics greus, com una mionecrosi, que poden evolucionar ràpidament a xoc sèptic, el microorganisme mostra una resistència, degut a les β-lactamases, als antibiòtics utilitzats en casos d’urgència. Per tant per aquests casos s’utilitzen antibiòtics com tetraciclines i aztreonam.
Normalment el tractament amb antibiòtic ve acompanyat amb tractament quirúrgic, drenant els abscessos i retirant el teixit necrosat, sobretot en Aeromonas hydrophila que sol causar fasciïtis necrosant.[12]
No obstant, en els casos de gastroenteritis, son infeccions autolimitades, és a dir, que el propi hostatger les pot resoldre sense la necessitat d'antibiòtics. Només s'administren antibiòtics en persones immunodeprimides o amb un quadre de gastroenteritis molt severa.[16]
Resposta del sistema immunitari
[modifica]S'ha observat que els neutròfils, mastòcits, eosinòfils i macròfags son capaços d'excretar una mena de trampes extracel·lulars (ET), les quals consisteixen en un esquelet d'àcid desoxiribonucleic estabilitzat amb histones, pèptids antimicrobians i proteases. La seva funció principal és bloquejar i matar el patogen en el lloc d'infecció, limitant així la seva disseminació en l'organisme infectat. No obstant, A. hydrophila és capaç de sintetitzar nucleases que degraden l'esquelet de DNA i acaben amb els ETs, d'aquesta forma es pot escapar i pot propagar-se pel cos de l'hoste.[2][3]
D'altra banda s'ha demostrat que l'addició de β-glucans a través de l'aliment, els quals se sap que estimulen el sistema immunitari, afavoreix la resistència dels ETs front les nucleases sintetitzades per A. hydrophila en peixos.[17]
Aeromonas hydrophila en els aliments
[modifica]A. hydrophila es troba en un rang ampli d’aliments predominant en els vegetals, productes carnis, llet, peixos i marisc. En aliments pasteuritzats es redueix la seva incidència però encara hi son presents. No obstant, el major reservori d’A. hydrophila és l'aigua. Degut a la seva capacitat de colonitzar aliments, si s'ingereixen productes contaminats amb aquest patogen, es poden donar infeccions en el tracte gastrointestinal.[18]
La resistència a la calor d’A. hydrophila és baixa, de manera que es pot eliminar fàcilment en aliments que requereixen cocció. També és susceptible a desinfectants com el clor, que es pot utilitzar pel tractament d’aigües. Tot i això, es pot trobar el microorganisme un cop tractada l'aigua, això pot ser conseqüència d'una alta concentració de microorganismes o de matèria orgànica que inactivarien el clor.[18]
Prevenció
[modifica]Prevenció en la indústria alimentària
[modifica]La prevenció de la propagació de soques d'Aeromonas implicades en brots de gastroenteritis depèn d’assegurar mesures sanitàries adients com la preparació adequada dels aliments, una bona higiene per part dels manipuladors dels productes i un sistema eficient d’eliminació d’aigües residuals. És imprescindible una vigilància adequada de les instal·lacions d’aigua, menjar i sanejament, mitjançant procediments de diagnòstic i detecció de salut pública per protegir els individus, inclosos els nadons, contra la diarrea causada per aquest patogen.[16]
Una altra de les mesures de prevenció és la cocció dels aliments, però no sempre és eficaç, ja que hi ha productes que no s’han de cuinar prèviament, de la mateixa manera que la ingesta d’aigua, per tant no es pot garantir que no hi hagi cap risc d’infecció.[16]
Prevenció en l'aqüicultura
[modifica]L'ús d’antibiòtics en aqüicultura com a mètode profilàctic té un paper important en l'aparició de soques multiresistents, ja que s’han trobat espècies com A. hydrophila, entre d'altres, aïllades dels peixos amb resistències a molts antibiòtics. A més, aquest ús excessiu deixa residus d’antibiòtics inacceptables en productes de l'aqüicultura i l'ambient, sobretot a les aigües.[16][5]
En l'aqüicultura, la prevenció de contaminacions consisteix en l'eliminació d’animals malalts i el tractament d’aigües per controlar la densitat d’Aeromonas en els sistemes d’aqüicultura. El manteniment d’alts estàndards de qualitat de l'aigua, control de la temperatura, desinfecció d’equips i reducció d’estrès poden reduir la prevalença de la malaltia. En l'aqüicultura la qualitat de l'aigua té molta importància en la prevenció de la contaminació.[16]
La presència de soques d'Aeromonas potencialment patògens i resistents a diversos medicaments a les aigües superficials continua sent una afectació important per a la salut. El control continu de les aigües superficials és vital per identificar possibles patògens que es puguin transmetre per l'aigua i així poder reduir els riscos per a la salut.[16]
Referències
[modifica]- ↑ «ITIS Standard Report Page: Aeromonas».
- ↑ 2,0 2,1 Citterio, Barbara; Biavasco, Francesca «Aeromonas hydrophila virulence». Virulence, 6, 5, 09-06-2015, pàg. 417–418. DOI: 10.1080/21505594.2015.1058479. ISSN: 2150-5594. PMC: 4601520. PMID: 26055576.
- ↑ 3,0 3,1 3,2 3,3 Ji, Yachan; Li, Jinquan; Qin, Zhendong; Li, Aihua; Gu, Zemao «Contribution of nuclease to the pathogenesis of Aeromonas hydrophila». Virulence, 6, 5, 24-06-2015, pàg. 515–522. DOI: 10.1080/21505594.2015.1049806. ISSN: 2150-5594.
- ↑ 4,00 4,01 4,02 4,03 4,04 4,05 4,06 4,07 4,08 4,09 4,10 4,11 4,12 4,13 4,14 4,15 4,16 4,17 4,18 4,19 4,20 Janda, J. M.; Abbott, S. L. «The Genus Aeromonas: Taxonomy, Pathogenicity, and Infection». Clinical Microbiology Reviews, 23, 1, 01-01-2010, pàg. 35–73. DOI: 10.1128/cmr.00039-09. ISSN: 0893-8512.
- ↑ 5,0 5,1 5,2 5,3 Stratev, Deyan; Odeyemi, Olumide A. «Antimicrobial resistance of Aeromonas hydrophila isolated from different food sources: A mini-review». Journal of Infection and Public Health, 9, 5, 9-2016, pàg. 535–544. DOI: 10.1016/j.jiph.2015.10.006. ISSN: 1876-0341.
- ↑ Vara-Brenes, Daniel; Santiago-Cuñer, Antares; Mateos-Rodríguez, José María; Fernández-Bermejo, Miguel; Molina-Infante, Javier «Colitis por Aeromonas hydrophila como primera manifestación de un cáncer de colon». Gastroenterología y Hepatología, 37, 4, 4-2014, pàg. 270–272. DOI: 10.1016/j.gastrohep.2013.09.003. ISSN: 0210-5705.
- ↑ Merino, Susana; Fulton, Kelly M.; Twine, Susan M.; Wilhelms, Markus; Molero, Raquel «Aeromonas hydrophila Flagella Glycosylation: Involvement of a Lipid Carrier». PLoS ONE, 9, 2, 21-02-2014, pàg. e89630. DOI: 10.1371/journal.pone.0089630. ISSN: 1932-6203.
- ↑ 8,0 8,1 «Aeromonas - an overview | ScienceDirect Topics». [Consulta: 18 novembre 2019].
- ↑ Rasmussen-Ivey, Cody R.; Hossain, Mohammad J.; Odom, Sara E.; Terhune, Jeffery S.; Hemstreet, William G. «Classification of a Hypervirulent Aeromonas hydrophila Pathotype Responsible for Epidemic Outbreaks in Warm-Water Fishes». Frontiers in Microbiology, 7, 18-10-2016. DOI: 10.3389/fmicb.2016.01615. ISSN: 1664-302X. PMC: PMC5067525. PMID: 27803692.
- ↑ 10,0 10,1 Chu, W-H; Lu, C-P «Multiplex PCR assay for the detection of pathogenic Aeromonas hydrophila» (en anglès). Journal of Fish Diseases, 28, 7, 7-2005, pàg. 437–441. DOI: 10.1111/j.1365-2761.2005.00628.x.
- ↑ 11,0 11,1 11,2 11,3 Rasmussen-Ivey, Cody R.; Figueras, Maria J.; McGarey, Donald; Liles, Mark R. «Virulence Factors of Aeromonas hydrophila: In the Wake of Reclassification». Frontiers in Microbiology, 7, 25-08-2016. DOI: 10.3389/fmicb.2016.01337. ISSN: 1664-302X. PMC: 4997093. PMID: 27610107.
- ↑ 12,0 12,1 12,2 12,3 Aguilar-García, César Raúl «Infección de piel y tejidos blandos por el género Aeromonas». Med Int Méx, 22-09-2015, pàg. 701-708.
- ↑ Grantham, Mica; Naab, Tammey «Aeromonas hydrophila Septicemia in a Healthy Male» (en anglès). American Journal of Clinical Pathology, 142, suppl_1, 01-10-2014, pàg. A167–A167. DOI: 10.1093/ajcp/142.suppl1.167. ISSN: 0002-9173.
- ↑ G. Castro Escarpulli M.G. Aguilera Arreola C.H. Hernández Rodríguez R.I. Arteaga Garibay A.A. Carmona Martínez A. Pérez Valdespino S. Giono Cerezo M.J. Figueras Salvat G. Aparicio Ozores. La identificación genética de Aeromonas, una realidad y una necesidad para la microbiología diagnóstica.. Asociación Mexicana de Bioquímica Clínica, 2006-04-26.
- ↑ Chao, C. M.; Lai, C. C.; Tsai, H. Y.; Wu, C. J.; Tang, H. J. «Pneumonia caused by Aeromonas species in Taiwan, 2004–2011» (en anglès). European Journal of Clinical Microbiology & Infectious Diseases, 32, 8, 8-2013, pàg. 1069–1075. DOI: 10.1007/s10096-013-1852-6. ISSN: 0934-9723.
- ↑ 16,0 16,1 16,2 16,3 16,4 16,5 16,6 16,7 16,8 Igbinosa, Isoken H.; Igumbor, Ehimario U.; Aghdasi, Farhad; Tom, Mvuyo; Okoh, Anthony I. «Emerging Aeromonas Species Infections and Their Significance in Public Health». The Scientific World Journal, 2012, 04-06-2012. DOI: 10.1100/2012/625023. ISSN: 2356-6140. PMC: 3373137. PMID: 22701365.
- ↑ Brogden, Graham; von Köckritz-Blickwede, Maren; Adamek, Mikołaj; Reuner, Friederike; Jung-Schroers, Verena «β-Glucan protects neutrophil extracellular traps against degradation by Aeromonas hydrophila in carp (Cyprinus carpio)» (en anglès). Fish & Shellfish Immunology, 33, 4, 10-2012, pàg. 1060–1064. DOI: 10.1016/j.fsi.2012.08.009.
- ↑ 18,0 18,1 Doyle, Michael P., 1949- editor. Diez-Gonzalez, Francisco, 1961- editor. Hill, Colin, PhD, editor.. Food microbiology : fundamentals and frontiers. ISBN 9781555819972.