Cianocobalamina
| Cianocobalamina | ||
|---|---|---|
 | ||
 | ||
| Nombre (IUPAC) sistemático | ||
| Cobalto(3+);[(2R,3S,4R,5S)-5-(5,6-dimetilbenzimidazol-1-il)-4-hidroxi-2-(hidroximetil)oxolán-3-il] [(2R)-1-[3-[(1R,2R,3R,5Z,7S,10Z,12S,13S,15Z,17S,18S,19R)-2,13,18-tris(2-amino-2-oxoetil)-7,12,17-tris(3-amino-3-oxopropil)-3,5,8,8,13,15,18,19-octametil-2,7,12,17-tetrahidro-1H-corrina-24-id-3-il]propanoilamino]propano-2-il] fosfato;cianuro | ||
| Identificadores | ||
| Número CAS | 68-19-9 | |
| Código ATC | B03BA01 V09XX01 V09XX02 | |
| PubChem | 16212801 | |
| DrugBank | DB00115 | |
| ChemSpider | 10469504 | |
| UNII | P6YC3EG204 | |
| Datos químicos | ||
| Fórmula | C63H88CoN14O14P | |
| Peso mol. | 1355,365177 g/mol | |
|
CC1=CC2=C(C=C1C)N(C=N2)C3C(C(C(O3)CO)OP(=O)([O-])OC(C)CNC(=O)CCC4(C(C5C6(C(C(C(=C(C7=NC(=CC8=NC(=C(C4=N5)C)C(C8(C)C)CCC(=O)N)C(C7(C)CC(=O)N)CCC(=O)N)C)[N-]6)CCC(=O)N)(C)CC(=O)N)C)CC(=O)N)C)O.[C-]#N.[Co+3]
| ||
|
InChI=1S/C62H90N13O14P.CN.Co/c1-29-20-39-40(21-30(29)2)75(28-70-39)57-52(84)53(41(27-76)87-57)89-90(85,86)88-31(3)26-69-49(83)18-19-59(8)37(22-46(66)80)56-62(11)61(10,25-48(68)82)36(14-17-45(65)79)51(74-62)33(5)55-60(9,24-47(67)81)34(12-15-43(63)77)38(71-55)23-42-58(6,7)35(13-16-44(64)78)50(72-42)32(4)54(59)73-56;1-2;/h20-21,23,28,31,34-37,41,52-53,56-57,76,84H,12-19,22,24-27H2,1-11H3,(H15,63,64,65,66,67,68,69,71,72,73,74,77,78,79,80,81,82,83,85,86);;/q;-1;+3/p-2/t31-,34-,35-,36-,37+,41-,52-,53-,56-,57?,59-,60+,61+,62+;;/m1../s1
Key: FDJOLVPMNUYSCM-QJRSUKKJSA-L | ||
| Sinónimos | Cobalamina, vitamina B12 | |
| Datos físicos | ||
| P. de fusión | -273 °C (-459 °F) | |
| P. de ebullición | 300 °C (572 °F) | |
| Solubilidad en agua | 3.84e-02 g/l mg/mL (20 °C) | |
| Rot. esp. | -59 o -9 °C NM (Diluidos en una solución acuosa) | |
| Farmacocinética | ||
| Biodisponibilidad | Absorbido fácilmente en la porción distal del íleon. | |
| Unión proteica | Muy alta, mediante transcobalaminas | |
| Metabolismo | Hepático | |
| Vida media | Unos 6 días; 400 días en el hígado | |
| Excreción | Heces fecales, renal | |
| Datos clínicos | ||
| Vías de adm. | Oral, intravenosa. | |
La cianocobalamina es la forma más común y ampliamente producida de los compuestos químicos que tienen actividad de vitamina B12. Vitamina B12 es el descriptor genérico para cualquiera de tales vitámeros de la B12. Ya que el cuerpo puede convertir la cianocobalamina en cualquier compuesto de vitamina B12 activa, hace de la cianocobalamina, por definición, un vitámero de B12, aunque es en gran parte artificial.
Este compuesto no es producido por los animales, pero estos pueden convertir este producto artificial en uno de los cofactores activos de la vitamina B12, tales como la metilcobalamina.[1] Durante su metabolización queda atrás una pequeñísima cantidad de cianuro.
Terminología
[editar]El nombre vitamina B12 y el alternativo cobalamina, por lo general hacen referencia a todas las formas de esta vitamina. Algunos médicos han sugerido que pueden ser divididos en dos categorías para su uso.
- En un sentido amplio, B12 se refiere a un grupo de vitámeros compuestos de cobalto conocidos como cobalaminas, los cuales son: la cianocobalamina, que es un producto artificial formado a partir del carbón activado.
- El término B12 puede ser utilizado correctamente para referirse a la cianocobalamina, la forma principal de B12, utilizada en los alimentos y en suplementos nutricionales. Generalmente esto no crea ningún problema, excepto tal vez, en casos poco frecuentes, daño en los nervios ópticos debido a los altos niveles de cianuro en la sangre ocasionados por el consumo de cigarrillos. Para evitar esto último se requiere dejar de fumar o suministrar otra forma de B12 para disminuir los problemas oculares. Sin embargo, la ambliopía generada por el tabaquismo es una enfermedad poco frecuente y aún no está claro si es síntoma de una particular hipovitaminosis B12 que es resistente al tratamiento con cianocobalamina.
Historia
[editar]La síntesis artificial total de la B12 fue reportada por Robert Burns Woodward[2] y Albert Eschenmoser en 1972,[3] y sigue siendo una de las hazañas clásicas de la síntesis orgánica. Se sabe que las especies de los siguientes géneros son conocidas por sintetizar la vitamina B12: acetobacterium, enterobacter, agrobacterium, alicaligenes, azotobacter, bacillus, clostridium, corynebacterium, flavobacterium, lactobacillus, micromonospora, mycobacterium, nocardia, propionibacterium, protaminobacter, proteus, pseudomonas, rhizobium, salmonella, serratia, streptomyces, streptococcus y xanthomonas.
Estructura
[editar]
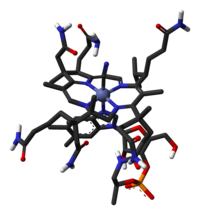
Bioquímicamente hablando, la cianocobalamina es compleja. El término cobalamina hace referencia a un grupo o familia de compuestos con una estructura específica. La cianocobalamina es una de estas cobalaminas que resulta de la unión asimétrica de cuatro anillos pirrólicos, formando un grupo macrocíclico casi planar (núcleo de corrina) en torno a un ion central de cobalto. El anillo de corrina es similar al anillo porfirínico, que también puede ser encontrado en el grupo hemo, la clorofila y en los citocromos; y se diferencia de estos por su asimetría en las uniones entre los grupos pirrólicos. En esta estructura, el cobalto posee seis valencias, cuatro de las cuales forman un enlace covalente con los átomos de nitrógeno de los anillos pirrólicos. La quinta valencia de coordinación siempre se encuentra unida a un pseudonucleótido complejo, el 5,6-dimetilbencimidazol, casi perpendicular al núcleo y, finalmente, cuando la sexta valencia se une a diversos radicales produce los diferentes derivados de la cobalamina. Cuando se une un grupo de cianuro (CN-) forma la cianocobalamina.[4]
La vitamina B12 es un descriptor genérico de un grupo de moléculas de cobalto y sus anillos de corrina, que son definidos por su particular función en el cuerpo. Todas las moléculas de sustrato corrina-cobalto de la B12, solo son sintetizadas por bacterias. Sin embargo, y excepto en los poco frecuentes casos y después de que esta síntesis está completa, el cuerpo humano tiene la capacidad de convertir cualquier forma de B12 en una forma activa, por medio de la eliminación enzimática de ciertos grupos prostéticos de químicos desde el átomo de cobalto y su posterior sustitución por otros grupos.
Todas las diversas formas de B12 (vitámeros), cristales y soluciones a base de agua, son de color rojo muy oscuro debido al complejo de corrina-cobalto.
Formas
[editar]- La cianocobalamina es uno de los vitámeros del complejo B, ya que puede ser metabolizada en el cuerpo por una forma de coenzima activa. Sin embargo, la cianocobalamina de B12 no se produce en la naturaleza, sino que es un subproducto hecho de otras formas de B12 que son aglutinantes con alta afinidad con el cianuro (CN-), el cual captan en el proceso de purificación de la vitamina realizado con carbón activado después de que esta es producida por las bacterias en el proceso industrial. Dado que la forma de cianocobalamina de B12 es fácil de cristalizar y no es propensa a la oxidación por aire, es utilizada normalmente como una forma de vitamina B12 para los aditivos alimentarios y en muchos multivitamínicos comunes. Sin embargo, esta forma no es exactamente igual a la natural, en cuanto al número de vitámeros que pueden activarla. Puede ser llamada correctamente vitamina B12, pero tan solo es una forma de ella; por lo tanto, toda cianocobalamina es vitamina B12, pero no toda B12 es cianocobalamina.[1] La cianocobalamina pura es de color rosa oscuro debido a la mayor presencia de cristales octaédricos de cobalto(II)alamina (Co2+), los cuales están bien formados y son un milímetro más grandes.
Propiedades químicas
[editar]La cianocobalamina es el vitámero de la familia de las cobalaminas más famoso y ampliamente producido, porque es estable al contacto con el aire al contrario de las demás formas de B12. Es la más fácil de cristalizar y, por lo tanto, más fácil de purificar después de producida por fermentación bacteriana o por sintetización in vitro. Puede ser obtenida en forma de cristales de color rojo oscuro o en forma de polvo amorfo rojo. Es muy higroscópica en su forma anhídrica y poco solube en agua (1:80). Es estable al tratamiento en autoclave durante cortos períodos de tiempo a 121 °C. Las coenzimas de la vitamina B12 son muy inestables en presencia de la luz.
En los animales el ligando de cianuro se sustituye por otros grupos como el adenosil y el metil, que son las formas biológicamente activas. La porción restante de la cianocobalamina se mantiene sin cambios.
Reacciones químicas
[editar]
En las cobalaminas el cobalto normalmente está presente en estado trivalente: Co(III). Sin embargo y bajo condiciones reductoras, el cobalto central se reduce a Co(II) o incluso a Co(I), que por lo general se denotan como B12r y B12s, para denotar a la forma reducida y súper reducida respectivamente.
Las B12r y B12s pueden ser preparadas a partir de la cianocobalamina por reducción potencial controlada, por reducción química usando borohidruro de sodio en una solución alcalina, en zinc, en ácido acético o por la acción de tioles. Tanto la B12r como la B12s son estables indefinidamente bajo condiciones libres de oxígeno. La B12r presenta un color entre naranja y marrón cuando está en alguna solución, mientras que la B12s toma un color verde azulado bajo luz natural y púrpura bajo luz artificial.[5]
La B12s es una de los tipos más nucleófilos conocidos en solución acuosa. Es llamado a menudo un «súper nucleófilo». Esta propiedad es la que permite la conveniente preparación de análogos de cobalamina con sus diferentes sustituyentes, gracias a un ataque nucleófilo de haloalcanos y haluros de vinilo.[5]
Por ejemplo, la cianocobalamina puede ser convertida a sus cobalaminas analógicas a través de la reducción a B12s, seguido por la adición de los siguientes compuestos: haloalcanos, haluro de ácido, alqueno o alquino. El impedimento estérico es el principal factor limitante en la síntesis de los análogos de la coenzima B12. Esto es, no hay reacción entre el cloruro de dimetilpropano y la B12s, mientras que los análogos de los haloalcanos secundarios son demasiado inestables para ser aislados.[5] Este efecto puede ser debido a la fuerte coordinación entre el benzimidazol y el átomo central de cobalto, que tira de él hacia abajo al plano del anillo de corrina. El efecto trans también determina la polaridad del enlace Co-C así formado. Sin embargo, una vez que el benzimidazol se separa del cobalto por cuaternización con yoduro de metilo, que sustituye por iones de H2O o de hidroxilo. Entonces, varios haloalcanos secundarios son atacados fácilmente por las B12s modificadas para formar los correspondientes análogos estables de cobalamina.[6] Por lo general, los productos son extraídos y purificados por extracción con cloruro de fenol-metileno o por cromatografía en columna.[5]
Los análogos de cobalamina preparados por este método incluyen las coenzimas de origen natural como la metilcobalamina y la cobamamida, y también otras cobalaminas que no se producen naturalmente, tales como la vinilcobalamina, la carboximetilcobalamina y la ciclohexilcobalamina.[5] Estas últimas reacciones están siendo estudiadas para su uso como catalizador de la deshalogenación química, como reactivo órganico y como un catalizador de sistemas fotosensibles.[7]
Producción
[editar]La cianocobalamina es elaborada comercialmente mediante fermentación bacteriana. La fermentación por una variedad de microorganismos produce una mezcla de metil, hydroxi-, y adenosilcobalamina. Estos compuestos se convierten en cianocobalamina por la adición de cianuro de potasio en presencia de nitrito de sodio y calor. Dado que un número de especies de Propionibacterium no producen exotoxinas o endotoxinas y ya que se les ha concedido la calificación de considerado generalmente como seguro (GRAS: Generally Regarded As Safe) por la Administración de Alimentos y Medicamentos de Estados Unidos; son los microorganismos para la fermentación bacteriana preferidos para la producción de vitamina B12.[8]
Tradicionalmente, una forma de vitamina B12 llamada hidroxocobalamina, es a menudo producida por bacterias, que luego muda a cianocobalamina en el proceso de purificación en columnas de carbón activado después de ser separada de los cultivos bacterianos. Este cambio no se realiza inmediatamente cuando la vitamina B12 es extraída para su caracterización. El cianuro está presente naturalmente en el carbón activado, y la hidroxocobalamina, que tiene una gran afinidad con el cianuro, lo recoge y cambia a la cianocobalamina. Esta última es la forma presente en la mayoría de las preparaciones farmacéuticas debido a que la adición de cianuro estabiliza la molécula.[1]
La producción francesa representa el 80% de la mundial, y más de 10 toneladas de este compuesto son vendidas al año; 55% de las ventas se destina a la alimentación animal, mientras que el 45% restante es para consumo humano.[9]
Uso farmacéutico
[editar]La cianocobalamina por lo general es prescrita después de la extirpación quirúrgica de parte o todo el estómago o el intestino para asegurar niveles adecuados de vitamina B12 en la sangre. También se utiliza para tratar la anemia perniciosa, deficiencia de vitamina B12 (debido a la baja ingesta de alimentos), tirotoxicosis, hemorragia, tumores malignos, enfermedad hepática y enfermedad renal. Las inyecciones de cianocobalamina son prescritas a menudo para los pacientes con un balón gástrico que han tenido una derivación de gran parte de su intestino delgado, lo que hace difícil la absorción de B12 de alimentos o vitaminas. También se utiliza la cianocobamida para realizar la prueba de Schilling que determina la capacidad de una persona para absorber la vitamina B12.[10]
Tratamiento del envenenamiento por cianuro
[editar]En los casos de envenenamiento por cianuro se administra al paciente hidroxicobalamina, que es un precursor de la cianocobalamina. La hidroxocobalamina se une con el ion de cianuro y forma la cianocobalamina, que luego puede ser secretada por los riñones. Esta ha sido utilizada durante muchos años en Francia y fue aprobado por la Administración de alimentos y medicamentos de Estados Unidos en diciembre de 2006, la cual se comercializa bajo el nombre de Cyanokit.[11]
Toxicidad
[editar]La vitamina B12 por lo general no es tóxica, incluso en grandes dosis; sin embargo puede producir diarrea leve y transitoria, trombosis vascular periférica, picazón, exantema transitoria, urticaria, sensación de hinchazón de todo el cuerpo. Se han reportado casos de anafilaxia y muerte. Aunque las reacciones alérgicas a la vitamina B12 en general se han atribuido a las impurezas en la preparación, algunos pacientes han reaccionado positivamente a la prueba cutánea con cianocobalamina purificada.[12]
Interacciones
[editar]- La absorción de la vitamina B12 en el tracto gastrointestinal puede decrecer por los antibióticos aminoglucósidos, la colchicina, la preparación de potasio de liberación prolongada, ácido aminosalicílico y sus sales, anticonvulsionantes (por ejemplo, fenitoína, fenobarbital, primidona), irradiación de cobalto del intestino delgado, y por la excesiva ingesta de alcohol durante más de dos semanas.[13]
- La absorción gastrointestinal de la vitamina B12 puede ser disminuida considerablemente por la neomicina oral. Parece que administrar colchicina aumenta la malabsorción inducida por neomicina de vitamina B12.[13]
- Los pacientes con anemia perniciosa no responden bien a la terapia de vitamina B12 si se administra concomitantemente con cloranfenicol.[13]
- En presencia de una deficiencia de vitamina B12 o bien de ácido fólico, la disminución de la síntesis de la metionina y s-adenosilmetionina interfiere con la biosíntesis de las proteínas, una serie de reacciones de metilación, y con la síntesis de las poliaminas. La célula responde a la deficiencia mediante la reorientación de las rutas metabólicas del folato para abastecer el aumento de la amtolmetina guacil de metiltetrahidrofolato; esto tiende a preservar las reacciones de metilación esenciales a expensas de la síntesis del ácido nucleico. Con la deficiencia de vitamina B12, la actividad de la metilentetrahidrofolato reductasa aumenta, lo que dirige los folatos intracelulares disponibles al conjunto del metiltetrahidrofolato. El metiltetrahidrofolato queda luego inhibido para aceptar y transferir grupos de metilo por falta de vitamina B12; los pasos subsiguientes en el metabolismo del folato que requieren un sustrato privado de ácido tetrahidrofólico. Esto proporciona una base común para el desarrollo de la anemia megaloblástica con la deficiencia ya sea de vitamina B12 o de ácido fólico.[13]
- La vitamina B12 inyectable ha sido reportada como incompatible con el clorhidrato de clorpromazina, la vitamina K1, edisilato de proclorperazina, warfarina de sodio, ácido ascórbico, dextrosa, metales pesados, agentes oxidantes o reductores, y soluciones alcalinas o fuertemente ácidas.[13]
- El metotrexato, la pirimetamina y la mayoría de los antiinfecciosos invalidan las pruebas microbiológicas de la sangre para diagnosticar los niveles de vitamina B12. Si los pacientes tienen anemia perniciosa, la previa administración de cianocobalamina puede provocar resultados falsos positivos para anticuerpos del factor intrínseco que están presentes en la sangre en aproximadamente 50%.[13]
Posibles efectos secundarios
[editar]El uso oral de cianocobalamina puede provocar varias reacciones alérgicas, como urticaria; dificultad para respirar; hinchazón de la cara, labios, lengua, o garganta. Los efectos secundarios menos graves pueden incluir dolor de cabeza, náuseas, malestar estomacal, diarrea, dolor en las articulaciones, picazón o sarpullido.[14]
Véase también
[editar]Referencias
[editar]- ↑ a b c Herbert, Victor (septiembre de 1988). «Vitamin B-12: plant sources, requirements, and assay» [Vitamina B12: fuentes vegetales, requerimientos y un ensayo]. The American Journal of Clinical Nutrition (en inglés). Vol. 48 (No. 3 [Suplemento]): 852-858. PMID 3046314. Consultado el 2 de agosto de 2014.
- ↑ Khan, Adil Ghani; Eswaran, S. V. (junio de 2003). «Woodward’s synthesis of vitamin B12» [La síntesis de la vitamina B12 por Woodward]. Resonance (en inglés). Vol. 8 (No. 6): 8-16. doi:10.1007/BF02837864.
- ↑ 1). Eschenmoser, Albert; Winter, Claude E. (24 de junio de 1977). «Natural product synthesis and vitamin B12» [Síntesis de productos naturales y la vitamina B12]. Science (en inglés). Vol. 196 (No. 4297): 1410-1420. doi:10.1126/science.867037.
2). Riether, Doris; Mulzer, Johann (enero de 2003). «Total synthesis of cobyric acid: historical development and recent synthetic innovations» [La síntesis total del ácido cobírico: desarrollo histórico y recientes innovaciones sintéticas]. European journal of organic chemistry (en inglés). Vol. 2003 (No. 1): 30-45. doi:10.1002/1099-0690(200301)2003:1<30::AID-EJOC30>3.0.CO;2-I.
- ↑ 1). Forrellat Barrios, Mariela; Gómis Hernández, Irma; Gautier du Défaix Gómez, Hortensia (1999). «Vitamina B12: metabolismo y aspectos clínicos de su deficiencia». Revista cubana de hematología, inmunología y hemoterapia (La Habana, Cuba: Ciencias Médicas. Centro Nacional de Información de Ciencias Médicas, Ministerio de Salud Pública). Vol. 15 (No. 3): 159-174. ISSN 1561-2996. OCLC 54623324. Archivado desde el original el 15 de julio de 2014. Consultado el 2 de agosto de 2014.
2) Jaouen, Gérard (2006) [2005]. Bioorganometallics: biomolecules, labelling, medicine [Biorganometálicos: biomoléculas, clasificación, medicina] (en inglés). Weinheim, Alemania y Chichester, Inglaterra: En Alemania Wiley-VCH y por John Wiley distributor en Inglaterra. ISBN 352730990X. OCLC 475222080. Archivado desde el original el 10 de agosto de 2014. Consultado el 2 de agosto de 2014.
- ↑ a b c d e «Preparation of the reduced forms of vitamin B12 and of some analogs of the vitamin B12 coenzyme containing a cobalt-carbon bond "vitamins and coenzymes," Vol. XVIII, part C.» [Preparación de las formas reducidas de la vitamina B12 y de algunos análogos de la coenzima de la vitamina B12 que contienen un enlace de cobalto-carbono «vitaminas y coenzimas»] (pdf). Cobalamins and cobamides (en inglés) (D.B. McCormick y L.D. Wright). Vol. XVIII Parte C. (No. 24). 1971. Archivado desde el original el 12 de agosto de 2014. Consultado el 11 de agosto de 2014.
- ↑ Brodie, Jonathan D. (1 de febrero de 1969). «On the mechanism of catalysis by vitamin B12» [Sobre el mecanismo de la catálisis de la vitamina B12]. Proceedings of the National Academy of Sciences of the United States of America (en inglés). Vol. 62 (No. 2): 461-467. Consultado el 11 de agosto de 2014.
- ↑ Shimakoshi, Hisashi; Hisaeda, Yoshio (agosto de 2009). «Environmental-friendly catalysts learned from vitamin B12-dependent enzymes» [Catalizadores respetuosos del medio ambiente: enseñanzas de las enzimas B12 dependientes] (pdf). TCIMAIL (en inglés) (TCI Chemicals) (No. 138): 2-11. Consultado el 11 de agosto de 2014.
- ↑ Riaz, Muhammad; Ansari, Zumir Ahmed; Iqbal, Fouzia; Akram, Muhammad (2007). «Microbial production of vitamin B12 by methanol utilizing strain of Pseudomonas specie» [Producción microbiana de la vitamina B12 mediante metanol utilizando una cepa de la especia Pseudomonas]. Pakistan journal of biochemistry and molecular biology (en inglés). Vol. 40 (No. 1): 5-10. Consultado el 18 de agosto de 2014.
- ↑ Kaesler, Bruno (2005). «9. Vitamin B12 (Cobalamins)» [9. Vitamina B12 (Cobalaminas)]. Ullmann's encyclopedia of industrial chemistry [Enciclopedia Ullmann de química industrial] (en inglés). Weinheim: Wiley-VCH. doi:10.1002/14356007.a27_443.
- ↑ Ehrlich, Steven D. (26 de junio de 2011). «Vitamin B12 (cobalamin)» (en inglés). Universidad de Maryland — Centro médico. Consultado el 18 de agosto de 2014.
- ↑ 1). Bledsoe, Bryan; Porter, Robert S.; Cherry, Richard A. (2009). Paramedic care: principles & practice [Atención en urgencias médicas: principios y práctica] (en inglés). 3. Medical emergencies (3.ª edición). Upper Saddle River, N. J., Londres: Pearson Prentice Hall. p. 471. ISBN 9780135137024. OCLC 781574899.
2). Hamel, Jillian (febrero de 2011). «A review of acute cyanide poisoning with a treatment update» [Una revisión de la intoxicación aguda por cianuro con una actualización del tratamiento]. Critical care nurse (en inglés). Vol. 31 (No. 1): 78-82. doi:10.4037/ccn201179.
- ↑ En Medline hay más información sobre Cianocobalamina (en inglés)
- ↑ a b c d e f «Cyanocobalamin» (en inglés). NIH U. S. National library of medicine. Consultado el 18 de agosto de 2014.
- ↑ Healthwise (15 de diciembre de 2012 [última revisión]). «Cyanocobalamin (oral)» (en inglés). MSN Health. Archivado desde el original el 15 de abril de 2012. Consultado el 18 de agosto de 2014.
Enlaces externos
[editar] Wikimedia Commons alberga una categoría multimedia sobre Cianocobalamina.
Wikimedia Commons alberga una categoría multimedia sobre Cianocobalamina.