Budésonide
| Budésonide | |

| |
| Identification | |
|---|---|
| No CAS | |
| No ECHA | 100.051.927 |
| No CE | 257-139-7 |
| Code ATC | A07, D07, R01, R03 |
| DrugBank | DB01222 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C25H34O6 [Isomères] |
| Masse molaire[1] | 430,533 9 ± 0,024 2 g/mol C 69,74 %, H 7,96 %, O 22,3 %, |
| Propriétés physiques | |
| T° fusion | 226 °C (décomposition) |
| Composés apparentés | |
| Autres composés | |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le budésonide est un médicament anti-inflammatoire (glucocorticoïde) utilisé entre autres pour le traitement de l'asthme, la rhinite non infectieuse (y compris la rhinite allergique et les autres allergies) et pour le traitement et la prévention des polypes nasaux[2]. Il est également utilisé pour soigner la maladie de Crohn.
Le budésonide est commercialisé par la firme AstraZeneca comme produit à inhaler par le nez sous le nom de Rhinocort (Rhinosol au Danemark), à inhaler par la bouche, en poudre, sous le nom de Pulmicort Turbuhaler. Il est également commercialisé en gélules pour le lavage de l'intestin sous le nom commercial d'Entocort. Et il est vendu en combinaison avec du fumarate de formotérol dihydraté sous le nom commercial de Symbicort.
Elle est utilisée pour le traitement de la rectocolite hémorragique[3],[4] et de la maladie de Berger[5],[6].
Stéréochimie
[modifier | modifier le code]| Budésonide (2 stéréoisomères) | |
|---|---|
 (22R)-configuration |
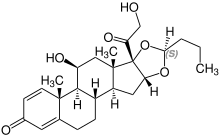 (22S)-configuration |
Pharmacologie
[modifier | modifier le code]Le budésonide a un fort effet de premier passage[7]. Il est efficace dans l'iléon terminal et le côlon droit.
Le budésonide, par rapport à la prednisolone, a été associé avec moins de perte de densité osseuse, et contrairement à d'autres corticostéroïdes, a peu d'influence sur l'axe hypotalamo-hypophyso-surrénalien, ce qui diminue également la nécessité d'un sevrage progressif.[citation nécessaire] Dans l'ensemble, l'incidence de manifestations systémiques est plus faible qu'avec des médicaments similaires.
Effets secondaires
[modifier | modifier le code]Le budésonide peut causer[8] :
- Irritation ou brûlure au nez
- Saignements ou plaies dans le nez
- Vertiges
- Maux d'estomac
- Toux
- Enrouement
- Sécheresse de la bouche
- Éruptions cutanées
- Maux de gorge
- Mauvais goût dans la bouche
- Changement de couleur du mucus
- Palpitations
De plus les symptômes suivants doivent être signalés immédiatement :
- Difficulté à respirer ou enflure du visage
- Taches blanches dans la gorge, la bouche ou le nez
- Menstruations irrégulières
- Acné sévère
- Rarement, des changements de comportement —- quand ils se produisent, ils semblent surtout affecter les enfants. Pour citation, voir la référence ci-dessus.
Rappel
[modifier | modifier le code]Les inhalateurs Pulmicort ont été rappelés par AstraZeneca en 2004 car on craignait qu'ils ne puissent pas toujours donner une dose complète[9].
Mauvaise utilisation ou abus
[modifier | modifier le code]Dans son plan de travail pour 2010, l'OIG (en anglais : Office of the Inspector General) du département de la Santé et des Services sociaux des États-Unis a déclaré qu'il y aurait une enquête pour déterminer si le nombre d'unités de budésonide facturé et payé par l'assurance maladie dans le sud de la Floride dépasse la quantité effectivement distribuée dans la région. L'OIG a noté que ses travaux précédents ont révélé « des modèles de facturation aberrants » pour le budésonide en inhalation, et croit que beaucoup de ces factures pourraient être frauduleuses[10].
On n'a pas démontré, contrairement aux décongestionnants nasaux en ventre libre, que le budésonide peut causer la congestion nasale par effet rebond[11].
Contre le Covid-19
[modifier | modifier le code]Selon des chercheurs de l'université d'Oxford, le budésonide semble réduire le besoin d'hospitalisations ainsi que le temps de récupération des patients COVID-19 s'il est administré dans les sept jours suivant l'apparition des symptômes. Les résultats ont été obtenus à la suite d’une étude à mi-parcours du budésonide stéroïde[12]. Ce produit est maintenant utilisé au Royaume-Uni pour traiter le Covid-19 en premiers soins[13] et permet d'abréger la récupération de patients non admis à l'hôpital[14],[15].
Faisant partie du Principle Trial, l'étude de 28 jours portant sur 146 patients et publiée en février 2021 suggère que le budésonide inhalé réduit le risque de soins urgents ou d'hospitalisation de 90 % par rapport aux soins habituels[16]. Les chercheurs ont déclaré que l'essai avait été inspiré par le fait que les patients atteints de maladies respiratoires chroniques, qui se voient souvent prescrire des stéroïdes inhalés, étaient considérablement sous-représentés parmi les patients hospitalisés atteints de COVID-19 au début de la pandémie. Les données initiales de l'étude ont également révélé que les volontaires traités par budésonide avaient une résolution plus rapide de la fièvre et moins de symptômes persistants[12],[17]. L'étude de phase II revue par les pairs publiée dans The Lancet le confirme ces données [18].
Au printemps 2021, il est inclus, en Inde, dans le protocole national de soin du Covid-19 (National management protocol for Covid-19)[19].
Divers
[modifier | modifier le code]Le budésonide fait partie de la liste des médicaments essentiels de l'Organisation mondiale de la santé (liste mise à jour en )[20].
Notes et références
[modifier | modifier le code]- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Propriétés du budésonide
- Stefanos Bonovas, Georgios K. Nikolopoulos, Daniele Piovani et Marien González-Lorenzo, « Comparative assessment of budesonide-MMX and mesalamine in active, mild-to-moderate ulcerative colitis: A systematic review and network meta-analysis », British Journal of Clinical Pharmacology, vol. 85, no 10, , p. 2244–2254 (ISSN 1365-2125, PMID 31269287, PMCID 6783624, DOI 10.1111/bcp.14051, lire en ligne, consulté le )
- (en) http://www.genengnews.com/gen-news-highlights/positive-phase-iii-data-mean-cosmo-and-santarus-plan-2011-nda-for-ulcerative-colitis-drug/81244010/
- (en) Center for Drug Evaluation and Research, « FDA approves first drug to decrease urine protein in IgA nephropathy, a rare kidney disease », FDA, (lire en ligne, consulté le )
- Jonathan Barratt, Richard Lafayette, Jens Kristensen et Andrew Stone, « Results from part A of the multi-center, double-blind, randomized, placebo-controlled NefIgArd trial, which evaluated targeted-release formulation of budesonide for the treatment of primary immunoglobulin A nephropathy », Kidney International, , S0085–2538(22)00836–5 (ISSN 1523-1755, PMID 36270561, DOI 10.1016/j.kint.2022.09.017, lire en ligne, consulté le )
- (en) http://www.pharmgkb.org/do/serve?objId=PA448681
- (en) BUDESONIDE - NASAL AEROSOL INHALER (Rhinocort) side effects, medical uses, and drug interactions
- (en) http://www.mhra.gov.uk/home/groups/is-md/documents/drugalert/con1002579.pdf Rappel d'AstraZeneca : Pulmicort
- (en) http://www.oig.hhs.gov/publications/docs/workplan/2010/Work_Plan_FY_2010.pdf Office of the Inspector General. p 26.
- (en) https://www.drugs.com/rhinocort.html
- (en) Common asthma drug cuts COVID-19 hospitalization risk, recovery time - Oxford study, reuters.com, 9 février 2021
- Asthma drug budesonide shortens recovery time in non-hospitalised patients with COVID-19
- Covid-19: Budesonide shortens recovery time in patients not admitted to hospital, study finds
- Asthma drug budesonide shortens recovery time in non-hospitalised patients with COVID-19
- Asthma drug budesonide speeds recovery for at-home COVID-19 patients
- (en) Sanjay Ramakrishnan et al., Inhaled budesonide in the treatment of early COVID-19 illness: a randomised controlled trial, medrxiv.org, 9 février 2021, doi.org/10.1101/2021.02.04.21251134
- « Inhaled budesonide in the treatment of early COVID-19 (STOIC): a phase 2, open-label, randomised controlled trial », sur thelancet.com,
- Clinical management protocol for Covid-19 (In adults)
- (en) WHO Model List of Essential Medicines, 18th list, avril 2013
Voir aussi
[modifier | modifier le code]Liens externes
[modifier | modifier le code]- Compendium suisse des médicaments : spécialités contenant Budésonide
- Page spécifique sur Le Vidal.fr