Dicer
| Dicer | |
| Azonosítók | |
| Jel | DICER1, DCR1, HERNA |
| Entrez | 23405 |
| OMIM | 606241 |
| RefSeq | NM_001195573 |
| UniProt | Q9UPY3 |
| PDB | 2EB1 |
| Egyéb adatok | |
| Lokusz | 14. krom. q32.13 |
A Dicer, más néven Dicer endoribonukleáz vagy DNázmotívumú helikáz a DICER1 gén által kódolt enzim. A RNáz III-család tagjaként a kétszálú RNS-t (dsRNS) és a pre-mikro-RNS-t (pre-miRNS) rövid kétszálú RNS-töredékekre (kis interferáló RNS és mikro-RNS) bontja. Ezek 20–25 bázispárból állnak 2 bázis többlettel a 3′-végen. A Dicer megkönnyíti az RNS-indukált csendesítőkomplex (RISC) aktiválását, mely az RNS-interferencia terén fontos. A RISC része a katalitikus Argonaute mRNS-bontó endonukleáz.
Felfedezés
[szerkesztés]A Dicert 2001-ben nevezte el a Stony Brook Egyetemen tanuló Emily Bernstein Gregory Hannon laboratóriumában, a Cold Spring Harbor Laboratóriumban végzett kutatása során. Felfedezett egy kis RNS-ek létrehozásáért felelős enzimet. A Dicer képességét 22 nukleotid körüli RNS-töredékek létrehozására annak RISC-komplextől való elválasztásával fedezték fel a dsRNS-transzfekcióval való RNSi-iniciáció után. E kísérlet kimutatta, hogy a RISC nem felel a kis nukleotidtöredékekért. A RNáz III-családbeli enzimek RNS-töredék-képző képességét vizsgáló kísérletek a Drosophila CG4792-re (ma Dicer) szűkítették a keresést.[1]
A Dicer-ortológok sok más élőlényben megtalálhatók.[2] A Physcomitrella patens moha DCL1b-je, a 4 DICER-fehérje egyike nem a miRNS-képzésért, hanem a miRNS-átiratok lebontásáért felel. Így új mechanizmust fedeztek fel a génexpresszió-szabályzásban, a gének miRNS általi epigenetikai csendesítését.[3]
Az első ismert kristályszerkezetű Dicer a Giardia duodenalisé volt. Ezt Ian MacRae fedezte fel posztdoktori kutatása során Jennifer Doudna laboratóriumában posztdoktori kutatása során a Kaliforniai Egyetemen. Egy PAZ és két RNáz III-domént röntgenkrisztallográfia révén fedeztek fel. A fehérje 82 kDa-os, és más élőlényekben lévő állandósult funkcionális magot képvisel – például a humán fehérje 219 kDa-os. A két méret eltérését a humán Dicer legalább 5 eltérő doménje okozza. Ezek fontosak a szabályzásban, a dsRNS-feldolgozásban és az RNS-interferenciaproteinfaktor-működésben.[4]
Funkciós domének
[szerkesztés]
A humán Dicer (más néven hsDicer vagy DICER1) ribonukleáz III, mivel kétszálú RNS-t bont. A két RNáz III-domén mellett helikáz-, PAZ (Piwi/Argonaute/Zwille) domént[6][7] és két dsRNS-kötő domént (DUF283 és dsRBD) tartalmaz.[4][8]
Egy 2006-os kutatás szerint a PAZ domén képes a dsRNS kétnukleotidos 3'-többletét megkötni, míg a RNáz III-katalitikusdomének pszeudodimert hoznak körülötte létre a szálak szétválasztásához. Ez a dsRNS funkcionális rövidülését okozza. A PAZ és a RNáz III-domének közti különbséget az összekötő hélix szöge befolyásolja, és befolyásolja a miRNS-termék hosszát.[5] A dsRBD a dsRNS-hez köt, bár a domén kötőhelye nem ismert. Feltehetően e domén más szabályzófehérjékkel (emberben TRBP, Drosophilában R2D2, Loqs) együtt működik a RNáz III-domének elhelyezéséhez és a sRNS-termékek irányításához.[9] A helikázdomén hosszú szubsztrátokat dolgozhat fel.[9]
Szerepe
[szerkesztés]RNSi
[szerkesztés]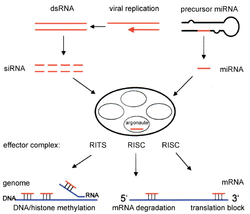
Mikro-RNS
[szerkesztés]Az RNS-interferencia az a folyamat, ahol az RNS miRNS-sé bomlása gátolja bizonyos gazda-mRNS-szekvenciák expresszióját. A miRNS a sejtben primer miRNS-ből keletkezik a sejtmagban. Ezek kisebb prekurzor (pre-) miRNS-sé bomlanak, melyek általában 70 nukleotidból állnak. A pri-miRNS-t a DGCR8 azonosítja, és a Drosha bontja pre-miRNS-sé a sejtmagban. Ezek a citoplazmába kerülnek, ahol a Dicer bontja le érett miRNS-sé.[11]
Kis interferáló RNS
[szerkesztés]A kis interferáló RNS (siRNS) hasonlóan jön létre a miRNS-hez a dsRNS kisebb, 21–23 nukleotid hosszú részekre bontásával.[9] A miRNS-ek és a siRNS-ek is aktiválják a RISC-et, ahol a komplementer cél-mRNS-szekvenciát célozzák, és RNázzal bontják az RNS-t.[12] Ez az adott gént RNSi-vel csendesíti.[13] A siRNS-ek a miRNS-ektől abban térnek el, hogy míg a siRNS-ek általában mRNS-specifikusak, a miRNS-ek nem teljesen komplementerek velük. A miRNS-ek hasonló szekvenciájú célokkal kölcsönhathatnak, különböző gének transzlációját gátolva.[14] Az RNS-interferencia normál folyamatok fontos része, és a rákcélpontokhoz használható diagnosztikai és terápiás eszközként kutatják.[11]

RNSi-n kívül
[szerkesztés]Spermatogenezis
[szerkesztés]A Dicer a spermatogenezisben szabályozza a fő szatellitismétlődés transzkriptumainak expresszióját és a meiotikus kromoszómaszegregációt.[15]
A DNS-ben
[szerkesztés]A heterokromatinképződéshez, a DNS-hipometiláció és a hiszton-hiperacetiláció akadályozásához szükséges. Egérembrió-őssejtekben a di-/trimetil-H3K9 szintjét és a centromerekben lévő ismétlődő szakaszok metilációját a Dicer-knockout csökkenti.[16]
Betegségek
[szerkesztés]Makuladegeneráció
[szerkesztés]A korral összefüggő makuladegeneráció gyakori vakságok fejlett országokban. A Dicer szerepe e betegségben fontos lett, miután kiderült, hogy az érintett betegek Dicer-szintje alacsonyabb a retinapigment-epitéliumban (RPE). A csak az RPE-ben való Dicer-hiánnyal rendelkező egerek hasonló tüneteket mutattak. Azonban más fontos RNSi-fehérjékkel, például Droshával vagy Pashával nem rendelkező egerek nem mutattak makuladegenerációs tüneteket. Ez alapján a retina egészségében a Dicernek specifikus szerepe van, mely független az RNSi-től, így nem a si/miRNS-keletkezéstől függ. Az Alu-RNS (az Alu elemek RNS-átiratai) nagyobb mennyiségben voltak jelen az elégtelen Dicerrel rendelkező betegekben. E nemkódoló RNS-ek hurkot alkotó dsRNS-eket alkothatnak, melyeket az egészséges retinában a Dicer lebont. Azonban az elégtelen Dicer-szint esetén az Alu-RNS szintnövekedése az RPE degenerációjához vezet gyulladás miatt.[17][18]
Rák
[szerkesztés]A rákok megváltozott miRNS-expressziós profilja miatt a miRNS-eknek, így a Dicernek fontos szerepe van a rákfejlődésben és -prognózisban. A miRNS-ek tumorszupresszorként működhetnek, így megváltozott expressziójuk tumorigenezist okozhat.[19] A tüdő- és petefészekrák esetén a rossz prognózis és a csökkent túlélési idők összefüggnek a kisebb Dicer- és Drosha-expresszióval. A kisebb Dicer-szint összefügg az előrehaladott tumorral is. Azonban a magas Dicer-expresszió más rákokban, például a prosztata-[20] és nyelőcsőrákban összefügg a rossz betegprognózissal. Ezen eltérées alapján egyedi Dicert tartalmazó RNSi-szabályzófolyamatok állnak a háttérben az eltérő tumortípusoknál.[11]
A Dicer a DNS-javításban is fontos. A DNS-károsodás a csökkent Dicer-expresszióval a DNS-javítás és egyéb mechanizmusok csökkent hatékonysága miatt növekszik. Például a Dicer termelte siRNS a kettősszál-töréseknél a kettősszáltörés-javításban fontos fehérjekomplexeket irányíthatja, továbbá kromatinmódosulásokat is irányíthat. Ezenkívül a miRNS-expresszióminták az ionizáló vagy ultraibolya sugárzás okozta DNS-károsodás hatására változnak. Az RNSi-mechanizmusok felelnek a transzpozoncsendesítéséért, hiányukban, mintha a Dicer expressziója csökkent vagy megszűnt volna, DNS-károsító aktivált transzpozonokat okozhat. A DNS-károsodás növekedése onkogén mutációkkal rendelkező sejteket – így tumorfejlődést – okozhat.[11]
Egyéb betegségek
[szerkesztés]A többcsomós schwannomatózisos golyva autoszomális domináns betegség, mely e gén mutációival függ össze.[21]
Virális patogenezis
[szerkesztés]Az RNS-vírusok általi fertőzés elindíthatja az RNSi-kaszkádot. Feltehetően a Dicer kapcsolódik a virális immunitáshoz, mivel a növényi és állati sejteket is fertőző vírusok rendelkeznek RNSi-válasz-gátló fehérjékkel. Emberben a HIV-1, az influenza- és vacciniavírus ilyen RNSi-gátló fehérjéket kódolnak. A Dicer gátlása hasznos a vírusnak, mivel a Dicer képes a virális dsRNS bontására RISC-be helyezésére, lebontva a virális mRNS-t, így küzdve a fertőzés ellen. Egy másik lehetséges víruspatogenezis-mechanizmus a Dicer blokkolása mint sejt-miRNS-utak gátlásához.[22]
Rovarokban
[szerkesztés]A Drosophilában a Dicer-1 pre-miRNS-feldolgozással hoz létre miRNS-t, a Dicer-2 siRNS-t hoz létre hosszú dsRNS-ből.[23] A rovarok a Dicert antivirális fehérjeként használhatják. Ez fontos, mivel a szúnyogok számos virális betegségért, például a gyakran halálos arbovírusok által okozottakért (nyugat-nílusi láz, dengue-láz, sárgaláz stb.) felelnek.[24] Míg a szúnyogok, ezen belül az Aedes aegypti e vírus vektorai, ők nem a tervezett gazdák. Az átadás egy nőstény szúnyog gerincesvérigénye miatt alakul ki a petefejlődéshez. Az RNSi-út a rovarokban más állatokéhoz hasonlít, a Dicer-2 lebontja a vírus-RNS-t és a RISC-be helyezi, ahol egy szál az RNSi-termékek templátja, a másik lebomlik. A nem működő RNSi-útvonal-részeket okozó mutációkkal rendelkező rovarok nagyobb vírusterhelést vagy -szuszceptibilitást mutatnak. Az emberekhez hasonlóan a vírusoknak is vannak az RNSi-elkerüléshez módszereik. Például a Drosophila C-vírus az 1A dsRNS-kötő proteint kódolja, mely megakadályozza a Dicer általi bontását és a RISC-be kerülését. A Heliothis virescens aszkovírus 3a a Dicerhez hasonló RNáz III-t kódol, mely versenghet a dsRNS-ért és siRNS-duplexeket bonthat, megakadályozva a RISC-töltést.[25]
Szabályzás
[szerkesztés]A Dicer hatását modulálja a PACT és a TRBP, melyekkel stabil komplexet képez. Ezek biztosítják a szubsztrát- és bontásspecificitását.[26]
A HSP90 és az AHA1 a miRNS-érést a Dicer szerkezetének kialakulását segítve növeli, melyek legjobban az újonnan transzlált Dicerhez kötnek.[27] Bármelyikük knockdownja csökkenti a Dicer szintjét.[27] Az AHA1 a HSP90 kochaperonja, első 20 aminosavja teszi lehetővé a dicerexpresszió növelését – ez az AHA1–E67K-hoz hasonlóan nem növeli a dicerszintet.[27]
Diagnosztikai és terápiás használat
[szerkesztés]A Dicer használható tumorok jelenlétének azonosítására a testben az enzim expressziós szintje alapján. Egy tanulmány szerint sok rákos betegben csökkent a Dicer-expresszió, és hogy a kisebb expresszió rövidebb túléléssel függ össze.[11] Amellett, hogy diagnosztikai eszköz, a Dicer használható betegek kezelésére idegen siRNS intravénás injekciójával, géncsendesítést okozva.[28]
A siRNS kétféleképp vihető be emlősfajokban, az egyik a közvetlen injekció, mely nem igényel Dicert, a másik a rövid hajtű-RNS-t (shRNS) kódoló plazmidokkal való bevitel, melyeket a Dicer siRNS-sé bont.[29]
A Dicer terápiás siRNS-termelésre való használatának előnye a célok specificitása és diverzitása, szemben a jelenleg használt technológiákkal, például az antitestekkel vagy a kismolekulás inhibitorokkal. Általában a kismolekulás inhibitorok specificitása nehezen kezelhető, és káros mellékhatásaik lehetnek, míg az antitestek bár a siRNS-hez hasonlóan specifikusak, de csak ligandumokkal vagy felszíni receptorokkal szemben használhatók. Azonban az alacsony sejtbe való felvétel a siRNS-injekciók fő akadálya.[11] Az injektált siRNS vérben kevéssé stabil, és stimulálja a nem specifikus immunitást.[30] Emellett a terápiás miRNS-termelés kevéssé specifikus, mivel csak 6–8 nukleotidos megfelelés kell, hogy a miRNS az mRNS-hez csatlakozzék.[31]
Dicerszerű fehérjék
[szerkesztés]A növényi genomok a Dicerhez hasonló fehérjéket kódolnak hasonló funkciókkal és doménekkel az állati Dicerhez. Például az Arabidopsis thaliana modellszervezetben 4 dicerszerű fehérje (DCL1–DCL4) van. A DCL1 a miRNS- és sRNS-termelésben fontos, a DCL2 siRNS-t állít elő cisz helyzetű antiszenz átirattal, segítve a vírusimmunitást és -védelmet, a DCL3 a kromatinmódosításban fontos siRNS-t hoz létre, a DCL4 a transz működésű siRNS-ek metabolizmusában és poszttranszkripciós átiratcsendesítésében fontos. Ezenkívül a DCL1 és 3 a virágzásban is fontos. Az A. thalianában a DCL-knockout súlyos gondot nem okoz.
A rizs és a szőlők is termelnek DCL-eket, mivel a Dicer-mechanizmus számos élőlény közös védekezési stratégiája. A rizs az általa előállított 5 DCL-re további funkciókat is fejlesztett, és fontosabbak a működésben és fejlődésben, mint az Arabidopsiséi. Ezenkívül az expressziós minták a különböző sejttípusok közt eltérnek, míg az Arabidopsisban homogénebb. A rizs-DCL-expressziót befolyásolhatja a biológiai stressz, beleértve a szárazságot, a sótartalmat és a hideget. Így e stresszorok csökkenthetik a növény vírusellenállását. Szemben az Arabidopsisszal, a DCL-funkcióvesztés fejlődési hibákat okoz a rizsben.[32]
Kölcsönhatások
[szerkesztés]A Dicer DNS-károsító anyagok hatására szabályozza a H3K18-deacetilációt a SIRT7-tel kölcsönhatva, és csökkenti a kromatinasszociált SIRT7 mennyiségét azt a citoplazmában tartva.[16]
Jegyzetek
[szerkesztés]- ↑ Bernstein E, Caudy AA, Hammond SM, Hannon GJ (2001). „Role for a bidentate ribonuclease in the initiation step of RNA interference”. Nature 409 (6818), 363–6. o. DOI:10.1038/35053110. PMID 11201747.

- ↑ Jaskiewicz L, Filipowicz W. Role of Dicer in Posttranscriptional RNA Silencing, RNA Interference, Current Topics in Microbiology and Immunology, 77–97. o.. DOI: 10.1007/978-3-540-75157-1_4 (2008). ISBN 978-3-540-75156-4
- ↑ Khraiwesh B, Arif MA, Seumel GI, Ossowski S, Weigel D, Reski R, Frank W (2010. január 1.). „Transcriptional control of gene expression by microRNAs”. Cell 140 (1), 111–22. o. DOI:10.1016/j.cell.2009.12.023. PMID 20085706.
- ↑ a b Lau PW, Potter CS, Carragher B, MacRae IJ (2009. október 1.). „Structure of the human Dicer-TRBP complex by electron microscopy”. Structure 17 (10), 1326–32. o. DOI:10.1016/j.str.2009.08.013. PMID 19836333. PMC 2880462.
- ↑ a b Macrae IJ, Zhou K, Li F, Repic A, Brooks AN, Cande WZ, Adams PD, Doudna JA (2006. január 1.). „Structural basis for double-stranded RNA processing by Dicer”. Science 311 (5758), 195–8. o. DOI:10.1126/science.1121638. PMID 16410517.
- ↑ Entrez Gene: DICER1 Dicer1, Dcr-1 homolog (Drosophila)
- ↑ Matsuda S, Ichigotani Y, Okuda T, Irimura T, Nakatsugawa S, Hamaguchi M (2000. január 1.). „Molecular cloning and characterization of a novel human gene (HERNA) which encodes a putative RNA-helicase”. Biochimica et Biophysica Acta (BBA) - Gene Structure and Expression 1490 (1–2), 163–9. o. DOI:10.1016/S0167-4781(99)00221-3. PMID 10786632.
- ↑ Hammond SM (2005. október 1.). „Dicing and slicing: the core machinery of the RNA interference pathway”. FEBS Letters 579 (26), 5822–9. o. DOI:10.1016/j.febslet.2005.08.079. PMID 16214139.
- ↑ a b c Cenik ES, Fukunaga R, Lu G, Dutcher R, Wang Y, Tanaka Hall TM, Zamore PD (2011. április 1.). „Phosphate and R2D2 restrict the substrate specificity of Dicer-2, an ATP-driven ribonuclease”. Molecular Cell 42 (2), 172–84. o. DOI:10.1016/j.molcel.2011.03.002. PMID 21419681. PMC 3115569.
- ↑ Hammond SM, Bernstein E, Beach D, Hannon GJ (2000. március 1.). „An RNA-directed nuclease mediates post-transcriptional gene silencing in Drosophila cells”. Nature 404 (6775), 293–6. o. DOI:10.1038/35005107. PMID 10749213.
- ↑ a b c d e f Merritt WM, Bar-Eli M, Sood AK (2010. április 1.). „The dicey role of Dicer: implications for RNAi therapy”. Cancer Research 70 (7), 2571–4. o. DOI:10.1158/0008-5472.CAN-09-2536. PMID 20179193. PMC 3170915.
- ↑ Vermeulen A, Behlen L, Reynolds A, Wolfson A, Marshall WS, Karpilow J, Khvorova A (2005. május 1.). „The contributions of dsRNA structure to Dicer specificity and efficiency”. RNA 11 (5), 674–82. o. DOI:10.1261/rna.7272305. PMID 15811921. PMC 1370754.
- ↑ Watson JD. Molecular Biology of the Gene. San Francisco, CA: Cold Spring Harbor Laboratory Press, 641–648. o. (2008). ISBN 978-0-8053-9592-1
- ↑ Zeng Y, Yi R, Cullen BR (2003. augusztus 1.). „MicroRNAs and small interfering RNAs can inhibit mRNA expression by similar mechanisms”. Proceedings of the National Academy of Sciences of the United States of America 100 (17), 9779–84. o. DOI:10.1073/pnas.1630797100. PMID 12902540. PMC 187842.
- ↑ Yadav RP, Mäkelä J-A, Hyssälä H, Cisneros-Montalvo S, Kotaja N (2020. június 2.). „DICER regulates the expression of major satellite repeat transcripts and meiotic chromosome segregation during spermatogenesis” 48 (13), 7135–7153. o. DOI:10.1093/nar/gkaa460. (Hozzáférés: 2024. július 15.)

- ↑ a b Zhang PY, Li G, Deng ZJ, Liu LY, Chen L, Tang JZ, Wang YQ, Cao ST, Fang YX, Wen F, Xu Y, Chen X, Shi KQ, Li WF, Xie C, Tang KF (2016. május 5.). „Dicer interacts with SIRT7 and regulates H3K18 deacetylation in response to DNA damaging agents”. Nucleic Acids Res 44 (8), 3629–3642. o. DOI:10.1093/nar/gkv1504. PMID 26704979. PMC 4856966.
- ↑ Meister G (2011. március 1.). „Vision: Dicer leaps into view”. Nature 471 (7338), 308–9. o. DOI:10.1038/471308a. PMID 21412326.
- ↑ Tarallo V, Hirano Y, Gelfand BD, Dridi S, Kerur N, Kim Y, Cho WG, Kaneko H, Fowler BJ, Bogdanovich S, Albuquerque RJ, Hauswirth WW, Chiodo VA, Kugel JF, Goodrich JA, Ponicsan SL, Chaudhuri G, Murphy MP, Dunaief JL, Ambati BK, Ogura Y, Yoo JW, Lee DK, Provost P, Hinton DR, Núñez G, Baffi JZ, Kleinman ME, Ambati J (2012. május 1.). „DICER1 loss and Alu RNA induce age-related macular degeneration via the NLRP3 inflammasome and MyD88”. Cell 149 (4), 847–59. o. DOI:10.1016/j.cell.2012.03.036. PMID 22541070. PMC 3351582.
- ↑ Tang KF, Ren H (2012). „The role of dicer in DNA damage repair”. International Journal of Molecular Sciences 13 (12), 16769–78. o. DOI:10.3390/ijms131216769. PMID 23222681. PMC 3546719.
- ↑ Chiosea S, Jelezcova E, Chandran U, Acquafondata M, McHale T, Sobol RW, Dhir R (2006. november 1.). „Up-regulation of dicer, a component of the MicroRNA machinery, in prostate adenocarcinoma”. The American Journal of Pathology 169 (5), 1812–20. o. DOI:10.2353/ajpath.2006.060480. PMID 17071602. PMC 1780192.
- ↑ Rivera B, Nadaf J, Fahiminiya S, Apellaniz-Ruiz M, Saskin A, Chong AS, Sharma S, Wagener R, Revil T, Condello V, Harra Z, Hamel N, Sabbaghian N, Muchantef K, Thomas C, de Kock L, Hébert-Blouin MN, Bassenden AV, Rabenstein H, Mete O, Paschke R, Pusztaszeri MP, Paulus W, Berghuis A, Ragoussis J, Nikiforov YE, Siebert R, Albrecht S, Turcotte R, Hasselblatt M, Fabian MR, Foulkes WD (2019). „DGCR8 microprocessor defect characterizes familial multinodular goiter with schwannomatosis”. J Clin Invest.
- ↑ Berkhout B, Haasnoot J (2006. május 1.). „The interplay between virus infection and the cellular RNA interference machinery”. FEBS Letters 580 (12), 2896–902. o. DOI:10.1016/j.febslet.2006.02.070. PMID 16563388. PMC 7094296.
- ↑ Cenik, ES (2011. április 22.). „Phosphate and R2D2 restrict the substrate specificity of Dicer-2, an ATP-driven ribonuclease.”. Molecular Cell 42 (2), 172–84. o. DOI:10.1016/j.molcel.2011.03.002. PMID 21419681. PMC 3115569.
- ↑ Mosquito-borne Diseases. National Center for Infections Disease, Center for Disease Control and Prevention. [2014. január 31-i dátummal az eredetiből archiválva]. (Hozzáférés: 2014. április 22.)
- ↑ Bronkhorst AW, van Rij RP (2014. augusztus 1.). „The long and short of antiviral defense: small RNA-based immunity in insects”. Current Opinion in Virology 7, 19–28. o. DOI:10.1016/j.coviro.2014.03.010. PMID 24732439.
- ↑ Lee HY, Zhou K, Smith AM, Noland CL, Doudna JA (2013. május 9.). „Differential roles of human Dicer-binding proteins TRBP and PACT in small RNA processing”. Nucleic Acids Research 41 (13), 6568–6576. o. DOI:10.1093/nar/gkt361. PMID 23661684. PMC 3711433. (Hozzáférés: 2024. március 2.)

- ↑ a b c Liu X, Yang Y-Y, Wang Y (2022. július 8.). „HSP90 and Aha1 modulate microRNA maturation through promoting the folding of Dicer1”. Nucleic Acids Res 50 (12), 6990–7001. o. DOI:10.1093/nar/gkac528. (Hozzáférés: 2024. április 16.)
- ↑ Kamlah F, Eul BG, Li S, Lang N, Marsh LM, Seeger W, Grimminger F, Rose F, Hänze J (2009. március 1.). „Intravenous injection of siRNA directed against hypoxia-inducible factors prolongs survival in a Lewis lung carcinoma cancer model”. Cancer Gene Therapy 16 (3), 195–205. o. DOI:10.1038/cgt.2008.71. PMID 18818708.
- ↑ Gene silencing by RNA interference is being used routinely to study gene function in cultured mammalian cells. Life Technologies. (Hozzáférés: 2014. április 23.)
- ↑ Schiffelers RM, Ansari A, Xu J, Zhou Q, Tang Q, Storm G, Molema G, Lu PY, Scaria PV, Woodle MC (2004). „Cancer siRNA therapy by tumor selective delivery with ligand-targeted sterically stabilized nanoparticle”. Nucleic Acids Research 32 (19), e149. o. DOI:10.1093/nar/gnh140. PMID 15520458. PMC 528817.
- ↑ Chi SW, Zang JB, Mele A, Darnell RB (2009. július 1.). „Argonaute HITS-CLIP decodes microRNA-mRNA interaction maps”. Nature 460 (7254), 479–86. o. DOI:10.1038/nature08170. PMID 19536157. PMC 2733940.
- ↑ Liu Q, Feng Y, Zhu Z (2009. augusztus 1.). „Dicer-like (DCL) proteins in plants”. Functional & Integrative Genomics 9 (3), 277–86. o. DOI:10.1007/s10142-009-0111-5. PMID 19221817.
Fordítás
[szerkesztés]Ez a szócikk részben vagy egészben a Dicer című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.