Foszfor-trijodid
| Foszfor-trijodid | |
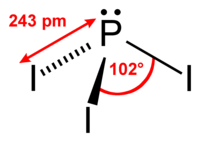 Foszfor-trijodid | |
 A foszor-trijodid modellje | |
| IUPAC-név | Foszfor-trijodid, Foszfor(III)-jodid |
| Más nevek | Trijód-foszfin |
| Kémiai azonosítók | |
|---|---|
| CAS-szám | 13455-01-1 |
| Kémiai és fizikai tulajdonságok | |
| Kémiai képlet | PI3 |
| Moláris tömeg | 411,58 g/mol |
| Megjelenés | sötétvörös, szilárd |
| Sűrűség | 4,18 g/cm³, 25 °C[1] |
| Olvadáspont | 61 °C |
| Forráspont | elbomlik |
| Oldhatóság (vízben) | elbomlik |
| Kristályszerkezet | |
| Molekulaforma | Trigonális piramis |
| Veszélyek | |
| EU osztályozás | Maró (C)[1] |
| R mondatok | R14, R34, R37[1] |
| S mondatok | S26, S36/37/39, S45[1] |
| Lobbanáspont | nem gyúlékony |
| Ha másként nem jelöljük, az adatok az anyag standardállapotára (100 kPa) és 25 °C-os hőmérsékletre vonatkoznak. | |
A foszfor-trijodid (PI3) egy sötétvörös színű, szilárd vegyület, amely vízzel hevesen reagál. Gyakori tévhit, hogy a PI3 annyira instabil,[2] hogy nem lehet tárolni (a levegő párájával reakcióba lép, lásd lejjebb), valójában azonban kereskedelmi forgalomban is kapható. Széles körben alkalmazzák az alkoholok alkil-jodidokká való átalakítására. Emellett erős redukálószer. A foszfornak létezik egy alacsonyabb oxidációs fokú jodidja is, a P2I4, az viszont kétséges, hogy a PI5 létezik-e szobahőmérsékleten.
Tulajdonságai
[szerkesztés]A PI3 dipólusmomentuma szén-diszulfidos oldatban lényegében 0, mert a P−I kötés alig dipólusos. A P−I kötés gyenge is, a PI3 sokkal kevésbé stabilis, mint a PCl3 vagy a PBr3, a PI3 standard képződési entalpiája mindössze −46 kJ/mol.
Reakciói
[szerkesztés]A foszfor-trijodid hevesen reagál vízzel – kis mennyiségű foszfin és P−P kötéseket tartalmazó vegyületek mellett – foszforossav (H3PO3) és hidrogén-jodid keletkezik. Az alkoholokkal hasonlóképpen alkil-jodidokat képez, ez jelenti a PI3 fő felhasználását.
A PI3 emellett erős redukálószer, a szulfoxidokat tioéterekké redukálja, még −78 °C-on is. Emellett a foszfor-trijodid 1-jódbutános oldata vörösfoszforral való hevítés hatására P2I4-dá redukálódik.
Előállítása
[szerkesztés]A szokásos eljárás a foszfor-trijodid előállítására az elemek egyesítése, például jód hozzáadása a fehérfoszfor szén-diszulfidos oldatához.
Emellett a PCl3 is átalakítható foszfor-trijodiddá hidrogén-jodiddal vagy bizonyos fém-jodidokkal.
Hivatkozások
[szerkesztés]
