Vorinostat
| |||
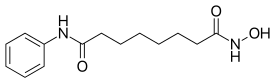
| Vorinostat | |||
| IUPAC-név | |||
| N-Hidroxi-N'-feniloktándiamid | |||
| Kémiai azonosítók | |||
| CAS-szám | 149647-78-9 | ||
| PubChem | 5311 | ||
| ChemSpider | 5120 | ||
| DrugBank | DB02546 | ||
| KEGG | D06320 | ||
| ChEBI | 45716 | ||
| ATC kód | L01XH01 | ||
| |||
| InChIKey | WAEXFXRVDQXREF-UHFFFAOYSA-N | ||
| UNII | 58IFB293JI | ||
| ChEMBL | 98 | ||
| Kémiai és fizikai tulajdonságok | |||
| Kémiai képlet | C14H20N2O3 | ||
| Moláris tömeg | 264,32 g/mol | ||
| Farmakokinetikai adatok | |||
| Biohasznosíthatóság | 1.8–11%[1] | ||
| Metabolizmus | Máj metabolizáció (glükuronidáció és β-oxidáció)
CYP enzimrendszer nem érintett | ||
| Biológiai felezési idő |
~2 óra (vorinostat és O-glükuronid), 11 óra (4-anilino-4-oxobutánsav) | ||
| Fehérjekötés | ~71% | ||
| Kiválasztás | Vesén keresztül (elhanyagolható) | ||
| Terápiás előírások | |||
| Licenc adat | Vorinostat (USA) | ||
| Jogi státusz | Vényköteles | ||
| Vényköteles | |||
| Terhességi kategória | D (US) | ||
| Alkalmazás | Orális (kapszula) | ||
A vorinostat (rINN)[3] néven is ismert szuberanilohidroxámsav (szuberoil + anilid + hidroxámsav, rövidítve SAHA) a hiszton deacetiláz (HDAC) enzimet gátló vegyületek nagy csoportjának a tagja. A hiszton-deacetiláz inhibítorok (HDI) széles spektrumú epigenetikus aktivitással rendelkeznek.
A vorinostatot Zolinza (/Z oʊ l ɪ N z ə / zoh-LIN -zə) néven forgalmazza a Merck cég, amely a bőrön megjelenő manifesztációk kezelésére javallott olyan kután T-sejtes limfómában (CTCL) szenvedő betegeknél, akiknél a betegség tartósan fennáll, súlyosbodik, vagy visszatér két szisztémás terápia alkalmazása alatt vagy után.[4] A vegyületet Ronald Breslow, a Columbia Egyetem vegyésze és Paul Marks, a Memorial Sloan-Kettering Intézet kutatója fejlesztette ki.[5] [6]
Gyógyászati felhasználás
[szerkesztés]A vorinostat volt az első hiszton-deacetiláz inhibítor,[7] amelyet az amerikai Élelmiszer- és Gyógyszerengedélyeztetési Hivatal (FDA) jóváhagyott a CTCL kezelésére 2006. október 6-án.[8] Egy II. fázisú klinikai vizsgálatban azonban nem sikerült bizonyítani az akut mieloid leukémia kezelésében kifejtett hatékonyságát.[9]
Hatásmechanizmus
[szerkesztés]Kimutatták, hogy a vorinostat kötődik a hiszton-deacetilázok aktív kötőhelyéhez, és kelátorként működik a cinkionokkal szemben, amelyek a hiszton-deacetilázok aktív kötőhelyén is megtalálhatók.[10] A hiszton-deacetilázok vorinostat általi gátlása acetilezett hisztonok és acetilezett fehérjék felhalmozódását eredményezi, beleértve a sejtdifferenciálódás kiváltásához szükséges gének expressziójában fontos szerepet játszó transzkripciós faktorokat. A hiszton-deacetilázok I., II. és IV. osztályára hat.
Klinikai vizsgálatok
[szerkesztés]A vorinostatot a CTCL-hez szorosan kapcsolódó Sézary-szindróma, egy másik típusú limfóma kezelésére is alkalmazzák.[11]
Egy nemrégiben készült tanulmány szerint a vorinostat rendelkezik bizonyos aktivitással a visszatérő glioblastoma multiforme ellen is, alkalmazása során az átlagos túlélési idő középértéke 5,7 hónapra módosult (szemben a korábbi vizsgálatok 4-4,4 hónapjával).[12] További agydaganatos betegekkel kapcsolatos vizsgálatokat is terveznek, amelyek során a vorinostatot más gyógyszerekkel kombinálják majd.
A vorinostat alkalmazása előrehaladott, nem kissejtes tüdőrák (NSCLC) kezelésében javuló válaszarányt, valamint megnövekedett átlagos progresszió nélküli túlélési időt és teljes túlélési időt eredményezett.[13]
Biztató eredményeket adott egy fázis II. vizsgálatban myelodysplasticus szindróma esetén idarubicinnel és citarabinnal kombinálva.[14]
Preklinikai vizsgálatok
[szerkesztés]A vorinostatot potenciális HIV-látencia visszafordító ágensként (Latency Reversing Agent = LRA) vizsgálják a "shock and kill" néven ismert kutatási terápiás stratégia részeként.[15] Kimutatták, hogy a vorinostat reaktiválja a HIV vírust a látens HIV-fertőzött T-sejtekben, in vitro és in vivo egyaránt.[16] [17]
A vorinostat bizonyos fokú hatásosságot mutatott a patofiziológiás elváltozásokkal szemben alfa1-antitripszin-hiány[18] és cisztás fibrózis esetén.[19] A legújabb bizonyítékok arra is utalnak, hogy a vorinostat terápiás eszköz lehet a Niemann-Pick kór C1 típusú változatában (NPC1), ami egy ritka lizoszomális lipidtárolási betegség.[20]
A University of Alabama at Birmingham kutatóinak preklinikai kísérletei azt sugallják, hogy a tumorellenes vorinostat, belinostat és panobinostat hatóanyagokat fel lehetne használni a humán papillomavírus, avagy HPV okozta fertőzések kezelésére is.[21]
A Covid19 betegséget okozó SARS-CoV-2-vírus sejtbe bejutásának az egyik kulcsfontosságú receptora az angiotenzin-konvertáló enzim-2 (ACE2) receptor, amelynek fokozott expressziója növeli a megfertőződés kockázatát és a vírus sejtbe jutását. Amerikai kutatók tanulmánya szerint a vorinostat az ACE2 receptorok upregulációját idézi elő.[22]
Kínai kutatók vizsgálták, hogy vemhes egerek szevoflurán expozíciója a vemhesség késői szakaszában neurotoxikus hatású az utódokra, memória- és tanulási zavarokat eredményez, amelynek hátterében többek között a hiszton-deacetiláz 2 enzim túlzott expressziója áll. A hiszton-deacetiláz gátló vorinostat alkalmazásával a szevoflurán utódokra kifejtett neurotoxikus hatása csökkenthető volt.[23]
A vorinostat kedvező hatást mutatott mTOR gátlókkal (sirolimus, everolimus) kombinálva refrakter Hodgkin-limfóma esetén.[24]
Jegyzetek
[szerkesztés]- ↑ Withdrawal Assessment Report for Vorinostat MSD 100 mg Hard Capsules (vorinostat). European Medicines Agency, 2008. október 23. [2016. szeptember 15-i dátummal az eredetiből archiválva]. (Hozzáférés: 2016. szeptember 1.)
- ↑ Zolinza (vorinostat) Capsules. Full Prescribing Information. Merck & Co., Inc., Whitehouse Station, NJ 08889, USA. (Hozzáférés: 2016. szeptember 1.)
- ↑ (2006) „International Nonproprietary Names for Pharmaceutical Substances (INN). Recommended International Nonproprietary Names: List 56”. WHO Drug Information 20 (3), 232. o. (Hozzáférés: 2016. szeptember 1.)
- ↑ Merck News Item. web.archive.org, 2006. szeptember 14. [2006. szeptember 14-i dátummal az eredetiből archiválva]. (Hozzáférés: 2021. május 28.)
- ↑ (2013. szeptember 1.) „Development of a histone deacetylase 6 inhibitor and its biological effects”. Proceedings of the National Academy of Sciences of the United States of America 110 (39), 15704–9. o. DOI:10.1073/pnas.1313893110. PMID 24023063.
- ↑ (2007. január 1.) „Dimethyl sulfoxide to vorinostat: development of this histone deacetylase inhibitor as an anticancer drug”. Nature Biotechnology 25 (1), 84–90. o. DOI:10.1038/nbt1272. PMID 17211407.
- ↑ HDAC Inhibitors Base (vorinostat)
- ↑ Zolinza (vorinostat) dosing, indications, interactions, adverse effects, and more. Medscape Reference. WebMD. (Hozzáférés: 2014. február 16.)
- ↑ (2009. október 1.) „A phase 2 study of vorinostat in acute myeloid leukemia”. Haematologica 94 (10), 1375–82. o. DOI:10.3324/haematol.2009.009217. PMID 19794082.
- ↑ (2005. december 1.) „Histone deacetylase inhibitors: discovery and development as anticancer agents”. Expert Opinion on Investigational Drugs 14 (12), 1497–511. o. DOI:10.1038/sj.bjc.6603463. PMID 16307490.
- ↑ Cuneo A: Mycosis fungoides/Sezary's syndrome. (Hozzáférés: 2008. február 15.)
- ↑ Vorinostat shows anti-cancer activity in recurrent gliomas (angol nyelven). EurekAlert!. (Hozzáférés: 2021. május 28.)
- ↑ (2010. január 1.) „Carboplatin and Paclitaxel in combination with either vorinostat or placebo for first-line therapy of advanced non-small-cell lung cancer”. Journal of Clinical Oncology 28 (1), 56–62. o. DOI:10.1200/JCO.2009.24.9094. PMID 19933908.
- ↑ Zolinza, Idarubicin, Cytarabine Combination Yields High Response Rates In MDS Patients (ASH 2011). [2014. október 30-i dátummal az eredetiből archiválva]. (Hozzáférés: 2021. május 28.)
- ↑ University of North Carolina, Chapel Hill (2017. május 30.). „A Phase I/II Investigation of the Effect of Vorinostat (VOR) on HIV RNA Expression in the Resting CD4+ T Cells of HIV-Infected Patients Receiving Stable Antiretroviral Therapy”.
- ↑ (2009. február 1.) „Expression of latent HIV induced by the potent HDAC inhibitor suberoylanilide hydroxamic acid”. AIDS Research and Human Retroviruses 25 (2), 207–12. o. DOI:10.1089/aid.2008.0191. PMID 19239360.
- ↑ (2009. március 1.) „Suberoylanilide hydroxamic acid reactivates HIV from latently infected cells”. The Journal of Biological Chemistry 284 (11), 6782–9. o. DOI:10.1074/jbc.M807898200. PMID 19136668.
- ↑ (2012. november 1.) „Histone deacetylase inhibitor (HDACi) suberoylanilide hydroxamic acid (SAHA)-mediated correction of α1-antitrypsin deficiency”. The Journal of Biological Chemistry 287 (45), 38265–78. o. DOI:10.1074/jbc.M112.404707. PMID 22995909.
- ↑ (2010. január 1.) „Reduced histone deacetylase 7 activity restores function to misfolded CFTR in cystic fibrosis”. Nature Chemical Biology 6 (1), 25–33. o. DOI:10.1038/nchembio.275. PMID 19966789.
- ↑ (2016. február 1.) „Chronic administration of an HDAC inhibitor treats both neurological and systemic Niemann-Pick type C disease in a mouse model”. Science Translational Medicine 8 (326), 326ra23. o. DOI:10.1126/scitranslmed.aad9407. PMID 26888431.
- ↑ Cancer drug may help treat human papillomavirus infections. (Hozzáférés: 2018. november 30.)
- ↑ Sinha, Sanju, Alejandro A. (2020. július 1.). „In vitro and in vivo identification of clinically approved drugs that modify ACE2 expression”. Molecular Systems Biology 16 (7), e9628. o. DOI:10.15252/msb.20209628. ISSN 1744-4292. PMID 32729248.
- ↑ Yu, Qi, Yan (2019). „Suberoylanilide hydroxamic acid (SAHA) alleviates the learning and memory impairment in rat offspring caused by maternal sevoflurane exposure during late gestation”. The Journal of Toxicological Sciences 44 (3), 177–189. o. DOI:10.2131/jts.44.177. ISSN 1880-3989. PMID 30842370.
- ↑ Janku, Filip, S. Greg (2020. november 1.). „Safety and Efficacy of Vorinostat Plus Sirolimus or Everolimus in Patients with Relapsed Refractory Hodgkin Lymphoma”. Clinical Cancer Research: An Official Journal of the American Association for Cancer Research 26 (21), 5579–5587. o. DOI:10.1158/1078-0432.CCR-20-1215. ISSN 1557-3265. PMID 33055173.
Fordítás
[szerkesztés]Ez a szócikk részben vagy egészben a Vorinostat című angol Wikipédia-szócikk ezen változatának fordításán alapul. Az eredeti cikk szerkesztőit annak laptörténete sorolja fel. Ez a jelzés csupán a megfogalmazás eredetét és a szerzői jogokat jelzi, nem szolgál a cikkben szereplő információk forrásmegjelöléseként.