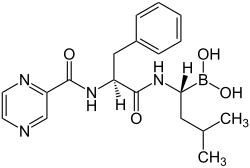
Bortezomib
| Bortezomib | |
|---|---|
 | |
 | |
| Caratteristiche generali | |
| Formula bruta o molecolare | C19H25BN4O4 |
| Massa molecolare (u) | 384.237 g/mol |
| Numero CAS | |
| Numero EINECS | 605-854-3 |
| Codice ATC | L01 |
| PubChem | 387447 |
| DrugBank | DBDB00188 |
| SMILES | O=C(N[C@H] (C(=O)N[C@H] (B(O)O)CC(C) C)Cc1ccccc1) c2nccnc2 |
| Dati farmacocinetici | |
| Legame proteico | 83% |
| Metabolismo | epatico tramite citocromo P450 |
| Emivita | 9-15 h |
| Indicazioni di sicurezza | |
Bortezomib è un farmaco chemioterapico, il primo della famiglia degli inibitori del proteasoma ad essere stato sperimentato[1] e approvato per l'uso nell'uomo[2].
Meccanismo d'azione
[modifica | modifica wikitesto]Bortezomib, inibendo il proteasoma, blocca il sistema di degradazione proteica cellulare, favorisce il processo apoptotico delle cellule mielomatose e agisce a livello midollare con la stimolazione del processo osteoblastogenetico e di inibizione di quello angiogenetico.
Indicazioni
[modifica | modifica wikitesto]È utilizzato efficacemente per il trattamento del mieloma multiplo, da solo o in associazione a doxorubicina, desametasone, talidomide e desametasone o melfalan e prednisone, e del linfoma mantellare[2]. In associazione a ciclofosfamide e desametasone Bortezomib è risultato efficace anche nel trattamento dell'amiloidosi sistemica.
Il Bortezomib è il primo inibitore del proteasoma clinicamente approvato per l'uso nell'uomo, è stato sperimentato sulla febbre grave con sindrome di trombocitopenia (SFTS) da Phlebovirus,[3] nell'infezione da herpes simplex virus (HSV) in associazione con aciclovir,[4], in combinazione con virus oncolitico (OV)[5] ed in alcune forme aggressive di linfoma non-Hodgkin (NHL)[6] (ad esempio il Linfoma mantellare [7], approvato negli USA nell'ottobre 2014).
Note
[modifica | modifica wikitesto]- ^ J. Adams, Potential for proteasome inhibition in the treatment of cancer., in Drug Discov Today, vol. 8, n. 7, Apr 2003, pp. 307-15, PMID 12654543.
- ^ a b (EN) National Cancer Institute, FDA Approval for Bortezomib, su cancer.gov, 7 gennaio 2013. URL consultato il 19 aprile 2014 (archiviato dall'url originale il 19 aprile 2014).
- ^ Liu S, Liu H, Zhang K, Li X, Duan Y, Wang Z, Wang T, Proteasome Inhibitor PS-341 Effectively Blocks Infection by the Severe Fever with Thrombocytopenia Syndrome Virus, in Virol Sin, vol. 34, n. 5, ottobre 2019, pp. 572–582, DOI:10.1007/s12250-019-00162-9, PMID 31637631. URL consultato il 31 marzo 2020.
- ^ Schneider SM, Pritchard SM, Wudiri GA, Trammell CE, Nicola AV, Early Steps in Herpes Simplex Virus Infection Blocked by a Proteasome Inhibitor, in mBio, vol. 10, n. 3, maggio 2019, DOI:10.1128/mBio.00732-19, PMC 6520451, PMID 31088925. URL consultato il 31 marzo 2020.
- ^ Kim Y, Yoo JY, Lee TJ, Liu J, Yu J, Caligiuri MA, Kaur B, Friedman A, Complex role of NK cells in regulation of oncolytic virus-bortezomib therapy, in Proc. Natl. Acad. Sci. U.S.A., vol. 115, n. 19, maggio 2018, pp. 4927–4932, DOI:10.1073/pnas.1715295115, PMC 5948955, PMID 29686060. URL consultato il 31 marzo 2020.
- ^ Arora N, Gupta A, Sadeghi N, Durable complete remission with combination chemotherapy and bortezomib in HIV-associated plasmablastic lymphoma, in BMJ Case Rep, vol. 2017, ottobre 2017, DOI:10.1136/bcr-2017-222063, PMC 5652596, PMID 28993364. URL consultato il 31 marzo 2020.
- ^ Raedler L, Velcade (Bortezomib) Receives 2 New FDA Indications: For Retreatment of Patients with Multiple Myeloma and for First-Line Treatment of Patients with Mantle-Cell Lymphoma, in American Health & Drug Benefits, vol. 8, Spec Feature, marzo 2015, pp. 135–40, PMC 4665054, PMID 26629279.
Altri progetti
[modifica | modifica wikitesto] Wikimedia Commons contiene immagini o altri file su Bortezomib
Wikimedia Commons contiene immagini o altri file su Bortezomib