Tế bào gốc
| Tế bào gốc | |
|---|---|
 Transmission electron micrograph of an adult stem cell displaying typical ultrastructural characteristics. | |
| Chi tiết | |
| Định danh | |
| Latinh | Cellula praecursoria |
| MeSH | D013234 |
| TH | TH H2.00.01.0.00001 {{{2}}}.html HH1.00.01.0.00028, H2.00.01.0.00001 .{{{2}}}.{{{3}}} |
| FMA | 63368 |
| Thuật ngữ giải phẫu | |
Tế bào gốc là các tế bào sinh học có khả năng biệt hoá thành các tế bào khác, từ đó phân bào để tạo ra nhiều tế bào gốc hơn. Chúng được tìm thấy trong các sinh vật đa bào. Đây là thuật ngữ dịch từ tiếng Anh "stem cell" dùng để chỉ các tế bào chưa biệt hoá để đảm nhiệm chức năng trò cụ thể mà chúng vốn có "số phận" phải phát triển thành. Chẳng hạn, một tế bào xương thì không thể "đẻ" ra tế bào xương khác, nhưng tế bào gốc xương thì có. Bởi thế, tế bào gốc có tiềm năng phát triển thành hầu hết bất kỳ loại tế bào nào tuỳ thuộc môi trường yêu cầu.[1] Trong cơ thể sống, có thể lấy tế bào gốc từ hai nguồn chính: mô cơ thể đã trưởng thành và trong phôi giai đoạn sớm. Ngoài ra, các nhà khoa học cũng đã nghiên cứu phương thức phát triển tế bào gốc từ các tế bào khác bằng kỹ thuật "lập trình lại" gen.[2]
Ở động vật có vú, có hai loại tế bào gốc: tế bào gốc phôi (Embryonic stem cell), được phân lập từ trong của phôi nang giai đoạn sớm, và tế bào gốc trưởng thành (Adult stem cell), được tìm thấy trong các mô khác nhau. Trong các sinh vật trưởng thành, tế bào gốc và các tế bào tiền thân đóng vai trò như một hệ thống sửa chữa cho cơ thể, chúng thay thế và bổ sung các tế bào lão hoá hoặc bị hư hại ở người trưởng thành. Trong phôi đang phát triển, tế bào gốc có thể biệt hoá thành các tế bào chuyên biệt - ngoại bì, nội bì và nội mạc tử cung (xem các tế bào gốc đa năng) - nhưng cũng duy trì số lượng tế bào của các cơ quan tái tạo, chẳng hạn như máu, da, hoặc các mô ruột.
Ở người, có ba nguồn đã được biết của các tế bào gốc trưởng thành có khả năng sinh ra thế hệ tế bào sau giống như nó (autologous):
- Tủy xương, được lấy từ phương thức khoan vào xương (điển hình là xương đùi hay xương chậu).
- Mô mỡ (gồm các tế bào mỡ) được lấy bằng phương pháp hút mỡ.[3]
- Máu, trong đó máu được rút ra từ người hiến tặng (tương tự như hiến máu), đi qua máy tách chiết các tế bào gốc và trả lại các phần khác của máu cho người hiến.
Tế bào gốc cũng có thể được lấy từ máu dây rốn ngay sau khi sinh. Trong tất cả các loại tế bào gốc, việc thu hoạch tế bào gốc tự thân sẽ có ít nguy cơ rủi ro nhất. Theo định nghĩa, các tế bào tự thân thu được từ cơ thể của chính mình, giống như người ta có thể sử dụng máu của chính mình cho các cuộc phẫu thuật của mình vậy.
Tế bào gốc trưởng thành thường được sử dụng trong các liệu pháp y khoa khác nhau (ví dụ, cấy ghép tủy xương). Tế bào gốc có thể được phát triển nhân tạo và chuyển đổi (biệt hoá) thành các tế bào chuyên biệt với các đặc tính phù hợp với các tế bào của các mô khác nhau như cơ và dây thần kinh. Các dòng tế bào phôi và các tế bào gốc phôi tự thân sinh ra thông qua việc chuyển gen hạt nhân (Somatic Cell Nuclear Transfer) hoặc biệt hoá ngược (Dedifferentiation) là những phương pháp điều trị rất tiềm năng trong tương lai.[4] Nghiên cứu về các tế bào gốc được phát triển từ những phát hiện của Ernest A. McCulloch và James E. Till ở đại học Toronto vào những năm 1960.[5][6]
Tính chất của tế bào gốc
[sửa | sửa mã nguồn]Theo định nghĩa kinh điển, một tế bào gốc phải có 2 yếu tố sau:[cần dẫn nguồn]
- Tính chất tự làm mới (self-renewal): khả năng đi xuyên suốt các chu kỳ sinh sản của tế bào nhưng vẫn giữ được tình trạng không biệt hoá.
- Tiềm năng (potency): khả năng biệt hoá thành các dạng tế bào chuyên biệt. Trong định nghĩa mới nhất, khả năng này đòi hỏi tế bào gốc phải là totipotent hay pluripotent để có khả năng tạo ra dạng tế bào trưởng thành bất kỳ mặc dù tế bào tiền thân multipotent hay unipotent thỉnh thoảng vẫn được xem như là tế bào gốc.
Tự làm mới
[sửa | sửa mã nguồn]Bao gồm hai cơ chế tồn tại để duy trì quần thể tế bào gốc:[cần dẫn nguồn]
- Cơ chế sao chép bất đối xứng bắt buộc (Obligatory asymmetric replication): Một tế bào gốc chia thành một tế bào giống hệt với tế bào gốc ban đầu và một tế bào con khác biệt. Khi tế bào gốc tự tái tạo, nó phân chia và không làm gián đoạn trạng thái không biệt hoá. Sự tự đổi mới này phụ thuộc vào sự kiểm soát chặt chẽ của chu kỳ tế bào cũng như duy trì tính đa năng của tế bào gốc.[7]
- Cơ chế biệt hóa ngẫu nhiên (Stochastic differentiation): khi một tế bào gốc phát triển thành hai tế bào con khác biệt, một trong hai tế bào đó phải chịu sự phân bào và tạo ra hai tế bào gốc giống hệt như tế bào lúc đầu.
Tiềm năng
[sửa | sửa mã nguồn]
Tiềm năng (potency) là khả năng biệt hoá tế bào của tế bào gốc.[8]
Totipotent: tế bào gốc totipotent được tạo ra từ một noãn và tinh trùng.[8] Các tế bào totipotent có khả năng biệt hoá thành các dạng tế bào phôi và ngoài phôi.[9]
Pruripotent: tế bào gốc pruripotent là hậu duệ của tế bào gốc totipotent và có khả năng biệt hoá thành các tế bào phát xuất từ bất kỳ lớp mầm nào trong 3 lớp mầm Endoderm, Mesoderm và Ectoderm.[8][10]
Multipotent: tế bào gốc multipotent có khả năng tạo ra duy nhất các tế bào cùng họ với tế bào đó (thí dụ như tế bào gốc tạo máu thì có khả năng biệt hoá thành hồng cầu, bạch cầu, tiểu cầu...) [8]
Oligopotent: Tế bào gốc Oligopotent có thể phân biệt thành một số loại tế bào, chẳng hạn như các tế bào gốc lymphoid hoặc tủy xương.
Unipotent: tế bào gốc unipotent có khả năng tạo ra duy nhất một loại tế bào nhưng vẫn có tính chất tự làm mới, đây là điểm để phân biệt với tế bào không phải tế bào gốc (thí dụ: tế bào gốc cơ).[8]
Nhận biết
[sửa | sửa mã nguồn]Trong thực tế, tế bào gốc được nhận biết bởi khả năng tự làm mới của nó. ví dụ như trường hợp xét nghiệm xác định khả năng cấy ghép của tủy xương hoặc tế bào gốc tạo máu (hematopoietic stem cell) để chữa trị cho bệnh nhân thiếu tế bào gốc tạo máu. Điều này chỉ ra rằng các tế bào có khả năng sản sinh ra tế bào máu trong một thời gian dài. Điều đó cũng cho thấy việc tách chiết các tế bào gốc từ các cá thể đã được cấy ghép, có thể được cấy ghép tiếp cho những bệnh nhân khác không có tế bào gốc tạo máu.
Đặc tính của tế bào gốc có thể được phân biệt trong thí nghiệm in vitro, bằng việc sử dụng các phương pháp như các xét nghiệm sinh học (clonogenic assays) để đánh giá khả năng biệt hoá và tự tái tạo.[11][12] Tế bào gốc có thể được tách chiết từ chính các dấu hiệu đặc biệt trên bề mặt tế bào. Tuy nhiên trong điều kiện nuôi cấy in vitro có thể thay đổi biểu hiện của tế bào, điều này gây khó khăn trong việc xác định biểu hiện của tế bào in vivo. Hiện tại các cuộc tranh luận về việc đề xuất một số tế bào trưởng thành là tế bào gốc.
Phân loại tế bào gốc
[sửa | sửa mã nguồn]Tế bào gốc phôi thai (Embryonic stem cells)
[sửa | sửa mã nguồn]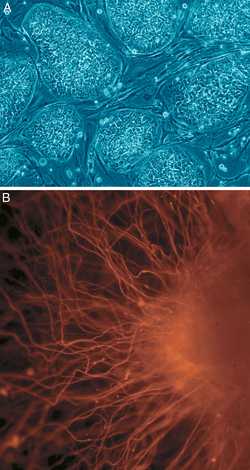
Tế bào phôi (ES) là tế bào của khối lượng tế bào bên trong của phôi nang, phôi giai đoạn đầu.[13] Phôi người đạt đến giai đoạn phôi nang giai đoạn 4-5 ngày sau khi thụ tinh, vào thời điểm đó chúng chứa 50-150 tế bào. Các tế bào ES là dạng tế bào vạn năng pluripotent và biệt hoá cũng như phát triển thành tất cả các tế bào chuyên biệt của ba lớp mầm sơ cấp: ectoderm, endoderm và Mesoderm. Nói cách khác, chúng có thể phát triển thành từng loại tế bào trong hơn 200 loại ở cơ thể người trưởng thành. Chúng không đóng góp vào màng phôi ngoài hoặc nhau thai.
Trong quá trình hình thành và phát triển phôi thai, khối lượng tế bào trong phôi được liên tục nhân lên về số lượng và trở nên chuyên biệt về đặc tính. Ví dụ như một phần ngoại bì (ectoderm) của phôi sẽ biệt hoá thành "neurecderm"- sẽ trở thành hệ thần kinh trung ương (Central Nervous System) trong tương lai.[14] Sau đó, quá trình tạo tế bào thần kinh sẽ hình thành các dây thần kinh từ neurectoderm. Ở giai đoạn tạo dây thần kinh, một phần tế bào tiền thân sẽ trở thành "tế bào máu" của não. Trong quá trình phát triển này, các tế bào chính của hệ thần kinh trung ương được coi như là tế bào gốc thần kinh. Các tế bào gốc thần kinh này là những tế bào đa năng pluripotent, chúng có thể tạo thành rất nhiều dạng neuron thần kinh khác nhau, mỗi loại sẽ có những biểu hiện gene cũng như hình thái và cấu trúc chức năng riêng biệt. Quá trình hình thành các neuron thần kinh từ tế bào gốc được gọi là neurogenesis. Một ví dụ điển hình của tế bào gốc thần kinh xuyên tâm (radial glial cell), loại tế bào có hình thái lưỡng cực đặc trưng cũng như sở hữu các tính chất của dòng tế bào glial, đáng chú ý nhất là biểu hiện của glial fibrilary acidic protein (GFAP).[15][16] Các tế bào thần kinh sẽ được giới hạn biệt hoá chỉ thành các dòng tế bào thần kinh (neurons, atrocytes và oligodendrocytes).[14]
Gần như tất cả các nghiên cứu cho đến nay đều sử dụng tế bào phôi thai chuột (mES) hoặc tế bào phôi thai người (hES) được lấy từ khối lượng tế bào bên trong phôi nang. Cả hai đều có các tính chất thiết yếu của tế bào gốc, tuy rằng chúng vẫn cần các điều kiện môi trường rất khác nhau để duy trì trạng thái không biệt hoá. Tế bào gốc của chuột được nuôi cấy trên một lớp thạch gelatin bao gồm cả yếu tố ức chế bạch cầu (Leukemia Inhibitory Factor) trong serum. Một hỗn hợp bao gồm các chất gây ức chế đối với GSK3B và đường truyền tín hiệu MAPK/ERK (được gọi là 2i), được biết đến có khả năng duy trì tính đa năng của tế bào gốc.[17] Các tế bào gốc của người được nuôi cấy trên một lớp nguyên bào sợi phôi của chuột (MEFs) và cần sự có mặt của yếu tố tăng trưởng nguyên bào sợi cơ bản (bFGF hoặc FGF-2).[18] Nếu không có điều kiện nuôi cấy tối ưu hoặc thao tác di truyền phù hợp, tế bào gốc phôi sẽ nhanh chóng biệt hoá.[19]
Tế bào gốc phôi thai của người được định nghĩa bởi sự biểu hiện của rất nhiều các yếu tố phiên mã và các protein bề mặt tế bào. Các yếu tố phiên mã như Oct-4, Nanog và Sox2 là mạng lưới điều hoà cốt lõi để đảm bảo sự biểu hiện của gene trong quá trình biệt hoá hay duy trì tính đa năng.[20] Bề mặt tế bào kháng nguyên được sử dụng phổ biến nhất để xác định các tế bào gốc phôi người là kháng nguyên glycolipids 3 và 4, cũng như các kháng nguyên keratan sunfat Tra-1-60 và Tra-1-81. Bằng cách sử dụng tế bào gốc phôi người để tạo ra các tế bào đã biệt hoá như tế bào thần kinh hoặc các tế bào tim trong phòng thí nghiệm, các nhà khoa học có thể tiếp cận các tế bào gốc trưởng thành (Adult stem cell) mà không cần lấy mô từ bệnh nhân. Sau đó, họ có thể nghiên cứu những tế bào trưởng thành đã biệt hoá này để thử và nắm bắt các biến chứng của bệnh tật, hoặc để nghiên cứu tế bào phản ứng với các thuốc mới tiềm ẩn. Định nghĩa phân tử của một tế bào gốc còn bao gồm nhiều loại protein hơn và vẫn tiếp tục là một chủ đề nghiên cứu.[21]
Hiện tại không có phương pháp điều trị nào sử dụng tế bào gốc phôi được chấp nhận. Thử nghiệm trên người được phê duyệt lần đầu tiên bởi Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ vào tháng 1 năm 2009.[22] Tuy nhiên, cuộc thử nghiệm trên người đã không được bắt đầu cho đến ngày 13 tháng 10 năm 2010 tại Atlanta để nghiên cứu tổn thương tủy sống. Vào ngày 14 tháng 11 năm 2011, công ty tiến hành thử nghiệm (Geron Corporation) đã thông báo ngừng phát triển các chương trình thí nghiệm tế bào gốc của họ.[23] Các tế bào gốc phôi nang (ES), là những tế bào đa năng, đòi hỏi các tín hiệu cụ thể để biệt hoá chính xác - nếu tiêm trực tiếp vào cơ thể khác, các tế bào ES sẽ biệt hoá thành nhiều loại tế bào khác nhau, gây ra một khối u ác tính. Việc biệt hoá các tế bào ES thành các tế bào có thể sử dụng được trong khi vẫn tránh được việc thải loại cấy ghép (transplant rejection) chỉ là một trong vài rào cản mà các nhà nghiên cứu phải đối mặt.[24] Do các lý do về đạo đức, nhiều quốc gia hiện đang có những hạn chế về nghiên cứu tế bào ES ở người hoặc sản xuất những dòng tế bào ES mới. Do khả năng tái tạo không giới hạn và tính đa năng, các tế bào gốc phôi vẫn là nguồn tiềm năng về mặt lý thuyết đối với y học trong việc tái tạo và thay thế mô bị tổn thương hoặc bệnh tật.[25]
Dòng tế bào gốc phôi thai được nuôi cấy từ các tế bào dẫn xuất từ mô ngoại phôi bì (epiblast) của khối lượng tế bào bên trong của một túi phôi. Túi phôi là giai đoạn sớm nhất của phôi, hình thành từ khoảng 4-5 ngày, và chứa khoảng từ 50-150 tế bào. Tế bào gốc phôi thai thuộc loại pruripotent và suốt quá trình phát triển có khả năng biệt hoá từ một trong 2 lớp phôi: ngoại bì (ectoderm), nội bì (endoderm) và trung bì (mesoderm). Ngoài ra, tế bào gốc phôi thai còn có thể phát triển thành một trong hơn 200 dạng tế bào của cơ thể trường thành nếu được kích thích đầy đủ và cần thiết. Chúng không can dự vào màng ngoài phôi hoặc nhau.
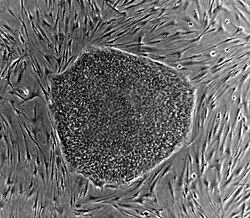
Tế bào gốc phôi thai ở người còn được xác định bằng sự hiện diện của nhiều yếu tố sao chép và protein bề mặt tế bào. Các yếu tố sao chép như Oct-4, Nanog và SOX2 tạo thành mạng điều hoà nhân, đảm bảo cho việc tiêu diệt các gen dẫn đến sự biệt hoá và duy trì tính chất pluripotent. Kháng nguyên bề mặt tế bào thường được dùng nhất để xác định tế bào gốc phôi thai là glycolipid SSEA3, SSEA4 và antigen sulfat keratan Tra-1-60 và Tra-1-81. Bằng cách sử dụng tế bào gốc phôi người để tạo ra các tế bào biệt hoá như tế bào thần kinh hoặc các tế bào cơ tim trong phòng thí nghiệm, các nhà khoa học có thể tiếp cận các tế bào trưởng thành mà không cần lấy mô từ bệnh nhân. Sau đó, họ có thể nghiên cứu những tế bào trưởng thành đã biệt hoá này để thử nghiệm và nắm bắt các biến chứng của bệnh tật, hoặc để nghiên cứu phản ứng của tế bào với các thuốc tiềm năng mới. Định nghĩa phân tử của một tế bào gốc bao gồm nhiều protein hơn và vẫn đang tiếp tục được nghiên cứu.[21]
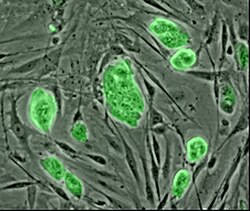
Tế bào gốc bào thai
[sửa | sửa mã nguồn]Các tế bào gốc nguyên thủy nằm trong các cơ quan của bào thai được gọi là tế bào gốc bào thai.[26] Có hai loại tế bào gốc bào thai:
1. Tế bào gốc nguyên thủy từ bào thai (Fetal proper stem cell) xuất phát từ mô của thai nhi, và thường được lấy sau quá trình phá thai. Những tế bào gốc này không phải là bất tử, nhưng có mức độ phân chia cao và đa dạng.
2. Tế bào gốc bào thai ngoài tử cung (Extraembryonic Fetal stem cell) xuất phát từ màng thừa của phôi, và thường không phân biệt với tế bào gốc người lớn. Các tế bào gốc này được thu nhặt sau khi sinh. Mặc dù các tế bào này không phải bất tử, nhưng là tế bào đa năng pluripotent và có mức độ phân chia tế bào cao.[27]
Tế bào gốc trưởng thành - Adult stem cell
[sửa | sửa mã nguồn]
Tế bào gốc trưởng thành (Adult stem cell), còn được gọi là tế bào gốc sinh dưỡng (somatic), là tế bào gốc duy trì và sửa chữa các mô bị tổn thương.[28] Chúng có thể được tìm thấy ở trẻ em, cũng như người lớn.[29]
Các tế bào gốc người trưởng thành đa số hiếm và nói chung là nhỏ về số lượng, nhưng chúng có thể được tìm thấy ở trong máu dây rốn và ở các mô khác.[30] Tủy xương là nơi bao gồm phong phú các tế bào gốc trưởng thành [31], đã được sử dụng trong điều trị một số bệnh bao gồm xơ gan [32], thiếu máu cục bộ mạn tính [33] và suy tim giai đoạn cuối.[34] Số lượng tế bào gốc tủy xương giảm theo tuổi và lớn hơn ở nam giới so với nữ giới trong những năm sinh đẻ.[35] Hầu hết mọi nghiên cứu về tế bào gốc trưởng thành cho đến nay đều nhằm mục đích nắm bắt được tính tiềm năng (potency) và năng lực tự làm mới (self-renewal) của chúng.[36] Theo thời gian, các thương tổn DNA sẽ được tích tụ ở tế bào gốc và cả các tế bào khác ở môi trường bao quanh tế bào gốc. Sự tích tụ này lý giải cho sự rối loạn chức năng của tế bào gốc khi lão hóa (xem lý thuyết về sự lão hóa của DNA).[37]
Hầu hết các tế bào gốc người lớn đều bị hạn chế về khả năng biệt hoá (chúng là dạng tế bào multipotent) [38] và thường được gọi bởi nguồn gốc mô của chúng (tế bào gốc trung mô, tế bào gốc có nguồn gốc từ mỡ, tế bào gốc nội mô...).[39] Các tế bào Muse (multi-lineage differentiating stress enduring cells) là một loại tế bào gốc đa năng mới được phát hiện thấy trong các mô người trưởng thành, bao gồm cả chất béo, các nguyên bào sợi da, và tủy xương. Mặc dù các tế bào muse có thể nhận biết được bằng SSEA-3, một dấu hiệu của các tế bào gốc không biệt hoá và các dấu hiệu tế bào gốc trung mô nói chung như CD105. Trong quá trình nuôi cấy, các tế bào sẽ tạo ra những cụm có hình thái giống như các phôi cũng như biểu hiện gen, bao gồm các dấu hiệu nhận biết như Oct4, Sox2, và Nanog.[40]
Các phương pháp điều trị bằng tế bào gốc người trưởng thành đã được sử dụng thành công trong nhiều năm để điều trị bệnh bạch cầu và ung thư xương / máu liên quan đến việc cấy ghép tủy xương.[41] Các tế bào gốc người trưởng thành cũng được sử dụng trong ngành thú y để điều trị chấn thương dây chằng và dây chằng ở ngựa.[42]
Việc sử dụng các tế bào gốc người lớn trong nghiên cứu và điều trị không gây tranh cãi như việc sử dụng các tế bào gốc phôi vì sản xuất các tế bào gốc người trưởng thành không đòi hỏi phá huỷ phôi. Ngoài ra, trong những trường hợp tế bào người trưởng thành được thu nhận từ cùng cơ thể (một phương pháp tự ghép), nguy cơ thải loại sẽ không tồn tại. Do đó chính phủ Hoa Kỳ đang đầu tư rất nhiều vốn để cung cấp tài trợ cho nghiên cứu tế bào gốc người trưởng thành.[43]
Tế bào gốc dịch màng ối (Amniotic)
[sửa | sửa mã nguồn]Các tế bào gốc đa năng cũng được tìm thấy trong dịch màng ối. Các tế bào gốc này rất hoạt hoá, có khả năng di chuyển rộng mà không cần nguồn dinh dưỡng, đặc biệt là không gây khối u. Tế bào gốc buồng ối là tế bào đa năng multipotent và có khả năng biệt hoá thành các dòng tế bào của các tuyến adipogenic, osteogenic, myogenic, endothelial, hepatic và nơ-ron thần kinh.[44] Tế bào gốc buồng ối hiện đang và sẽ là một chủ đề nghiên cứu rất hứa hẹn.
Sử dụng các tế bào gốc từ nước ối không còn mắc phải các phản đối về mặt đạo đức đối với việc sử dụng phôi người cho nghiên cứu. Giáo huấn Công giáo Rôma đã cấm việc sử dụng tế bào gốc phôi thai trong thử nghiệm; theo đó, tờ Vatican "Osservatore Romano" gọi là tế bào gốc buồng ối "tương lai của y học".[45]
Có thể thu thập các tế bào gốc nước ối cho các nhà tài trợ hoặc cho điều trị tự trị: ngân hàng tế bào gốc ối Hoa Kỳ đầu tiên [46][47] được khai trương vào năm 2009 tại Medford, MA bởi Tập đoàn Biocell Center [48][49][50] và cộng tác với nhiều bệnh viện và các trường đại học trên khắp thế giới.[51]
Tế bào gốc "vạn năng cảm ứng" (Induced Pluripotent Stem Cells- iPSC)
[sửa | sửa mã nguồn]Tế bào gốc người lớn có những hạn chế về mặt tiềm năng; không giống như ESCs, chúng không thể phân biệt thành các tế bào từ cả ba lớp mầm. Như vậy, chúng được cho là tế bào đa năng multipotent.
Tuy nhiên, việc lập trình lại cho phép tạo ra các tế bào vạn năng pluripotent từ tế bào người trưởng thành. Điều quan trọng cần lưu ý rằng đây không phải là các tế bào gốc người trưởng thành, mà là các tế bào đã biệt hoá (ví dụ như tế bào biểu mô) được lập trình lại để làm phát sinh khả năng đa năng pluripotent của tế bào. Sử dụng tái lập trình di truyền (genetic reprogramming) với các protein phiên mã, các tế bào gốc đa năng với khả năng tương ứng tế bào gốc phôi ESC được tạo thành.[52][53][54] Các tế bào gốc iPSC lần đầu tiên được nghiên cứu và thử nghiệm thành công bởi Shinya Yamanaka và các đồng nghiệp của ông tại Đại học Kyoto.[55] Họ sử dụng 4 yếu tố phiên mã Oct3 / 4, Sox2, c-Myc, và Klf4 để tái lập trình các tế bào nguyên bào sợi chuột thành các tế bào vạn năng pluripotent.[52][56] Các nghiên cứu tiếp theo sử dụng những yếu tố này để tạo ra sự đa năng trong tế bào nguyên bào sợi người.[57] Junying Yu, James Thomson, và các đồng nghiệp của họ tại Đại học Wisconsin-Madison đã sử dụng một bộ các nhân tố khác nhau, bao gồm Oct4, Sox2, Nanog và Lin28, và thực hiện các thí nghiệm của họ bằng cách sử dụng các tế bào từ da người [49] [55]. Việc họ đã có thể lặp lại kết quả của Yamanaka chỉ ra rằng sự tạo tế bào gốc vạn năng pluripotency là hoàn toàn có thể.[58]
Điều quan trọng cần lưu ý là iPSC và ESCs không tương đương. Chúng có nhiều tính chất tương tự, ví dụ như tính đa năng và khả năng biệt hoá, sự biểu hiện của gen đa năng, mô hình biểu sinh (epigenetic patterns), cơ thể phôi và quá trình hình thành teratoma và sự hình thành chimer.[55][56] Tuy nhiên, tương tự không có nghĩa là chúng như nhau. Trong thực tế, có rất nhiều sự khác biệt giữa các thuộc tính này. Điều quan trọng là chromatin của iPSC dường như bị "đóng" hoặc bị methyl hóa hơn so với các ESCs.[55][56] Tương tự, mô hình biểu hiện gen giữa ESCs và iPSCs, hoặc thậm chí cả iPSCs đều có nguồn gốc khác nhau.[55] Có những câu hỏi về "sự hoàn chỉnh" của việc lập trình lại các tế bào gốc đa năng iPSC. Mặc dù vậy, việc biến tế bào người trưởng thành thành tế bào vạn năng pluripotent là khả thi.
Kết quả của sự thành công của những thí nghiệm này, Ian Wilmut, người đã giúp tạo ra động vật nhân bản đầu tiên - Chú cừu Dolly, đã tuyên bố rằng ông sẽ từ bỏ việc chuyển hạt nhân tế bào soma.[59]
Hơn nữa, các tế bào gốc iPSC mang lại nhiều ưu điểm trong điều trị. Giống như ESC, iPSC đều là những tế bào vạn năng pluripotent. Do đó chúng có khả năng biệt hoá rất cao; Về mặt lý thuyết, chúng có thể tạo ra bất kỳ tế bào nào trong cơ thể con người (nếu tế bào iPSC được tạo ra một cách "hoàn chỉnh").[55] Hơn nữa, không giống như ESCs, họ có khả năng cho phép các bác sĩ tạo ra một dòng tế bào gốc đa năng pluripotent cho từng bệnh nhân.[60] Trên thực tế, các mẫu máu đông lạnh có thể được sử dụng như một nguồn cung cấp tế bào gốc đa năng pluripotent, mở ra một con đường mới cho việc thu hoạch các tế bào có giá trị.[61] Các tế bào gốc đặc hiệu cho bệnh nhân cho phép sàng lọc các tác dụng phụ trước khi điều trị bằng thuốc, cũng như giảm nguy cơ thải loại trong cấy ghép tế bào.[60] Mặc dù vẫn còn nhiều hạn chế trong điều trị, việc sử dụng iPSCs trong điều trị y tế và nghiên cứu vẫn rất tiềm năng trong tương lai.
Ngoài ra, tế bào gốc còn có thể chia ra thành tế bào gốc nội sinh và ngoại sinh. Tế bào gốc nội sinh là các tế bào gốc có sẵn trong cơ thể chúng ta. Tế bào gốc ngoại sinh là các tế bào gốc được lấy ra từ cơ thể người cho, sau đó được sử dụng các phương pháp để tăng sinh trong phòng thí nghiệm, rồi được cấy ghép trở lại cơ thể người bệnh – phương pháp này còn được gọi là liệu pháp cấy ghép tế bào gốc ngoại sinh.
Dòng tế bào gốc
[sửa | sửa mã nguồn]Để đảm bảo tính năng tự đổi mới, tế bào gốc phải trải qua hai loại phân chia tế bào (xem phân chia tế bào gốc và sơ đồ biệt hoá). Sự phân chia đối xứng tạo ra hai tế bào con giống hệt nhau, cả hai đều có đặc tính tế bào gốc. Mặt khác phân chia bất đối xứng chỉ tạo ra một tế bào gốc và một tế bào tiền thân progenitor có tiềm năng tự đổi mới. Các tế bào progenitor có thể đi qua nhiều vòng phân chia tế bào trước khi biệt hoá thành một tế bào trưởng thành. Các phân tử phụ trách cho phân chia đối xứng và bất đối xứng có thể nằm trong phân tách khác nhau của các protein màng tế bào (như thụ thể) giữa các tế bào con.[62]
Một lý thuyết khác là các tế bào gốc vẫn không phân biệt do các tín hiệu môi trường riêng biệt (niche) của chúng. Các tế bào gốc biệt hoá khi họ rời khỏi môi trường đó hoặc không còn nhận được những tín hiệu đó. Các nghiên cứu trên Drosophila đã xác định được các dấu hiệu cắt decapentaplegic và adherens junctions ngăn ngừa tế bào gốc germarium khỏi việc biệt hoá.[63][64]
Điều trị
[sửa | sửa mã nguồn]Bài chi tiết: Liệu pháp tế bào gốc
Liệu pháp tế bào gốc là việc sử dụng tế bào gốc trong điều trị hoặc ngăn ngừa bệnh. Cấy ghép tủy xương là một hình thức liệu pháp tế bào gốc đã được sử dụng trong nhiều năm mà không có bất kỳ tranh cãi nào. Không có liệu pháp tế bào gốc nào ngoài ghép tủy xương được sử dụng rộng rãi.[65][66]
Ưu điểm
[sửa | sửa mã nguồn]Điều trị bằng tế bào gốc có thể làm giảm các triệu chứng và tình trạng của bệnh. Việc làm giảm các triệu chứng có thể cho phép bệnh nhân giảm lượng thuốc trong việc điều trị bệnh. Điều trị bằng tế bào gốc cung cấp kiến thức và hiểu biết về tế bào và mở ra các hướng điều trị mới trong tương lai.[67]
Nhược điểm
[sửa | sửa mã nguồn]Việc điều trị tế bào gốc có thể cần đến sự ức chế miễn dịch do cần chiếu xạ (radiation) trước khi cấy ghép để loại bỏ các tế bào trước đó của bệnh nhân, hoặc bởi vì hệ thống miễn dịch của bệnh nhân có thể tấn công các tế bào gốc. Một cách tiếp cận để tránh thải loại cấy ghép là sử dụng các tế bào gốc từ chính bệnh nhân đang được điều trị.[cần dẫn nguồn]
Tính đa năng trong các tế bào gốc cũng gây khó khăn trong việc biệt hoá thành một loại tế bào cụ thể. Cũng rất khó để thu được chính xác loại tế bào cần thiết sau quá trình biệt hoá, bởi vì không phải tất cả các tế bào trong một quần thể đều biệt hoá một cách thống nhất. Các tế bào không biệt hoá có thể tạo các mô mà không phải tạo thành các loại tế bào mong muốn.[67]
Một số tế bào gốc hình thành các khối u sau khi cấy,[68] sự đa năng có liên quan đến sự hình thành khối u; đặc biệt trong tế bào gốc phôi thai, tế bào gốc bào thai, các tế bào gốc đa năng iPS. Các tế bào gốc bào thai tạo thành các khối u mặc dù có tính đa năng multipotency.[69]
Nghiên cứu
[sửa | sửa mã nguồn]Một số bằng sáng chế cơ bản bao gồm các tế bào gốc phôi người thuộc sở hữu của Tổ chức nghiên cứu Wisconsin (WARF) - họ được cấp bằng sáng chế 5,843,780, 6,200,806 và 7,029,913 phát minh bởi James A. Thomson. WARF không sử dụng các bằng sáng chế này trong thương mại hoá với các công ty mà sử dụng chúng trong môi trường nghiên cứu học thuật.[70]
Năm 2006, Tổ chức Sáng chế Công cộng (USPTO) đã yêu cầu Văn phòng Sáng chế và Nhãn hiệu Hoa Kỳ (USPTO) xem xét lại ba bằng sáng chế thay mặt cho khách hàng của mình, tổ chức giám sát bằng sáng chế phi lợi nhuận Consumer Watchdog (trước đây là Hiệp hội người nộp thuế và quyền lợi người tiêu dùng).[70] Trong quá trình kiểm tra lại, trong đó có một vài cuộc thảo luận giữa USPTO và các bên, USPTO ban đầu đã đồng ý với Consumer Watchdog và từ chối tất cả các yêu cầu trong cả ba bằng sáng chế.[71] Tuy nhiên đáp lại, WARF đã sửa đổi các tuyên bố của tất cả ba bằng sáng chế để làm cho chúng trở nên cụ thể hơn. Trong năm 2008, USPTO đã phát hiện ra các yêu cầu sửa đổi trong cả ba bằng sáng chế có thể được cấp bằng sáng chế. Quyết định về một trong các bằng sáng chế (7,029,913) đã được kháng cáo, trong khi vẫn giữ nguyên quyết định cho 2 bằng sáng chế còn lại.[72][73] Consumer Watchdog đã kêu gọi việc cấp bằng sáng chế 913 cho Ủy ban Kháng nghị và Tội nhiễu (BPAI) của USPTO đã đưa ra lời kêu gọi, và trong năm 2010 BPAI đã quyết định rằng các yêu cầu sửa đổi của "bằng sáng chế 913 không được cấp bằng sáng chế".[74] Tuy nhiên, WARF đã có thể mở lại việc truy tố vụ án và đã làm như vậy, thay đổi các yêu cầu của bằng sáng chế 931 một lần nữa cho cụ thể hơn, và vào tháng 1 năm 2013 các tuyên bố sửa đổi đã được cho phép.[75]
Vào tháng 7 năm 2013, Consumer Watchdog đã thông báo rằng họ sẽ kháng cáo quyết định cho phép các khiếu nại của bằng sáng chế 913 cho Toà án Kháng cáo Hoa Kỳ cho Circuit liên bang (CAFC), tòa phúc thẩm liên bang nghe các vụ kiện bằng sáng chế.[76] Tại buổi điều trần vào tháng 12 năm 2013, CAFC đã đưa ra câu hỏi liệu Consumer Watchdog có quyền kháng cáo hay không; vụ án không thể tiến hành cho đến khi vấn đề đó được giải quyết.[77]
Điều trị
[sửa | sửa mã nguồn]
Bệnh đã và đang được điều trị bằng tế bào gốc bao gồm:
- Tiểu đường [78]
- Rheumatoid viêm khớp [78]
- Bệnh Parkinson [78]
- Bệnh Alzheimer [78]
- Viêm xương khớp [78]
- Tai biến mạch máu não và chấn thương sọ não [79]
- Khuyết tật do rối loạn bẩm sinh [80]
- Tổn thương tủy sống [81]
- Nhồi máu cơ tim [82]
- Điều trị chống ung thư [83]
- Hói [84]
- Thay thế răng bị mất [85]
- Hạn chế thính giác [86]
- Phục hồi thị lực [87] và sửa chữa hư hỏng cho giác mạc [88]
- Xơ cứng động mạch [89]
- Bệnh Crohn [90]
- Điều trị vết thương [91]
- Sự vô sinh do thiếu tế bào gốc tinh trùng [92]
Nghiên cứu đang được tiến hành để phát triển các nguồn khác nhau cho tế bào gốc, và áp dụng các phương pháp điều trị tế bào gốc cho các bệnh và điều kiện thoái hoá thần kinh, tiểu đường, bệnh tim và các điều kiện khác.[93] Nghiên cứu cũng đang được tiến hành trong việc tạo ra các organoids bằng việc sử dụng các tế bào gốc, điều này sẽ giúp hiểu rõ hơn về sự phát triển của con người, sự hình thành cơ thể và mô hình hóa các bệnh của con người.[94]
Trong những năm gần đây, sự phát triển của khoa học đã thành công trong việc cô lập và tạo ra các tế bào gốc phôi thai, cũng như việc tạo ra các tế bào gốc bằng cách chuyển nhân tế bào soma hay các kỹ thuật tạo ra các tế bào gốc iPS. Điều này gây ra các cuộc tranh luận xung quanh vấn đề phá thai, chính trị và nhân bản con người.
Nhiễm độc gan và tổn thương gan gây ra do thuốc là nguyên nhân chiếm số lượng đáng kể trong các thất bại của việc thử nghiệm thuốc mới. Điều này làm nổi bật sự cần thiết của việc sử dụng tế bào gốc để biệt hoá thành các tế bào gan có khả năng phát hiện độc tính sớm trong quá trình phát triển thuốc.[95]
Lịch sử
[sửa | sửa mã nguồn]- Từ những năm 1950, các nhà khoa học nước ngoài đã phát hiện ra các kháng nguyên trên màng tế bào và kháng thể cơ thể.
- Năm 1994, Ariff Bongso, Nhà khoa học người Sri Lanka, là người đầu tiên trên thế giới tách thành công tế bào gốc (TBG) từ phôi người. Sau đó, rất nhiều Nhà khoa học nổi tiếng khác tiếp tục nghiên cứu và đã có nhiều thành tựu quan trọng trong việc sử dụng TBG nhằm điều trị, chăm sóc sức khỏe con người. Cần nói thêm trong lịch sử nghiên cứu TBG, việc tách TBG từ gốc phôi hoặc nhũ nhi (thai) có thời gian từng bị lên án dữ dội từ dư luận xã hội và tín ngưỡng tôn giáo phương Tây, về việc vi phạm vấn đề y đức. TBG trưởng thành cũng ít được quan tâm bởi khả năng cho tế bào ít, già và khó biệt hóa...
- Đến năm 2004, tại trường ĐH Quốc gia Singapore, bác sĩ Phan Toàn Thắng là người đầu tiên trên thế giới tách được tế bào gốc từ màng cuống dây rốn, một phát minh đã tạo nên sự quan tâm đặc biệt của giới khoa học thế giới. Đây là tiền đề quan trọng để có thể chữa lành các vết thương do bỏng, loét do phóng xạ và đặc biệt là ứng dụng trong lĩnh vực chăm sóc sắc đẹp.
Tính xác thực của ứng dụng tế bào gốc từ dây rốn
[sửa | sửa mã nguồn]Ngày 20 tháng 2 năm 2010, phát biểu tại hội nghị thường niên Hiệp hội vì sự tiến bộ của khoa học Mỹ (AAAS), Irving Weissman, Giám đốc Viện Y học phục hồi và tế bào gốc sinh học, thuộc trường Đại học Stanford ở California, Mỹ[96] cho biết dây rốn chứa các tế bào gốc có thể duy trì khả năng tạo máu ở mức độ chỉ cho trẻ nhỏ. Tuy nhiên, "khả năng chữa bệnh chưa hề được chứng minh" Lưu trữ ngày 29 tháng 6 năm 2012 tại Wayback Machine của các tế bào gốc lại đang rất thịnh hành ở nhiều nước có quy định lỏng lẻo trong ngành y. Ông Weissman cho rằng các bệnh viện tư đang "kiếm tiền" từ những người tin vào khả năng kỳ diệu của tế bào gốc lấy từ dây rốn.[97]
Tham khảo
[sửa | sửa mã nguồn]- ^ "Stem cells: Sources, types, and uses". Truy cập ngày 7 tháng 9 năm 2024.
- ^ "Types of Stem Cells".
- ^ "Ryan P. Coughlin et al: 'Adipose-Derived Stem Cell Transplant Technique for Degenerative Joint Disease'".
- ^ Tuch BE (2006). "Stem cells – a clinical update". Australian Family Physician. 35 (9): 719–21. PMID 16969445
- ^ Becker AJ, McCulloch EA, Till JE (1963). "Cytological demonstration of the clonal nature of spleen colonies derived from transplanted mouse marrow cells". Nature. 197 (4866): 452–54. Bibcode:1963Natur.197..452B. doi:10.1038/197452a0. PMID 13970094.
- ^ Siminovitch L, Mcculloch EA, Till JE (1963). "The distribution of colony-forming cells among spleen colonies". Journal of Cellular and Comparative Physiology. 62 (3): 327–36. doi:10.1002/jcp.1030620313. PMID 14086156.
- ^ Shenghui, H. E., Nakada, D., & Morrison, S. J. (2009). Mechanisms of stem cell self-renewal. Annual Review of Cell and Developmental, 25, 377-406.
- ^ a b c d e Schöler, Hans R. (2007). "The Potential of Stem Cells<: An Inventory". In Nikolaus Knoepffler; Dagmar Schipanski; Stefan Lorenz Sorgner. Humanbiotechnology as Social Challenge. Ashgate Publishing. p. 28. ISBN 978-0-7546-5755-2.
- ^ Mitalipov S, Wolf D (2009). "Totipotency, pluripotency and nuclear reprogramming". Adv. Biochem. Eng. Biotechnol. Advances in Biochemical Engineering/Biotechnology. 114: 185–99. Bibcode:2009esc..book..185M. doi:10.1007/10_2008_45. ISBN 978-3-540-88805-5. PMC 2752493. PMID 19343304.
- ^ Ulloa-Montoya F, Verfaillie CM, Hu WS (2005). "Culture systems for pluripotent stem cells". J Biosci Bioeng. 100 (1): 12–27. doi:10.1263/jbb.100.12. PMID 16233846.
- ^ Friedenstein AJ, Deriglasova UF, Kulagina NN, Panasuk AF, Rudakowa SF, Luriá EA, Ruadkow IA (1974). "Precursors for fibroblasts in different populations of hematopoietic cells as detected by the in vitro colony assay method". Experimental Hematology. 2 (2): 83–92. ISSN 0301-472X. PMID 4455512.
- ^ Friedenstein AJ, Gorskaja JF, Kulagina NN (1976). "Fibroblast precursors in normal and irradiated mouse hematopoietic organs". Experimental Hematology. 4 (5): 267–74. PMID 976387.
- ^ Thomson JA, Itskovitz-Eldor J, Shapiro SS, Waknitz MA, Swiergiel JJ, Marshall VS, Jones JM (1998). "Blastocysts Embryonic Stem Cell Lines Derived from Human". Science. 282 (5391): 1145–47. Bibcode:1998Sci...282.1145T. doi:10.1126/science.282.5391.1145. PMID 9804556.
- ^ a b Gilbert, Scott F.; College, Swarthmore; Helsinki, the University of (2014). Developmental biology (Tenth ed.). Sunderland, Mass.: Sinauer. ISBN 978-0878939787.
- ^ Rakic, P (October 2009). "Evolution of the neocortex: a perspective from developmental biology". Nature Reviews. Neuroscience. 10 (10): 724–35. doi:10.1038/nrn2719. PMC 2913577. PMID 19763105.
- ^ Noctor, SC; Flint, AC; Weissman, TA; Dammerman, RS; Kriegstein, AR (ngày 8 tháng 2 năm 2001). "Neurons derived from radial glial cells establish radial units in neocortex". Nature. 409 (6821): 714–20. doi:10.1038/35055553. PMID 11217860.
- ^ Ying, Q. L.; Wray, J; Nichols, J; Batlle-Morera, L; Doble, B; Woodgett, J; Cohen, P; Smith, A (2008). "The ground state of embryonic stem cell self-renewal". Nature. 453 (7194): 519–23. doi:10.1038/nature06968. PMC 5328678. PMID 18497825.
- ^ "Culture of Human Embryonic Stem Cells (hESC)". National Institutes of Health. Archived from the original on 2010-01-06. Truy cập 2010-03-07.
- ^ Chambers I, Colby D, Robertson M, Nichols J, Lee S, Tweedie S, Smith A (2003). "Functional expression cloning of Nanog, a pluripotency sustaining factor in embryonic stem cells". Cell. 113 (5): 643–55. doi:10.1016/S0092-8674(03)00392-1. PMID 12787505.
- ^ Boyer LA, Lee TI, Cole MF, Johnstone SE, Levine SS, Zucker JP, Guenther MG, Kumar RM, Murray HL, Jenner RG, Gifford DK, Melton DA, Jaenisch R, Young RA (2005). "Core transcriptional regulatory circuitry in human embryonic stem cells". Cell. 122 (6): 947–56. doi:10.1016/j.cell.2005.08.020. PMC 3006442. PMID 16153702.
- ^ a b Adewumi O, Aflatoonian B, Ahrlund-Richter L, Amit M, Andrews PW, Beighton G, Bello PA, Benvenisty N, Berry LS, Bevan S, Blum B, Brooking J, Chen KG, Choo AB, Churchill GA, Corbel M, Damjanov I, Draper JS, Dvorak P, Emanuelsson K, Fleck RA, Ford A, Gertow K, Gertsenstein M, Gokhale PJ, Hamilton RS, Hampl A, Healy LE, Hovatta O, Hyllner J, Imreh MP, Itskovitz-Eldor J, Jackson J, Johnson JL, Jones M, Kee K, King BL, Knowles BB, Lako M, Lebrin F, Mallon BS, Manning D, Mayshar Y, McKay RD, Michalska AE, Mikkola M, Mileikovsky M, Minger SL, Moore HD, Mummery CL, Nagy A, Nakatsuji N, O'Brien CM, Oh SK, Olsson C, Otonkoski T, Park KY, Passier R, Patel H, Patel M, Pedersen R, Pera MF, Piekarczyk MS, Pera RA, Reubinoff BE, Robins AJ, Rossant J, Rugg-Gunn P, Schulz TC, Semb H, Sherrer ES, Siemen H, Stacey GN, Stojkovic M, Suemori H, Szatkiewicz J, Turetsky T, Tuuri T, van den Brink S, Vintersten K, Vuoristo S, Ward D, Weaver TA, Young LA, Zhang W (2007). "Characterization of human embryonic stem cell lines by the International Stem Cell Initiative". Nat. Biotechnol. 25 (7): 803–16. doi:10.1038/nbt1318. PMID 17572666.
- ^ Ron Winslow (2009). "First Embryonic Stem-Cell Trial Gets Approval from the FDA". The Wall Street Journal. 23. January 2009.
- ^ "Embryonic Stem Cell Therapy At Risk? Geron Ends Clinical Trial". ScienceDebate.com. Truy cập 2011-12-11.
- ^ Wu DC, Boyd AS, Wood KJ (2007). "Embryonic stem cell transplantation: potential applicability in cell replacement therapy and regenerative medicine". Front Biosci. 12 (8–12): 4525–35. doi:10.2741/2407. PMID 17485394.
- ^ Mahla RS (2016). "Stem cells application in regenerative medicine and disease threpeutics". International Journal of Cell Biology. 2016 (7): 19. doi:10.1155/2016/6940283. PMID 27516776.
- ^ Ariff Bongso; Eng Hin Lee, eds. (2005). "Stem cells: their definition, classification and sources". Stem Cells: From Benchtop to Bedside. World Scientific. p. 5. ISBN 981-256-126-9. OCLC 443407924.
- ^ Moore, K.L., T.V.N. Persaud, and A.G. Torchia. Before We Are Born: Essentials of Embryology and Birth Defects. Philadelphia, PA: Saunders, Elsevier. 2013. Print
- ^ "Stem Cells" Mayo Clinic. Mayo foundation for medical education and research n.d Web. ngày 23 tháng 3 năm 2013
- ^ Jiang Y, Jahagirdar BN, Reinhardt RL, Schwartz RE, Keene CD, Ortiz-Gonzalez XR, Reyes M, Lenvik T, Lund T, Blackstad M, Du J, Aldrich S, Lisberg A, Low WC, Largaespada DA, Verfaillie CM (2002). "Pluripotency of mesenchymal stem cells derived from adult marrow". Nature. 418 (6893): 41–9. doi:10.1038/nature00870. PMID 12077603.
- ^ Jump up^ Narasipura SD, Wojciechowski JC, Charles N, Liesveld JL, King MR (2008). "P-Selectin
- ^ Narasipura SD, Wojciechowski JC, Charles N, Liesveld JL, King MR (2008). "P-Selectin coated microtube for enrichment of CD34+ hematopoietic stem and progenitor cells from human bone marrow". Clin Chem. 54 (1): 77–85. doi:10.1373/clinchem.2007.089896. PMID 18024531.
- ^ Terai S, Ishikawa T, Omori K, Aoyama K, Marumoto Y, Urata Y, Yokoyama Y, Uchida K, Yamasaki T, Fujii Y, Okita K, Sakaida I (2006). "Improved liver function in patients with liver cirrhosis after autologous bone marrow cell infusion therapy". Stem Cells. 24 (10): 2292–8. doi:10.1634/stemcells.2005-0542. PMID 16778155.
- ^ Subrammaniyan R, Amalorpavanathan J, Shankar R, et al. (September 2011). "Application of autologous bone marrow mononuclear cells in six patients with advanced chronic critical limb ischemia as a result of diabetes: our experience". Cytotherapy. 13 (8): 993–9. doi:10.3109/14653249.2011.579961. PMID 21671823.
- ^ Madhusankar N. "Use of Bone Marrow derived Stem Cells in Patients with Cardiovascular Disorders". Journal of Stem Cells and Regenerative Medicine.
- ^ Dedeepiya VD, Rao YY, Jayakrishnan GA, Parthiban JK, Baskar S, Manjunath SR, Senthilkumar R, Abraham SJ (2012). "Index of CD34+ Cells and Mononuclear Cells in the Bone Marrow of Spinal Cord Injury Patients of Different Age Groups: A Comparative Analysis". Bone Marrow Res. 2012: 787414. doi:10.1155/2012/787414. PMC 3398573. PMID 22830032.
- ^ Gardner RL (2002). "Stem cells: potency, plasticity and public perception". Journal of Anatomy. 200 (3): 277–82. doi:10.1046/j.1469-7580.2002.00029.x. PMC 1570679. PMID 12033732.
- ^ Behrens A, van Deursen JM, Rudolph KL, Schumacher B (2014). "Impact of genomic damage and ageing on stem cell function". Nat. Cell Biol. 16 (3): 201–7. doi:10.1038/ncb2928. PMC 4214082. PMID 24576896.
- ^ Barrilleaux B, Phinney DG, Prockop DJ, O'Connor KC (2006). "Review: ex vivo engineering of living tissues with adult stem cells". Tissue Eng. 12 (11): 3007–19. doi:10.1089/ten.2006.12.3007. PMID 17518617.
- ^ Gimble JM, Katz AJ, Bunnell BA (2007). "Adipose-derived stem cells for regenerative medicine". Circ Res. 100 (9): 1249–60. doi:10.1161/01.RES.0000265074.83288.09. PMID 17495232.
- ^ Kuroda Y, Kitada M, Wakao S, Nishikawa K, Tanimura Y, Makinoshima H, Goda M, Akashi H, Inutsuka A, Niwa A, Shigemoto T, Nabeshima Y, Nakahata T, Nabeshima Y, Fujiyoshi Y, Dezawa M (2010). "Unique multipotent cells in adult human mesenchymal cell populations". Proc Natl Acad Sci U S A. 107 (19): 8639–43. Bibcode:2010PNAS..107.8639K. doi:10.1073/pnas.0911647107. PMC 2889306. PMID 20421459.
- ^ "Bone Marrow Transplant". ucsfchildrenshospital.org.
- ^ Kane, Ed (2008-05-01). "Stem-cell therapy shows promise for horse soft-tissue injury, disease". DVM Newsmagazine. Truy cập 2008-06-12.
- ^ "Stem Cell FAQ". US Department of Health and Human Services. 2004-07-14. Archived from the original on 2009-01-09.
- ^ De Coppi P, Bartsch G, Siddiqui MM, Xu T, Santos CC, Perin L, Mostoslavsky G, Serre AC, Snyder EY, Yoo JJ, Furth ME, Soker S, Atala A (2007). "Isolation of amniotic stem cell lines with potential for therapy". Nature Biotechnology. 25 (5): 100–106. doi:10.1038/nbt1274. PMID 17206138.
- ^ "Vatican newspaper calls new stem cell source 'future of medicine':: Catholic News Agency (CNA)". Catholic News Agency. 2010-02-03. Truy cập 2010-03-14.
- ^ "European Biotech Company Biocell Center Opens First U.S. Facility for Preservation of Amniotic Stem Cells in Medford, Massachusetts". Reuters. 2009-10-22. Archived from the original on 2009-10-30. Truy cập 2010-03-14.
- ^ "Europe's Biocell Center opens Medford office – Daily Business Update". The Boston Globe. 2009-10-22. Truy cập 2010-03-14.
- ^ "The Ticker". BostonHerald.com. 2009-10-22. Truy cập 2010-03-14.
- ^ "Biocell Center opens amniotic stem cell bank in Medford". Mass High Tech Business News. 2009-10-23. Archived from the original on 2012-10-14. Truy cập 2012-08-26.
- ^ "News » World's First Amniotic Stem Cell Bank Opens In Medford". wbur.org. Truy cập 2010-03-14.
- ^ "Biocell Center Corporation Partners with New England's Largest Community-Based Hospital Network to Offer a Unique... – MEDFORD, Mass., March 8 /PRNewswire/". Massachusetts: Prnewswire.com. Truy cập 2010-03-14.
- ^ a b "Making human embryonic stem cells". The Economist. 2007-11-22.
- ^ Brand, Madeleine; Palca, Joe; Cohen, Alex (2007-11-20). "Skin Cells Can Become Embryonic Stem Cells". National Public Radio.
- ^ "Breakthrough Set to Radically Change Stem Cell Debate". News Hour with Jim Lehrer. 2007-11-20.
- ^ a b c d e Kimbrel, E. A.; Lanza, R (2016). "Pluripotent stem cells: The last 10 years". Regenerative Medicine. 11 (8): 831–847. doi:10.2217/rme-2016-0117. PMID 27908220
- ^ a b c Takahashi, K; Yamanaka, S (2006). "Induction of pluripotent stem cells from mouse embryonic and adult fibroblast cultures by defined factors". Cell. 126 (4): 663–76. doi:10.1016/j.cell.2006.07.024. PMID 16904174.
- ^ Takahashi, K; Tanabe, K; Ohnuki, M; Narita, M; Ichisaka, T; Tomoda, K; Yamanaka, S (2007). "Induction of pluripotent stem cells from adult human fibroblasts by defined factors". Cell. 131 (5): 861–72. doi:10.1016/j.cell.2007.11.019. PMID 18035408.
- ^ Yu, J; Vodyanik, M. A.; Smuga-Otto, K; Antosiewicz-Bourget, J; Frane, J. L.; Tian, S; Nie, J; Jonsdottir, G. A.; Ruotti, V; Stewart, R; Slukvin, I. I.; Thomson, J. A. (2007). "Induced pluripotent stem cell lines derived from human somatic cells". Science. 318 (5858): 1917–20. doi:10.1126/science.1151526. PMID 18029452.
- ^ "His inspiration comes from the research by Prof Shinya Yamanaka at Kyoto University, which suggests a way to create human embryo stem cells without the need for human eggs, which are in extremely short supply, and without the need to create and destroy human cloned embryos, which is bitterly opposed by the pro life movement."
- ^ a b Robinton, D. A.; Daley, G. Q. (2012). "The promise of induced pluripotent stem cells in research and therapy". Nature. 481 (7381): 295–305. doi:10.1038/nature10761. PMC 3652331. PMID 22258608.
- ^ Frozen blood a source of stem cells, study finds. newsdaily.com (2010-07-01)
- ^ Beckmann J, Scheitza S, Wernet P, Fischer JC, Giebel B (2007). "Asymmetric cell division within the human hematopoietic stem and progenitor cell compartment: identification of asymmetrically segregating proteins". Blood. 109 (12): 5494–501. doi:10.1182/blood-2006-11-055921. PMID 17332245.
- ^ Xie T, Spradling AC (1998). "decapentaplegic is essential for the maintenance and division of germline stem cells in the Drosophila ovary". Cell. 94 (2): 251–60. doi:10.1016/S0092-8674(00)81424-5. PMID 9695953.
- ^ Song X, Zhu CH, Doan C, Xie T (2002). "Germline stem cells anchored by adherens junctions in the Drosophila ovary niches". Science. 296 (5574): 1855–7. Bibcode:2002Sci...296.1855S. doi:10.1126/science.1069871. PMID 12052957.
- ^ Ian Murnaghan for Explore Stem Cells. Updated: ngày 16 tháng 12 năm 2013 Why Perform a Stem Cell Transplant?
- ^ Bone Marrow Transplantation and Peripheral Blood Stem Cell Transplantation In National Cancer Institute Fact Sheet web site. Bethesda, MD: National Institutes of Health, U.S. Department of Health and Human Services, 2010. Cited ngày 24 tháng 8 năm 2010
- ^ a b Master, Zubin; McLeod, Marcus; Mendez, Ivar (2007). "Benefits, Risks and Ethical Considerations in Translation of Stem Cell Research to Clinical Applications in Parkinson's Disease". Journal of Medical Ethics. 33 (3): 169–173.
- ^ Moore, Keith L., T.V.N. Persaud, and Mark G. Torchia. Before We Are Born: Essentials of Embryology and Birth Defects. Philadelphia, PA: Saunders, Elsevier. 2013 Print.
- ^ Bernadine Healy, M.D.. "Why Embryonic Stem Cells are obsolete" US News and world report. Truy cập Aug 17, 2015.
- ^ a b "Fetal Stem Cells Cause Tumor in a Teenage Boy".
- ^ Regalado, Antonio, David P. Hamilton (July 2006). "How a University's Patents May Limit Stem-Cell Researcher." The Wall Street Journal. Truy cập ngày 24 tháng 7 năm 2006.
- ^ Stephen Jenei for Patent Baristas, ngày 3 tháng 4 năm 2007 WARF Stem Cell Patents Knocked Down in Round One
- ^ Stephen Jenei for Patent Baristas, ngày 3 tháng 3 năm 2008 Ding! WARF Wins Round 2 As Stem Cell Patent Upheld
- ^ Constance Holden for Science Now. ngày 12 tháng 3 năm 2008 WARF Goes 3 for 3 on Patents
- ^ Stephen G. Kunin for Patents Post Grant. ngày 10 tháng 5 năm 2010 BPAI Rejects WARF Stem Cell Patent Claims in Inter Partes Reexamination Appeal
- ^ United States Patent And Trademark Office. Board Of Patent Appeals and Interferences. The Foundation For Taxpayer & Consumer Rights, Requester And Appellant V. Patent Of Wisconsin Alumni Research Foundation, Patent Owner And Respondent. Appeal 2012-011693, Reexamination Control 95/000,154. Patent 7,029,913 Decision on AppealArchived 2013-02-20 at the Wayback Machine.
- ^ GenomeWeb staff, ngày 3 tháng 7 năm 2013 Consumer Watchdog, PPF Seek Invalidation of WARF's Stem Cell Patent
- ^ a b c d e Stem Cell Basics: What are the potential uses of human stem cells and the obstacles that must be overcome before these potential uses will be realized?. In Stem Cell Information World Wide Web site. Bethesda, MD: National Institutes of Health, U.S. Department of Health and Human Services, 2009. cited Sunday, ngày 26 tháng 4 năm 2009
- ^ Steinberg, Douglas (November 2000) Stem Cells Tapped to Replenish Organsthescientist.com
- ^ ISRAEL21c: Israeli scientists reverse brain birth defects using stem cells ngày 25 tháng 12 năm 2008. (Researchers from the Hebrew University of Jerusalem-Hadassah Medical led by Prof. Joseph Yanai)
- ^ Kang KS, Kim SW, Oh YH, Yu JW, Kim KY, Park HK, Song CH, Han H (2005). "A 37-year-old spinal cord-injured female patient, transplanted of multipotent stem cells from human UC blood, with improved sensory perception and mobility, both functionally and morphologically: a case study". Cytotherapy. 7 (4): 368–73. doi:10.1080/14653240500238160. PMID 16162459.
- ^ Strauer BE, Schannwell CM, Brehm M (2009). "Therapeutic potentials of stem cells in cardiac diseases". Minerva Cardioangiol. 57 (2): 249–67. PMID 19274033.
- ^ Stem Cells Tapped to Replenish Organs thescientist.com, Nov 2000. By Douglas Steinberg
- ^ Hair Cloning Nears Reality as Baldness Cure WebMD November 2004
- ^ Yen AH, Sharpe PT (2008). "Stem cells and tooth tissue engineering". Cell Tissue Res. 331 (1): 359–72. doi:10.1007/s00441-007-0467-6. PMID 17938970.
- ^ "Gene therapy is first deafness 'cure'". New Scientist. ngày 14 tháng 2 năm 2005.
- ^ "Stem cells used to restore vision". BBC News.
- ^ Hanson, Charles; Hardarson, Thorir; Ellerström, Catharina; Nordberg, Markus; Caisander, Gunilla; Rao, Mahendra; Hyllner, Johan; Stenevi, Ulf (2013-03-01). "Transplantation of human embryonic stem cells onto a partially wounded human cornea in vitro". Acta Ophthalmologica. 91 (2): 127–130. doi:10.1111/j.1755-3768.2011.02358.x. ISSN 1755-3768. PMC 3660785. PMID 22280565.
- ^ Vastag B (2001). "Stem Cells Step Closer to the Clinic: Paralysis Partially Reversed in Rats with ALS-like Disease". JAMA: The Journal of the American Medical Association. 285(13): 1691–1693. doi:10.1001/jama.285.13.1691. PMID 11277806.
- ^ Anderson, Querida (2008-06-15). "Osiris Trumpets Its Adult Stem Cell Product". Genetic Engineering & Biotechnology News. Mary Ann Liebert, Inc. p. 13. Truy cập 2008-07-06.
(subtitle) Procymal is being developed in many indications, GvHD being the most advanced
- ^ Gurtner GC, Callaghan MJ, Longaker MT (2007). "Progress and potential for regenerative medicine". Annu. Rev. Med. 58: 299–312. doi:10.1146/annurev.med.58.082405.095329. PMID 17076602. Bone marrow transplantation is, as of 2009, the only established use of stem cells.
- ^ Hanna V, Gassei K, Orwig KE (2015). "Stem Cell Therapies for Male Infertility: Where Are We Now and Where Are We Going?". Biennial Review of Infertility. Bone marrow transplantation is, as of 2009, the only established use of stem cells.
- ^ Bubela T, Li MD, Hafez M, Bieber M, Atkins H (2012). "Is belief larger than fact: Expectations, optimism and reality for translational stem cell research". BMC Med. 10: 133. doi:10.1186/1741-7015-10-133. PMC 3520764. PMID 23131007.
- ^ Ader, M., & Tanaka, E. M. (2014). Modeling human development in 3D culture. Current Opinion in Cell Biology, 31, 23-28. doi:10.1016/j.ceb.2014.06.013
- ^ Greenhough S, Hay DC (2012). "Stem Cell-Based Toxicity Screening: Recent Advances in Hepatocyte Generation". Pharm Med. 26 (2): 85–89. doi:10.1007/BF03256896. Archived from the original on 2012-06-16.
- ^ Viện Y học phục hồi và tế bào gốc sinh học, thuộc trường Đại học Stanford ở California, Mỹ
- ^ VietnamPlus.vn, "Lập ngân hàng tế bào gốc từ dây rốn là trò bịp" Lưu trữ ngày 29 tháng 6 năm 2012 tại Wayback Machine
![[Review Sách] Điều kỳ diệu của tiệm tạp hóa Namiya](https://down-tx-vn.img.susercontent.com/8fef976e7fdbed68de49b58b2421f741.webp) GIẢM
16%
GIẢM
16%
 GIẢM
50%
GIẢM
50%
 GIẢM
14%
GIẢM
14%
 GIẢM
0%
GIẢM
0%
 GIẢM
-26%
GIẢM
-26%
 GIẢM
18%
GIẢM
18%

![[Eula] Giải nghĩa cung mệnh - Aphros Delos](https://upanh.nhatkythuthuat.com/images/2021/05/13/image-1.jpg)
:max_bytes(150000):strip_icc()/buffetts-road-to-riches-05f95062a9554d688bab91b1c3515a5d.png)
