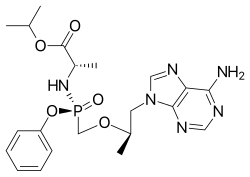
Tenofovir alafenamide
 | |
| Dữ liệu lâm sàng | |
|---|---|
| Tên thương mại | Vemlidy Genvoya (with elvitegravir, cobicistat và emtricitabine) Odefsey (with emtricitabine and rilpivirine) Descovy (with emtricitabine) |
| Đồng nghĩa | GS-7340 |
| Giấy phép | |
| Dược đồ sử dụng | Oral (tablets) |
| Mã ATC | |
| Tình trạng pháp lý | |
| Tình trạng pháp lý |
|
| Dữ liệu dược động học | |
| Liên kết protein huyết tương | ~80%[1] |
| Chu kỳ bán rã sinh học | 0.51 hours |
| Bài tiết | Feces (31.7%), urine (<1%) |
| Các định danh | |
Tên IUPAC
| |
| Số đăng ký CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| Định danh thành phần duy nhất | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| Dữ liệu hóa lý | |
| Công thức hóa học | C21H29N6O5P |
| Khối lượng phân tử | 476.466 g/mol |
| Mẫu 3D (Jmol) | |
SMILES
| |
Định danh hóa học quốc tế
| |

Tenofovir alafenamide (tên thương mại Vemlidy) là một chất ức chế men sao chép ngược nucleotide và là tiền chất của tenofovir. Nó được phát triển bởi Gilead Science để sử dụng trong điều trị nhiễm HIV và viêm gan B mạn tính, và được áp dụng dưới dạng tenofovir alafenamide fumarate (TAF). Liên quan chặt chẽ với chất ức chế men sao chép ngược thường được sử dụng tenofovir disoproxil fumarate (TDF), TAF có hoạt tính chống vi rút lớn hơn và phân phối tốt hơn vào các mô bạch huyết so với tác nhân đó.[2][3] Gilead đã được FDA chấp thuận vào tháng 11 năm 2016 cho thuốc Vemlidy.
Gilead công bố một thử nghiệm lâm sàng giai đoạn 3 đánh giá một chế độ single-tablet kết hợp tenofovir alafenamide với cobicistat, emtricitabine và elvitegravir [4] và phát triển một coformulation của thuốc với cobicistat, emtricitabine và chất ức chế protease darunavir.[5][6][7] Trong một nghiên cứu 48 tuần so sánh elvitegravir/cobicistat/emtricitabine/tenofovir disoproxil (tên thương mại Stribild) để elvitegravir/cobicistat/emtricitabine/tenofovir alafenamide (tên thương mại Genvoya), kết quả cho thấy loại thuốc mới hơn là noninferior đến đại lý thiết lập, nhưng với liều lượng thấp hơn nhiều và với tỷ lệ thấp hơn của các tác dụng phụ bất lợi như suy giảm chức năng thận.[8][9][10] FDA đã phê duyệt chế độ điều trị dựa trên TAF để điều trị HIV-1 vào tháng 11 năm 2015.[11] Genvoya là chế độ dựa trên TAF đầu tiên nhận được phê duyệt.[11]
Kết hợp liều cố định có chứa tenofovir alafenamide
[sửa | sửa mã nguồn]- Elvitegravir/cobicistat/emtricitabine/tenofovir alafenamide (tên thương mại Genvoya) - được phê duyệt ngày 5 tháng 11 năm 2015 (so sánh Elvitegravir/cobicistat/emtricitabine/tenofovir; tên thương mại Stribild)
- Emtricitabine/rilpivirine/tenofovir alafenamide (tên thương mại Odefsey) [12] - đã được phê duyệt ngày 1 tháng 3 năm 2016 (so sánh Emtricitabine/rilpivirine/tenofovir; tên thương mại tuân thủ)
- Emtricitabine/tenofovir alafenamide (tên thương mại Descovy) [13] - được phê duyệt ngày 4 tháng 4 năm 2016 (so sánh Emtricitabine/tenofovir; tên thương mại Truvada)
- Bictegravir/emtricitabine/tenofovir alafenamide (tên thương mại là Biktarvy) - đã được phê duyệt 2018.
- Darunavir/cobicistat/emtricitabine/tenofovir alafenamide (tên thương mại Symtuza) [14] - được phê duyệt ngày 17 tháng 7 năm 2018
Xem thêm
[sửa | sửa mã nguồn]- Sofosbuvir - một chất ức chế HCV RNA polymerase (NS5B) mang sự tương đồng về cấu trúc (chuỗi bên phosphoramidate được chuyển hóa bởi cathepsin A, carboxylesterase 1 và protein gắn với nucleotide triad nucleotide 1) [15][16]
Tham khảo
[sửa | sửa mã nguồn]- ^ “GENVOYA (elvitegravir, cobicistat, emtricitabine, and tenofovir alafenamide) Tablets, for Oral Use. Full Prescribing Information” (PDF). Gilead Sciences, Inc. Foster City, CA 94404.
- ^ Eisenberg, E. J.; He, G. X.; Lee, W. A. (2001). “Metabolism of Gs-7340, A Novel Phenyl Monophosphoramidate Intracellular Prodrug of Pmpa, in Blood”. Nucleosides, Nucleotides and Nucleic Acids. 20 (4–7): 1091–1098. doi:10.1081/NCN-100002496. PMID 11562963.
- ^ M Markowitz, A Zolopa, et al. GS-7340 Demonstrates Greater Declines in HIV-1 RNA than Tenofovir Disoproxil Fumarate During 14 Days of Monotherapy in HIV-1 Infected Subjects Lưu trữ 2012-04-25 tại Wayback Machine. 18th Conference on Retroviruses and Opportunistic Infections 2 Mar 2011. Paper # 152LB
- ^ “Gilead Initiates Phase 3 Clinical Program for Tenofovir Alafenamide” (Thông cáo báo chí). Gilead. tháng 1 năm 2013. Bản gốc lưu trữ ngày 7 tháng 2 năm 2013.
- ^ McQueen, Courtney (16 tháng 11 năm 2011). “Gilead And Tibotec To Develop Single-Pill Protease Inhibitor-Based Combination Regimen”. The AIDS Beacon. Bản gốc lưu trữ ngày 6 tháng 3 năm 2016. Truy cập ngày 14 tháng 8 năm 2019.
- ^ GS-7340 Packs Greater HIV Punch, Potentially Better Safety, Versus Viread Lưu trữ 2015-09-08 tại Wayback Machine Horn, Tim. 15 Mar 2012. AIDSmeds.com
- ^ Pharmacokinetics of a Novel EVG/COBI/FTC/GS-7340 Single Tablet Regimen. 13th International Workshop on Clinical Pharmacology of HIV Therapy. Barcelona, Spain. April 16–18, 2012.
- ^ Once-Daily Tenofovir Prodrug Combo Pill as Effective as Stribild Lưu trữ 2015-09-20 tại Wayback Machine. AIDSmeds.com 1 Nov 2012.
- ^ CROI 2013: New Pro-drug Tenofovir Alafenamide Appears Equally Effective but Better Tolerated Lưu trữ 2020-10-25 tại Wayback Machine. Highleyman, Liz. HIVandHepatitis.com. ngày 6 tháng 3 năm 2013.
- ^ Horn, T. et al. Tenefovir Alafenamide Fumarate (TAF) Sign-On Letter to Gilead. ngày 13 tháng 6 năm 2013. Treatment Action Group.
- ^ a b “U.S. Food and Drug Administration Approves Gilead's Single Tablet Regimen Genvoya (Elvitegravir, Cobicistat, Emtricitabine and Tenofovir Alafenamide) for Treatment of HIV-1 Infection”. Gilead. ngày 5 tháng 11 năm 2015. Bản gốc lưu trữ ngày 24 tháng 1 năm 2016. Truy cập ngày 14 tháng 8 năm 2019.
- ^ “Odefsey (emtricitabine, rilpivirine, and tenofovir alafenamide) Tablets, for Oral Use. U.S. Full Prescribing Information” (PDF). Gilead Sciences, Inc. Truy cập ngày 2 tháng 3 năm 2016.
- ^ “Descovy (emtricitabine and tenofovir alafenamide) Tablets, for Oral Use. U.S. Full Prescribing Information” (PDF). Gilead Sciences, Inc. Truy cập ngày 5 tháng 4 năm 2016.
- ^ Ankinapalli, AjayKumarReddy Ankinapalli. https://www.symtuza.com/ (PDF) http://www.janssenlabels.com/package-insert/product-monograph/prescribing-information/SYMTUZA-pi.pdf.
|title=trống hay bị thiếu (trợ giúp); Liên kết ngoài trong|website=(trợ giúp) - ^ “Comparison of tenofovir prodrugs: TAF vs TDF”. DRUG R&D INSIGHT. Truy cập ngày 24 tháng 11 năm 2015.
- ^ Murakami, E.; Tolstykh, T.; Bao, H.; Niu, C.; Steuer, H. M. M.; Bao, D.; Chang, W.; Espiritu, C.; Bansal, S. (ngày 26 tháng 8 năm 2010). “Mechanism of Activation of PSI-7851 and Its Diastereoisomer PSI-7977”. Journal of Biological Chemistry. 285 (45): 34337–34347. doi:10.1074/jbc.M110.161802. PMC 2966047. PMID 20801890.
 GIẢM
25%
GIẢM
25%
 GIẢM
39%
GIẢM
39%
![[Review sách] Bay trên tổ cúc cu - Ken Kesey](https://down-tx-vn.img.susercontent.com/079e668073f965ecde883224be898386.webp) GIẢM
20%
GIẢM
20%
 GIẢM
19%
GIẢM
19%
 GIẢM
29%
GIẢM
29%
 GIẢM
31%
GIẢM
31%


![[Lôi Thần] Không về phe Thiên Lý và mục đích của](https://gamek.mediacdn.vn/133514250583805952/2021/7/9/c2e58-16229262575586-800-16258434373711138241017.jpg)
![[Review] Mirai Radio to Jinkou Bato Trial - Radio Tương Lai Và Chim Bồ Câu Nhân Tạo](https://4.bp.blogspot.com/-wAz5UZWhWVo/W3H8DQDxJEI/AAAAAAAAAk8/tA7_cq6-49E-ii8MC-hsDWWKDXLZ2p5XwCLcBGAs/s1600/mirai%2Bradio%2B1.jpg)