Koštanomorfogenetski protein 4
Koštanomorfogenetski protein 4 jest protein koji je kod ljudi kodiran genom BMP4 sa hromosoma 14, sekvenca 14q22-q23.[4][5]
Otkriće
[uredi | uredi izvor]Koštanomorfogenetski proteini su prvobitno identifikovani sposobnošću demineralizovanog ekstrakta kostiju da indukuje endohrskavičnu osteogenezu in vivo na vanskeletnom mjestu.
Aminokiselinska sekvenca
[uredi | uredi izvor]Dužina polipeptidnog lanca je aminokiselina, a molekulska težina Da.[5]
| 10 | 20 | 30 | 40 | 50 | ||||
|---|---|---|---|---|---|---|---|---|
| MIPGNRMLMV | VLLCQVLLGG | ASHASLIPET | GKKKVAEIQG | HAGGRRSGQS | ||||
| HELLRDFEAT | LLQMFGLRRR | PQPSKSAVIP | DYMRDLYRLQ | SGEEEEEQIH | ||||
| STGLEYPERP | ASRANTVRSF | HHEEHLENIP | GTSENSAFRF | LFNLSSIPEN | ||||
| EVISSAELRL | FREQVDQGPD | WERGFHRINI | YEVMKPPAEV | VPGHLITRLL | ||||
| DTRLVHHNVT | RWETFDVSPA | VLRWTREKQP | NYGLAIEVTH | LHQTRTHQGQ | ||||
| HVRISRSLPQ | GSGNWAQLRP | LLVTFGHDGR | GHALTRRRRA | KRSPKHHSQR | ||||
| ARKKNKNCRR | HSLYVDFSDV | GWNDWIVAPP | GYQAFYCHGD | CPFPLADHLN | ||||
| STNHAIVQTL | VNSVNSSIPK | ACCVPTELSA | ISMLYLDEYD | KVVLKNYQEM | ||||
| VVEGCGCR |
Struktura proteina
[uredi | uredi izvor]Dajući aktivni karboksi-terminalni peptid od 116 ostataka, ljudski BMP4 se inicijalno sintetizira kao preprotein od 40% ostatka koji se cijepa nakon translacije. BMP4 ima sedam ostataka koji su konzervirani i glikozilirani.[6] Monomeri se drže disulfidnim mostovima i tri para cisteinskih aminokiselina. Ova konformacija naziva se "cistinski čvor". BMP4 može formirati homodimere ili heterodimere sa sličnim BMPS. Jedan primjer za to je BMP7. Ova sposobnost stvaranja homodimera ili heterodimera daje mogućnost veće osteoinduktivne aktivnosti nego samog BMP4.[7] Još se ne zna mnogo o tome kako BMPS stupa u interakciju sa vanćelijskim matriksom. Isto tako, malo se zna o putevima koji zatim razgrađuju BMP4.
Funkcija
[uredi | uredi izvor]BMP4 je član porodice koštanomorfogenetskih proteina koja je dio natporodice transformirajućih faktora rasta-beta. Natporodica uključuje velike porodice faktora rasta i diferencijacije. BMP4 je evolucijski visoko konzerviran. Nalazi u ranom embrionskom razvoju u ventralnoj marginalnoj zoni i u očima, srčanoj krvi i ušnoj vezikuli.[8]
BMP4 također ograničava stepen do kojeg dolazi do nervne diferencijacije u embrionima ksenopusa izazivanjem epiderme. Mogu pomoći u indukciji bočnih karakteristika u somitima. Somiti su potrebni za razvoj struktura kao što su mišići udova. BMP4 pomaže u oblikovanju glave u razvoju iako izaziva apoptoze ćelija nerevnog grebena ćelije; ovo se dešava u zadnjem mozgu.[9]
Kod odraslih, BMP4 je važan za neurogenezu (tj. stvaranje novih neurona) koja se javlja tokom života u dvije neurogene niše mozga, dentatni girus hipokampusa i subventrikulskoj zoni (SVZ) uz bočne komore. U ovim nišama, novi neuroni se kontinuirano stvaraju iz matičnih ćelija. U stvari, pokazalo se da u dentatnom girusu BMP4 održava nervne matične ćelije u mirovanju, čime se sprečava iscrpljivanje pula matičnih ćelija.[10] U SVZ, BMP posredovana signalizacija putem Smad4 je potrebna za pokretanje neurogeneze iz odraslih nervnih matičnih ćelija i potiskivanje alternativne sudbine oligodendrogliogeneze.[11] Štaviše, pokazalo se da u SVZ BMP4 ima diferencijativni učinak, jer sprečava defekt terminalne diferencijacije u SVZ neurosferama gdje je deletira gen Tis21/BTG2 –x potreban za terminalnu diferencijaciju.[12] Tis21 is a positive regulator of BMP4 expression in the SVZ.[12]
BMP4 je važan za metabolizam kostiju i hrskavice. BMP4 signalizacija je pronađena u formiranju ranih mezodermnih i zametnih ćelija. Regulacija pupoljaka ekstremiteta i razvoj pluća, jetre, zuba i mezenhimskih ćelija lica su druge važne funkcije koje se pripisuju signalizaciji BMP4-a.[13] Na formiranje prstiju utiče BMP4, zajedno sa drugim BMP signalima. Interdigitalni mezenhim pokazuje BMP4, koji sprečava apoptozu regije.[14] Formiranje zuba se oslanja na ekspresiju BMP4, koja indukuje Msx 1 i 2. Ovi faktori transkripcije pretvaraju formirani zub da postane i sjekutić.
BMP4 također ima važnu ulogu u masnom tkivu: neophodan je za adipogenezu bijelog masnog tkiva i promovira diferencijaciju adipocita.[15] Osim toga, važan je i za smeđu mast, gdje indukuje UCP1, povezan sa termogenezom bez drhtanja.[15]
Izlučivanje BMP4 pomaže u diferencijaciji pupoljka uretera u mokraćovod.[16]
BMP4 antagonizira tkivo organizatora i eksprimira se u ranom razvoju u tkivu ektoderma i mezoderma. Nakon gastrulacije, transkripcija BMP4 je ograničena na ventrolateralnu marginalnu zonu, zbog inhibicije sa dorzalne strane embriona u razvoju. BMP4 pomaže u ventralizaciji mezoderma, koji vodi formiranje dorzalno-ventralne ose. U rodu Xenopus, za BMP4 otkriveno je da pomaže u formiranju krvi i krvnih ostrva.[17]
BMP4, prvobitno eksprimiran u epidermi, tokom formiranja nervne cijevi, nalazi se u krovnoj ploči. Gradijent BMP signalizacije nalazi se u suprotnosti sa gradijentom zvučnog ježa. Ova ekspresija BMP4 oblikuje dorzalne neurone.[18]
BMP4, zajedno sa FGF2, promoviše diferencijaciju matičnih ćelija u mezodermne linije. Nakon diferencijacije, ćelije tretirane BMP4 i FGF2 općenito proizvode veće količine osteogene i hondorgene diferencijacije nego netretirane matične ćelije.[19] Također, u kombinaciji sa FGF2 može proizvesti progenitorne ćelije štitne žlijezde iz pluripotentnih matičnih ćelija kod miševa i ljudi.[20]
Pokazalo se da BMP4 indukuje ekspresiju gena porodice Msx, za koju se vjeruje da je dio formiranja hrskavice iz somitskog mezoderma.[21]
BMP4, parakrini faktor rasta, pronađen je kod pacovskih jajnika. BMP4, zajedno sa BMP7, reguliše rani razvoj folikula jajnika i prelazak iz primordijalnog u primarni folikul. Osim toga, pokazalo se da inhibicija BMP4 antitijelima smanjuje ukupnu veličinu jajnika. Ovi rezultati pokazuju da BMP4 može pomoći u preživljavanju i prevenciji apoptoze kod oocita.[13]
Kod ptica pokazalo se da BMP4 utiče na veličinu kljuna Darwinove zebe. Male količine BMP4 su u korelaciji sa niskom dubinom i širinom kljuna. Suprotno tome, visoka ekspresija BMP4 stvara veliku dubinu i širinu kljuna. Genetička regulacija BMP4 pruža osnovu za prirodnu selekciju u ptičjim kljunovima.[22]
Inhibicija
[uredi | uredi izvor]Inhibicija BMP4 signala (putem hordina, nogina ili folistatina) uzrokuje da se ektoderm diferencira u nervnu ploču. Ako ove ćelije takođe primaju signale od FGF, one će se diferencirati u kičmenu moždinu; u nedostatku FGF ćelije postaju moždano tkivo.
Dok prekomjerna ekspresija BMP4 može dovesti do ventralizacije, inhibicija s dominantnim negativnim uticajem može rezultirati potpunom dorzalizacijom embrija ili formiranjem dvije osovine.[23]
Važno je napomenuti da su miševi kod kojih je BMP4 inaktiviran obično uginuli tokom gastrulacija. Smatra se da bi inaktivacija ljudskog BMP4 vjerovatno imala isti efekat. Međutim, mutacije koje su suptilne kod ljudi mogu imati i suptilne fenotipske efekte.
Izoforme
[uredi | uredi izvor]Opisana je alternativna preradaalternativno u 5' neprevedenom regionu ovog gena i opisane su tri varijante transkripta, od kojih sve kodiraju identičan protein.[24]
Molekulski mehanizmi
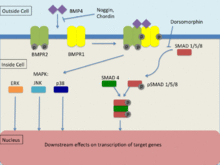
[uredi | uredi izvor]BMP4, kao član porodice transformirajućih faktora rasta-β (TGF-β), vezuje se za dva različita tipa receptora serin-treonin kinaze, poznatih kao BMPR1 i BMPR2.[25] Dolazi do prijenosa signala preko ovih receptora putem Smad-a i mapiraju kinazne puteve da bi izvršili transkripciju svojih ciljnih gena. Da bi došlo do transdukcije signala, oba receptora moraju biti funkcionalna. BMP se može vezati za BMPR2 bez BMPR1; međutim afinitet se značajno povećava u prisustvu oba receptora. BMPR1 je transfosforiliran preko BMPR2 koji indukuje nizvodnu signalizaciju unutar ćelije, utičući na transkripciju.[25]
Signalni put Smad
[uredi | uredi izvor]Za transdukciju signala, receptori porodice TGF-β najčešće koriste Smadov signalni put.[25] Tip 2 receptora odgovorni su za aktiviranje tipa 1 receptora, gdje njihova funkcija uključuje fosforilacije R-Smada (Smad-1, Smad-5, Smad-8). Nakon fosforilacije, javlja se formiranje R-SMAD kompleksa u sprezi sa zajedničkim partnerom Smad (ko-Smad), gdje migrira u nukleus. Signalizacija ovog puta regulirana je malim molekulskim inhibitorom, poznatim kao doruzomorfin koji sprječava nizvodne efekte R-smada.[25]
Mapa signalnih kinaznih puteva (MAPK)
[uredi | uredi izvor]Mitogenom aktivirane proteinske kinaze (MAPK) prolaze kroz fosforilaciju putem signalne kaskade, gdje MAPKKK fosforilira i aktivira MAPKK i MAPKK fosforilira i aktivira MAPK, što zatim inducira unutarćelijski odgovor.[26] Aktivacija MAPKKK je putem interakcije uglavnom GTPaza ili druge grupe proteinskih kinaza. TGF-β receptori induciraju MAPK signalne puteve ERK, JNK i p38.[26] Poznato je da BMP4 aktivira ERK, JNK i p38 MAPK signalne puteve, dok je otkriveno da djeluje nezavisno od Smad puteva signalizacije, uglavnom su aktivni u sprezi sa Smadom.[27] Aktivacija ERK i JNK puteva djeluje na fosforilaciju Smada i stoga reguliše njegovu aktivaciju. Pored toga, MAPK putevi mogu biti u mogućnosti da direktno utiču na transkripcijske faktore u interakciji sa Smadom, preko JNK ili p38 supstrata koji indukuje konvergenciju dva signalna puta. Zapaženo je da se ova konvergencija uglavnom sastoji od kooperativnog ponašanja; međutim, postoje dokazi koji ukazuju na to da se oni ponekad mogu međusobno suprotstaviti. Nadalje, ravnoteža koja postoji između direktne aktivacije ovih signalnih puteva ima značajan utjecaj na TGF-β inducirane ćelijske odgovore.[27]
Klinički značaj
[uredi | uredi izvor]Povećanje ekspresije BMP4 povezano je sa raznim bolestima kostiju, uključujući nasljedni poremećaj fibrodysplasia ossificans progressiva.[28] Postoje jaki dokazi iz studija sekvenciranja gena kandidata uključenih u rascjep da mutacije u genu koštanomorfogenetskog proteina 4 (BMP4) mogu biti povezane u patogenezi rascjepa usne i/ili nepca.[29]
Razvoj očiju
[uredi | uredi izvor]Oči su neophodne organizmima, posebno kopnenim kičmenjacima, da posmatraju plijen i prepreke; ovo je ključno za njihov opstanak. Formiranje očiju počinje kao očne vezikule i sočiva izvedena iz neuroektoderma. Poznato je da koštanomorfogenetski proteini stimulišu formiranje očnih sočiva.
Tokom ranog razvoja očiju, formiranje očnih vezikula je bitno kod miševa i BMP4 je snažno izražen u očnoj vezikuli i slabo u okolnom mezenhimu i površinskom ektodermu. Ovaj koncentracijski gradijent BMP4 u očnoj vezikuli je kritičan za indukciju sočiva. Dr. Furuta i dr. Hogan otkrili su da ako se laserski inducira mutacija na embrionima miševa nastaje BMP4 homozigotna nulta mutacija, zbog koje ovaj embrion neće razviti sočivo. Također su uradili in situ hibridizacija gena BMP4, pokazujući zelenu boju i Sox2 gen u crvenoj za koji su mislili da je također uključen u formiranje sočiva. Nakon što su izvršili ove dvije in situ hibridizacije u embrionima miševa, otkrili su da se i zelena i crvena boja nalaze u optičkoj vezikuli mišjih embriona. Ovo je pokazalo da su BMP4 i Sox2 eksprimirani na pravom mjestu u pravo vrijeme očnih vezikula i dokazuju da imaju neke bitne funkcije za indukciju sočiva. Nadalje, izvršili su naknadni eksperiment ubrizgavanjem BMP4 u BMP4 homozigotni mutantni embrioni i spasili formiranje sočiva. Ovo ukazuje da je BMP4 definitivno potreban za formiranje sočiva. Međutim, također su otkrili da se neki od mutiranih miševa ne mogu spasiti. Kasnije su otkrili da tim mutantima nedostaje Msx 2 koji se aktivira BMP4. Mehanizam koji su predvidjeli bio je da će BMP4 aktivirati Msx 2 u očnoj vezikuli i da su zajednička kombinacija koncentracije BMP4 i Msx2 i aktivni Sox2 i Sox2 neophodni za diferencijaciju sočiva.[30]
Injection of Noggin into lens fiber cells in mice significantly reduces the BMP4 proteins in the cells. This indicates that Noggin is sufficient to inhibit the production of BMP4. Moreover, another inhibitor protein, Alk6 was found that blocked the BMP4 from activating the Msx2 which stopped lens differentiation .[31] However, there are still a lot of unknown about the mechanism of inhibition on BMP4 and downstream regulation of Sox2. In the future, researchers are aiming to find out a more complete pathway of whole eye development and hoping one day, they can find a way to cure some genetic caused eye diseases.
Gubitak kose
[uredi | uredi izvor]Gubitak kose/dlake, poznat kao alopecija uzrokovan je promjenom morfologije folikula dlake i njenim ciklusom na abnormalan način.[32] Ciklusi folikula dlake su ciklusi rasta, ili anagen, regresije ili katagen, i mirovanja ili telogen.[33] Kod sisara, recipročne epitelne i mezenhimske interakcije kontrolišu razvoj dlake. Geni kao što su BMP4 i BMP2 su oba aktivni unutar dlakinih prekursora. Konkretno, BMP4 nalazi se u dermnoj papili. BMP4 je dio signalne mreže koja kontrolira razvoj kose. Potreban je za indukciju biohemijskih puteva i signalizaciju za regulaciju diferencijacije osovine dlake u anagenom dlakinom folikulu. Ovo se postiže kontrolom ekspresije transkripcijskih faktora koji regulišu diferencijaciju dlaka. Međutim, još uvijek je nejasno gdje BMP djeluju unutar genetičke mreže. Signalizacija bmp4 može potencijalno kontrolirati ekspresiju terminalnih diferencijacijskih molekula kao što su keratini. Pokazalo se da i drugi regulatori kontrolišu razvoj dlakinog folikula. HOXC13 i FOXN1 smatraju se važnim regulatorima jer eksperimenti s gubitkom funkcije pokazuju narušenu diferencijaciju osovine dlake koja ne ometa formiranje folikula dlake.[34]
Kada se BMP4 eksprimira ektopijski, kod transgenih miševa inhibira se vanjska ovojnica korijena dlakinog folikula (ORS) i proliferacija ćelijskog matriksa. BMP4 takođe aktivira ekspresije gena za dlakin keratin, napominjući da je BMP4 važan u diferencijaciji vlasi. Nogin, poznati inhibitor BMP4, nalazi se u ćelijama dlakinog matriksa. Drugi važni faktori koje treba uzeti u obzir u razvoju dlake su ekspresija Shh (sonični jež), BMP7, BMP2, WNT i β-katenin jer su oni potrebni u ranoj fazi morfogeneze.[35]
Ostali geni koji mogu inhibirati BMP4 ili stupiti u interakciju s BMP4 su nogin, folistatin i gremlin, koji su svi eksprimirani u folikulima dlake u razvoju.[36] Kod miševa kod kojih nedostaje nogin, ima manje dlakinih folikula nego kod normalnog miša i razvoj folikula je inhibiran. U kokošijim embrionima pokazano je da ektopijsko eksprimirani nogin proizvodi uvećane folikule, a BMP4 signalizacija pokazuje potisnutu sudbinu plakoda u obližnjim ćelijama.[7] Tokom eksperimenata in vivo, pokazalo se da nogin je također indukuje rast dlaka na postneonatusnoj koži.[37]
BMP4 je važna komponenta bioloških puteva koji su uključivali regulaciju diferencijacije osovine dlake unutar anagenog dlakinog folikula. Najjači nivoi ekspresiranog BMP4 nalaze se unutar medule, ćelija dlake, distalnog matriksa dlake i potencijalnih prekursora kutikula. Dva glavna načina koji BMP4 inhibiraju ekspresiju dlake su ograničavanje ekspresije faktora rasta u matriksu dlake i antagonizam između signalizacije rasta i diferencijacije.[35]
Putevi koji regulišu formiranje folikula dlake i rast dlake ključni su u razvoju terapijskih metoda za stanja opadanja kose. Takva stanja uključuju razvoj novih folikula, promjenu oblika karakteristika postojećih folikula i promjenu rasta dlake u postojećim dlakinim folikulima. Nadalje, BMP4 i put kroz koji djeluje mogu pružiti terapeutske ciljeve za prevenciju gubitka kose.[33]
Reference
[uredi | uredi izvor]- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000021835 - Ensembl, maj 2017
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ van den Wijngaard A, Weghuis DO, Boersma CJ, van Zoelen EJ, Geurts van Kessel A, Olijve W (novembar 1995). "Fine mapping of the human bone morphogenetic protein-4 gene (BMP4) to chromosome 14q22-q23 by in situ hybridization". Genomics. 27 (3): 559–60. doi:10.1006/geno.1995.1096. hdl:2066/22049. PMID 7558046.
- ^ a b Oida S, Iimura T, Maruoka Y, Takeda K, Sasaki S (novembar 1995). "Cloning and sequence of bone morphogenetic protein 4 (BMP-4) from a human placental cDNA library". DNA Seq. 5 (5): 273–5. doi:10.3109/10425179509030980. PMID 7579580.
- ^ Aono A, Hazama M, Notoya K, Taketomi S, Yamasaki H, Tsukuda R, Sasaki S, Fujisawa Y (maj 1995). "Potent ectopic bone-inducing activity of bone morphogenetic protein-4/7 heterodimer". Biochem. Biophys. Res. Commun. 210 (3): 670–7. doi:10.1006/bbrc.1995.1712. PMID 7763240.
- ^ a b Botchkarev VA, Botchkareva NV, Roth W, Nakamura M, Chen LH, Herzog W, Lindner G, McMahon JA, Peters C, Lauster R, McMahon AP, Paus R (juli 1999). "Noggin is a mesenchymally derived stimulator of hair-follicle induction". Nat. Cell Biol. 1 (3): 158–64. doi:10.1038/11078. PMID 10559902. S2CID 8777441.
- ^ Knöchel S, Dillinger K, Köster M, Knöchel W (novembar 2001). "Structure and expression of Xenopus tropicalis BMP-2 and BMP-4 genes". Mech. Dev. 109 (1): 79–82. doi:10.1016/S0925-4773(01)00506-8. PMID 11677055. S2CID 792305.
- ^ Graham et al., 1994
- ^ Mira H, Andreu Z, Suh H, Lie DC, Jessberger S, Consiglio A, San Emeterio J, Hortigüela R, Marqués-Torrejón MA, Nakashima K, Colak D, Götz M, Fariñas I, Gage FH (2010). "Signaling through BMPR-IA regulates quiescence and long-term activity of neural stem cells in the adult hippocampus". Cell Stem Cell. 7 (1): 78–89. doi:10.1016/j.stem.2010.04.016. PMID 20621052.
- ^ Colak D, Mori T, Brill MS, Pfeifer A, Falk S, Deng C, Monteiro R, Mummery C, Sommer L, Götz M (2008). "Adult neurogenesis requires Smad4-mediated bone morphogenic protein signaling in stem cells". The Journal of Neuroscience. 28 (2): 434–446. doi:10.1523/JNEUROSCI.4374-07.2008. PMC 6670509. PMID 18184786.
- ^ a b Farioli-Vecchioli S, Ceccarelli M, Saraulli D, Micheli L, Cannas S, D'Alessandro F, Scardigli R, Leonardi L, Cinà I, Costanzi M, Mattera A, Cestari V, Tirone F (2014). "Tis21 is required for adult neurogenesis in the subventricular zone and for olfactory behavior regulating cyclins, BMP4, Hes1/5 and Ids". Front Cell Neurosci. 8: 98. doi:10.3389/fncel.2014.00098. PMC 3977348. PMID 24744701.
- ^ a b Nilsson EE, Skinner MK (oktobar 2003). "Bone morphogenetic protein-4 acts as an ovarian follicle survival factor and promotes primordial follicle development". Biol. Reprod. 69 (4): 1265–72. doi:10.1095/biolreprod.103.018671. PMID 12801979. S2CID 2141586.
- ^ Arteaga-Solis E, Gayraud B, Lee SY, Shum L, Sakai L, Ramirez F (juli 2001). "Regulation of limb patterning by extracellular microfibrils". J. Cell Biol. 154 (2): 275–81. doi:10.1083/jcb.200105046. PMC 2150751. PMID 11470817.
- ^ a b Blázquez-Medela AM, Jumabay M, Boström KI (maj 2019). "Beyond the bone: Bone morphogenetic protein signaling in adipose tissue". Obesity Reviews. 20 (5): 648–658. doi:10.1111/obr.12822. PMC 6447448. PMID 30609449.
- ^ Miyazaki Y, Oshima K, Fogo A, Ichikawa I (mart 2003). "Evidence that bone morphogenetic protein 4 has multiple biological functions during kidney and urinary tract development". Kidney Int. 63 (3): 835–44. doi:10.1046/j.1523-1755.2003.00834.x. PMID 12631064.
- ^ Hemmati-Brivanlou A, Thomsen GH (1995). "Ventral mesodermal patterning in Xenopus embryos: expression patterns and activities of BMP-2 and BMP-4". Dev. Genet. 17 (1): 78–89. doi:10.1002/dvg.1020170109. PMID 7554498.
- ^ Selleck MA, García-Castro MI, Artinger KB, Bronner-Fraser M (decembar 1998). "Effects of Shh and Noggin on neural crest formation demonstrate that BMP is required in the neural tube but not ectoderm". Development. 125 (24): 4919–30. doi:10.1242/dev.125.24.4919. PMID 9811576. Arhivirano s originala, 20. 5. 2022. Pristupljeno 16. 3. 2022.
- ^ Lee TJ, Jang J, Kang S, Jin M, Shin H, Kim DW, Kim BS (januar 2013). "Enhancement of osteogenic and chondrogenic differentiation of human embryonic stem cells by mesodermal lineage induction with BMP-4 and FGF2 treatment". Biochem. Biophys. Res. Commun. 430 (2): 793–7. doi:10.1016/j.bbrc.2012.11.067. PMID 23206696.
- ^ Kurmann AA, Serra M, Hawkins F, Rankin SA, Mori M, Astapova I, Ullas S, Lin S, Bilodeau M, Rossant J, Jean JC, Ikonomou L, Deterding RR, Shannon JM, Zorn AM, Hollenberg AN, Kotton DN (novembar 2015). "Regeneration of Thyroid Function by Transplantation of Differentiated Pluripotent Stem Cells". Cell Stem Cell (jezik: engleski). 17 (5): 527–42. doi:10.1016/j.stem.2015.09.004. PMC 4666682. PMID 26593959.
- ^ Watanabe Y, Le Douarin NM (juni 1996). "A role for BMP-4 in the development of subcutaneous cartilage". Mech. Dev. 57 (1): 69–78. doi:10.1016/0925-4773(96)00534-5. PMID 8817454. S2CID 16858412.
- ^ Abzhanov A, Protas M, Grant BR, Grant PR, Tabin CJ (septembar 2004). "Bmp4 and morphological variation of beaks in Darwin's finches". Science. 305 (5689): 1462–5. Bibcode:2004Sci...305.1462A. doi:10.1126/science.1098095. PMID 15353802. S2CID 17226774.
- ^ Metz A, Knöchel S, Büchler P, Köster M, Knöchel W (juni 1998). "Structural and functional analysis of the BMP-4 promoter in early embryos of Xenopus laevis". Mech. Dev. 74 (1–2): 29–39. doi:10.1016/S0925-4773(98)00059-8. PMID 9651472. S2CID 14496024.
- ^ "Entrez Gene: BMP4 bone morphogenetic protein 4".
- ^ a b c d Miyazono K, Kamiya Y, Morikawa M (januar 2010). "Bone morphogenetic protein receptors and signal transduction". J. Biochem. 147 (1): 35–51. doi:10.1093/jb/mvp148. PMID 19762341.
- ^ a b Cell Signaling Technology, Inc. "Mitogen-Activated Protein Kinase Cascades". Pristupljeno 17. 11. 2012.
- ^ a b Derynck R, Zhang YE (oktobar 2003). "Smad-dependent and Smad-independent pathways in TGF-beta family signaling". Nature. 425 (6958): 577–84. Bibcode:2003Natur.425..577D. doi:10.1038/nature02006. PMID 14534577. S2CID 4419607.
- ^ Kan L, Hu M, Gomes WA, Kessler JA (oktobar 2004). "Transgenic Mice Overexpressing BMP4 Develop a Fibrodysplasia Ossificans Progressiva (FOP)-Like Phenotype". Am. J. Pathol. 165 (4): 1107–15. doi:10.1016/S0002-9440(10)63372-X. PMC 1618644. PMID 15466378.
- ^ Dixon MJ, Marazita ML, Beaty TH, Murray JC (mart 2011). "Cleft lip and palate: understanding genetic and environmental influences". Nat. Rev. Genet. 12 (3): 167–78. doi:10.1038/nrg2933. PMC 3086810. PMID 21331089.
- ^ Furuta Y, Hogan BL (decembar 1998). "BMP4 is essential for lens induction in the mouse embryo". Genes Dev. 12 (23): 3764–75. doi:10.1101/gad.12.23.3764. PMC 317259. PMID 9851982.
- ^ Faber SC, Robinson ML, Makarenkova HP, Lang RA (august 2002). "Bmp signaling is required for development of primary lens fiber cells". Development. 129 (15): 3727–37. doi:10.1242/dev.129.15.3727. PMID 12117821.
- ^ Cotsarelis G, Millar SE (juli 2001). "Towards a molecular understanding of hair loss and its treatment". Trends Mol Med. 7 (7): 293–301. doi:10.1016/S1471-4914(01)02027-5. PMID 11425637.
- ^ a b Millar SE (februar 2002). "Molecular mechanisms regulating hair follicle development". J. Invest. Dermatol. 118 (2): 216–25. doi:10.1046/j.0022-202x.2001.01670.x. PMID 11841536.
- ^ Kulessa H, Turk G, Hogan BL (decembar 2000). "Inhibition of Bmp signaling affects growth and differentiation in the anagen hair follicle". EMBO J. 19 (24): 6664–74. doi:10.1093/emboj/19.24.6664. PMC 305899. PMID 11118201.
- ^ a b Huelsken J, Vogel R, Erdmann B, Cotsarelis G, Birchmeier W (maj 2001). "beta-Catenin controls hair follicle morphogenesis and stem cell differentiation in the skin". Cell. 105 (4): 533–45. doi:10.1016/S0092-8674(01)00336-1. PMID 11371349. S2CID 16775006.
- ^ Feijen A, Goumans MJ, van den Eijnden-van Raaij AJ (decembar 1994). "Expression of activin subunits, activin receptors and follistatin in postimplantation mouse embryos suggests specific developmental functions for different activins". Development. 120 (12): 3621–37. doi:10.1242/dev.120.12.3621. PMID 7821227.
- ^ Botchkarev VA, Botchkareva NV, Nakamura M, Huber O, Funa K, Lauster R, Paus R, Gilchrest BA (oktobar 2001). "Noggin is required for induction of the hair follicle growth phase in postnatal skin". FASEB J. 15 (12): 2205–14. doi:10.1096/fj.01-0207com. PMID 11641247. S2CID 10236217.
Dopunska literatura
[uredi | uredi izvor]- Wozney JM, Rosen V, Celeste AJ, Mitsock LM, Whitters MJ, Kriz RW, Hewick RM, Wang EA (1989). "Novel regulators of bone formation: molecular clones and activities". Science. 242 (4885): 1528–34. doi:10.1126/science.3201241. PMID 3201241.
- Rosenzweig BL, Imamura T, Okadome T, Cox GN, Yamashita H, ten Dijke P, Heldin CH, Miyazono K (1995). "Cloning and characterization of a human type II receptor for bone morphogenetic proteins". Proc. Natl. Acad. Sci. U.S.A. 92 (17): 7632–6. Bibcode:1995PNAS...92.7632R. doi:10.1073/pnas.92.17.7632. PMC 41199. PMID 7644468.
- Nohno T, Ishikawa T, Saito T, Hosokawa K, Noji S, Wolsing DH, Rosenbaum JS (1995). "Identification of a human type II receptor for bone morphogenetic protein-4 that forms differential heteromeric complexes with bone morphogenetic protein type I receptors". J. Biol. Chem. 270 (38): 22522–6. doi:10.1074/jbc.270.38.22522. PMID 7673243.
- Yamaji N, Celeste AJ, Thies RS, Song JJ, Bernier SM, Goltzman D, Lyons KM, Nove J, Rosen V, Wozney JM (1995). "A mammalian serine/threonine kinase receptor specifically binds BMP-2 and BMP-4". Biochem. Biophys. Res. Commun. 205 (3): 1944–51. doi:10.1006/bbrc.1994.2898. PMID 7811286.
- Harris SE, Harris MA, Mahy P, Wozney J, Feng JQ, Mundy GR (1994). "Expression of bone morphogenetic protein messenger RNAs by normal rat and human prostate and prostate cancer cells". Prostate. 24 (4): 204–11. doi:10.1002/pros.2990240406. PMID 8146069. S2CID 21276656.
- van den Wijngaard A, van Kraay M, van Zoelen EJ, Olijve W, Boersma CJ (1996). "Genomic organization of the human bone morphogenetic protein-4 gene: molecular basis for multiple transcripts". Biochem. Biophys. Res. Commun. 219 (3): 789–94. doi:10.1006/bbrc.1996.0312. hdl:2066/23948. PMID 8645259.
- Nishitoh H, Ichijo H, Kimura M, Matsumoto T, Makishima F, Yamaguchi A, Yamashita H, Enomoto S, Miyazono K (1996). "Identification of type I and type II serine/threonine kinase receptors for growth/differentiation factor-5". J. Biol. Chem. 271 (35): 21345–52. doi:10.1074/jbc.271.35.21345. PMID 8702914.
- Bonaldo MF, Lennon G, Soares MB (1997). "Normalization and subtraction: two approaches to facilitate gene discovery". Genome Res. 6 (9): 791–806. doi:10.1101/gr.6.9.791. PMID 8889548.
- Shore EM, Xu M, Shah PB, Janoff HB, Hahn GV, Deardorff MA, Sovinsky L, Spinner NB, Zasloff MA, Wozney JM, Kaplan FS (1998). "The human bone morphogenetic protein 4 (BMP-4) gene: molecular structure and transcriptional regulation". Calcif. Tissue Int. 63 (3): 221–9. doi:10.1007/s002239900518. PMID 9701626. S2CID 8339465.
- Tucker AS, Matthews KL, Sharpe PT (1998). "Transformation of tooth type induced by inhibition of BMP signaling". Science. 282 (5391): 1136–8. Bibcode:1998Sci...282.1136T. doi:10.1126/science.282.5391.1136. PMID 9804553.
- Van den Wijngaard A, Pijpers MA, Joosten PH, Roelofs JM, Van zoelen EJ, Olijve W (1999). "Functional characterization of two promoters in the human bone morphogenetic protein-4 gene". J. Bone Miner. Res. 14 (8): 1432–41. doi:10.1359/jbmr.1999.14.8.1432. PMID 10457277.
- Li W, LoTurco JJ (2000). "Noggin is a negative regulator of neuronal differentiation in developing neocortex". Dev. Neurosci. 22 (1–2): 68–73. doi:10.1159/000017428. PMID 10657699. S2CID 35547875.
- Raatikainen-Ahokas A, Hytönen M, Tenhunen A, Sainio K, Sariola H (2000). "BMP-4 affects the differentiation of metanephric mesenchyme and reveals an early anterior-posterior axis of the embryonic kidney". Dev. Dyn. 217 (2): 146–58. doi:10.1002/(SICI)1097-0177(200002)217:2<146::AID-DVDY2>3.0.CO;2-I. PMID 10706139.
- van den Wijngaard A, Mulder WR, Dijkema R, Boersma CJ, Mosselman S, van Zoelen EJ, Olijve W (2000). "Antiestrogens specifically up-regulate bone morphogenetic protein-4 promoter activity in human osteoblastic cells". Mol. Endocrinol. 14 (5): 623–33. doi:10.1210/me.14.5.623. PMID 10809227.
- Ying Y, Liu XM, Marble A, Lawson KA, Zhao GQ (2000). "Requirement of Bmp8b for the generation of primordial germ cells in the mouse". Mol. Endocrinol. 14 (7): 1053–63. doi:10.1210/mend.14.7.0479. PMID 10894154.
- Nakade O, Takahashi K, Takuma T, Aoki T, Kaku T (2001). "Effect of extracellular calcium on the gene expression of bone morphogenetic protein-2 and -4 of normal human bone cells". J. Bone Miner. Metab. 19 (1): 13–9. doi:10.1007/s007740170055. PMID 11156467. S2CID 23873280.
- Hatta T, Konishi H, Katoh E, Natsume T, Ueno N, Kobayashi Y, Yamazaki T (2001). "Identification of the ligand-binding site of the BMP type IA receptor for BMP-4". Biopolymers. 55 (5): 399–406. doi:10.1002/1097-0282(2000)55:5<399::AID-BIP1014>3.0.CO;2-9. PMID 11241215.
- Aoki H, Fujii M, Imamura T, Yagi K, Takehara K, Kato M, Miyazono K (2001). "Synergistic effects of different bone morphogenetic protein type I receptors on alkaline phosphatase induction". J. Cell Sci. 114 (Pt 8): 1483–9. doi:10.1242/jcs.114.8.1483. PMID 11282024.
- Kalinovsky A, Boukhtouche F, Blazeski R, Bornmann C, Suzuki N, Mason CA, Scheiffele P (2011). Polleux F (ured.). "Development of Axon-Target Specificity of Ponto-Cerebellar Afferents". PLOS Biology. 9 (2): e1001013. doi:10.1371/journal.pbio.1001013. PMC 3035609. PMID 21346800.
- Cotsarelis G, Millar SE (juli 2001). "Towards a molecular understanding of hair loss and its treatment". Trends Mol Med. 7 (7): 293–301. doi:10.1016/S1471-4914(01)02027-5. PMID 11425637.
- Feijen A, Goumans MJ, van den Eijnden-van Raaij AJ (decembar 1994). "Expression of activin subunits, activin receptors and follistatin in postimplantation mouse embryos suggests specific developmental functions for different activins". Development. 120 (12): 3621–37. doi:10.1242/dev.120.12.3621. PMID 7821227.
- Graham A, Francis-West P, Brickell P, Lumsden A (decembar 1994). "The signalling molecule BMP4 mediates apoptosis in the rhombencephalic neural crest". Nature. 372 (6507): 684–6. Bibcode:1994Natur.372..684G. doi:10.1038/372684a0. PMID 7990961. S2CID 4361935.
- Huelsken J, Vogel R, Erdmann B, Cotsarelis G, Birchmeier W (maj 2001). "beta-Catenin controls hair follicle morphogenesis and stem cell differentiation in the skin". Cell. 105 (4): 533–45. doi:10.1016/S0092-8674(01)00336-1. PMID 11371349. S2CID 16775006.
- Kulessa H, Turk G, Hogan BL (decembar 2000). "Inhibition of Bmp signaling affects growth and differentiation in the anagen hair follicle". EMBO J. 19 (24): 6664–74. doi:10.1093/emboj/19.24.6664. PMC 305899. PMID 11118201.
- Leong LM, Brickell PM (decembar 1996). "Bone morphogenic protein-4". Int. J. Biochem. Cell Biol. 28 (12): 1293–6. doi:10.1016/S1357-2725(96)00075-1. PMID 9022288.
- Liem KF, Tremml G, Roelink H, Jessell TM (septembar 1995). "Dorsal differentiation of neural plate cells induced by BMP-mediated signals from epidermal ectoderm". Cell. 82 (6): 969–79. doi:10.1016/0092-8674(95)90276-7. PMID 7553857. S2CID 17106597.
- Millar SE (februar 2002). "Molecular mechanisms regulating hair follicle development". J. Invest. Dermatol. 118 (2): 216–25. doi:10.1046/j.0022-202x.2001.01670.x. PMID 11841536.
- Pourquié O, Fan CM, Coltey M, Hirsinger E, Watanabe Y, Bréant C, Francis-West P, Brickell P, Tessier-Lavigne M, Le Douarin NM (februar 1996). "Lateral and axial signals involved in avian somite patterning: a role for BMP4". Cell. 84 (3): 461–71. doi:10.1016/S0092-8674(00)81291-X. PMID 8608600. S2CID 15824329.
- Wang EA, Israel DI, Kelly S, Luxenberg DP (1993). "Bone morphogenetic protein-2 causes commitment and differentiation in C3H10T1/2 and 3T3 cells". Growth Factors. 9 (1): 57–71. doi:10.3109/08977199308991582. PMID 8347351.
- Winnier G, Blessing M, Labosky PA, Hogan BL (septembar 1995). "Bone morphogenetic protein-4 is required for mesoderm formation and patterning in the mouse". Genes Dev. 9 (17): 2105–16. doi:10.1101/gad.9.17.2105. PMID 7657163.
Vanjski linkovi
[uredi | uredi izvor]- BMPedia - the Bone Morphogenetic Protein Wiki[trajno mrtav link]
- BMP4 lokacija ljudskog genoma UCSC Genome Browser.
BMP4 detalji ljudskog genoma u UCSC Genome Browser.



