MTR (gen)
Metionin-sintaza znana i kao MS, MeSe, MTR osdgovorna za regeneraciju metionina iz homocisteina. To jest protein koji je kod ljudi kodiran genom MTR (5-metiltetrahidrofolat-homocistein metiltransferaza) sa hromosoma 1.[5][6] Metionin-sintaza čini dio ciklusa S-adenozilmetionina (SAMe) biosinteze i regeneracije.[7] Kod životinja ovaj enzim zahtijeva Vitamin B12 (kobalamin) kao kofaktor, dok je oblik koji se nalazi u biljkama neovisan o kobalaminu.[8] Mikroorganizmi eksprimiraju oblike zavisne i nezavisne od kobalamina.[8]
Aminokiselinska sekvenca[uredi | uredi izvor]
Dužina polipeptidnog lanca je 1 265 aminokiselina, a molekulska težina 140 527 Da.[9]
| 10 | 20 | 30 | 40 | 50 | ||||
|---|---|---|---|---|---|---|---|---|
| MSPALQDLSQ | PEGLKKTLRD | EINAILQKRI | MVLDGGMGTM | IQREKLNEEH | ||||
| FRGQEFKDHA | RPLKGNNDIL | SITQPDVIYQ | IHKEYLLAGA | DIIETNTFSS | ||||
| TSIAQADYGL | EHLAYRMNMC | SAGVARKAAE | EVTLQTGIKR | FVAGALGPTN | ||||
| KTLSVSPSVE | RPDYRNITFD | ELVEAYQEQA | KGLLDGGVDI | LLIETIFDTA | ||||
| NAKAALFALQ | NLFEEKYAPR | PIFISGTIVD | KSGRTLSGQT | GEGFVISVSH | ||||
| GEPLCIGLNC | ALGAAEMRPF | IEIIGKCTTA | YVLCYPNAGL | PNTFGDYDET | ||||
| PSMMAKHLKD | FAMDGLVNIV | GGCCGSTPDH | IREIAEAVKN | CKPRVPPATA | ||||
| FEGHMLLSGL | EPFRIGPYTN | FVNIGERCNV | AGSRKFAKLI | MAGNYEEALC | ||||
| VAKVQVEMGA | QVLDVNMDDG | MLDGPSAMTR | FCNLIASEPD | IAKVPLCIDS | ||||
| SNFAVIEAGL | KCCQGKCIVN | SISLKEGEDD | FLEKARKIKK | YGAAMVVMAF | ||||
| DEEGQATETD | TKIRVCTRAY | HLLVKKLGFN | PNDIIFDPNI | LTIGTGMEEH | ||||
| NLYAINFIHA | TKVIKETLPG | ARISGGLSNL | SFSFRGMEAI | REAMHGVFLY | ||||
| HAIKSGMDMG | IVNAGNLPVY | DDIHKELLQL | CEDLIWNKDP | EATEKLLRYA | ||||
| QTQGTGGKKV | IQTDEWRNGP | VEERLEYALV | KGIEKHIIED | TEEARLNQKK | ||||
| YPRPLNIIEG | PLMNGMKIVG | DLFGAGKMFL | PQVIKSARVM | KKAVGHLIPF | ||||
| MEKEREETRV | LNGTVEEEDP | YQGTIVLATV | KGDVHDIGKN | IVGVVLGCNN | ||||
| FRVIDLGVMT | PCDKILKAAL | DHKADIIGLS | GLITPSLDEM | IFVAKEMERL | ||||
| AIRIPLLIGG | ATTSKTHTAV | KIAPRYSAPV | IHVLDASKSV | VVCSQLLDEN | ||||
| LKDEYFEEIM | EEYEDIRQDH | YESLKERRYL | PLSQARKSGF | QMDWLSEPHP | ||||
| VKPTFIGTQV | FEDYDLQKLV | DYIDWKPFFD | VWQLRGKYPN | RGFPKIFNDK | ||||
| TVGGEARKVY | DDAHNMLNTL | ISQKKLRARG | VVGFWPAQSI | QDDIHLYAEA | ||||
| AVPQAAEPIA | TFYGLRQQAE | KDSASTEPYY | CLSDFIAPLH | SGIRDYLGLF | ||||
| AVACFGVEEL | SKAYEDDGDD | YSSIMVKALG | DRLAEAFAEE | LHERVRRELW | ||||
| AYCGSEQLDV | ADLRRLRYKG | IRPAPGYPSQ | PDHTEKLTMW | RLADIEQSTG | ||||
| IRLTESLAMA | PASAVSGLYF | SNLKSKYFAV | GKISKDQVED | YALRKNISVA | ||||
| EVEKWLGPIL | GYDTD |
Struktura[uredi | uredi izvor]
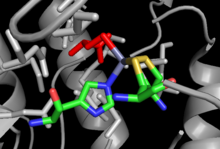
Riješene su kristalne strukture i za Meth-zavisni i za kob-zavisni, s malo sličnosti u cjelokupnoj strukturi uprkos identičnoj neto reakciji koju obavljaju oba i sličnosti unutar mjesta vezanja, kao što je Hcy vezujuće mjesto.[10] MetH ovisan o Cob podijeljen je u četiri odvojena domena: Aktivacija, kobalamin-vezujući domen (Cob domen), homocisteinsko vezivanje (Hcy domen) i N5-metilTHF vezivanje (MeTHF domen). Aktivaciona domena je mjesto interakcije sa metionin-sintaznom reduktazom i vezuje SAM koje se koristi kao dio ciklusa reaktivacije enzima. Cob domen sadrži Cob u sendviču između nekoliko velikih alfa-heliksa i vezan za enzim, tako da je atom kobalta iz grupe izložen kontaktu sa drugim domenima. Hcy domen sadrži kritično mjesto vezivanja cinka, koje se sastoji od ostataka cisteina ili histidina, koordiniranih sa ionom cinka koji može vezati Hcy, s primjerom iz MetH koji nije zavisan od Cob, prikazan na desnoj strani. N5-MeTHF vezujući domen sadrži konzervirani barel u kojem se N5-MeTHF može vezati putem vodika sa ostacima asparagina, arginina i asparaginske kiseline. Cijela struktura prolazi kroz dramatično ljuljanje tokom kataliza, dok se Cob domen pomiče naprijed-nazad od Hcy domena u Fol domen, prenoseći aktivnu metilnu grupu iz Fol u Hcy domen.[11]
Funkcija[uredi | uredi izvor]

Glavna funkcija metionin-sintaze je regeneracija Met u ciklusu S-adenozil metionina, koji u jednom prometu troši Met i ATP i stvara Hcy. Ovaj ciklus je kritičan jer se S-adenozil metionin uveliko koristi u biologiji kao izvor aktivne metil-grupe, pa tako metionin-sintaza služi esencijalnoj funkciji omogućavajući SAM ciklusu da traje bez stalnog priliva Met. Na ovaj način, metionin-sintaza služi i za održavanje niskih nivoa Hcy i, pošto je jedan od rijetkih enzima koji koriste N5-MeTHF kao supstrat, za indirektno održavanje nivoa THF.
U biljkama i mikroorganizmima, metioninsintaza služi dvostrukoj svrsi i održava SAM ciklus i katalizira završni sintetski korak u sintezi Met de novo. Iako je reakcija potpuno ista za oba procesa, ukupna funkcija razlikuje se od metionin -sintaze kod ljudi jer je Met esencijalna aminokiselina koja se ne sintetizira de novo u tijelu.[12]
Mehanizam[uredi | uredi izvor]

Metionin-sintaza katalizira završni korak u regeneraciji metionina (Met) iz homocisteina (Hcy). Ukupna reakcija transformiras 5-metiltetrahidrofolat (N5-MeTHF) u tetrahidrofolat (THF), dok prenosi metil-grupu u homocistein da bi se formirao metionin. Metionin-sintaza je jedini enzim sisara koji metabolizira N5-MeTHF, kako bi regenerirao aktivni kofaktor THF. Kod oblika enzima zavisnih od kobalamina, reakcija se odvija u dva koraka u ping-pong reakciji. Enzim se inicijalno dovodi u reaktivno stanje transferom metilne grupe sa N5-MeTHF na Co(I) u enzimski vezani kobalamin (Cob), formirajući metil-kobalamin (Me-Cob) koji sada sadrži Me-Co(III) i aktivira enzim. Zatim, Hcy, koji je koordinirao za enzim vezan cink da bi formirao reaktivni tiolat, reaguje sa Me-Cob. Aktivirana metilna grupa se prenosi sa Me-Cob na Hcy tiolat, koji regeneriše Co(I) u cob, a Met se oslobađa iz enzima. Mehanizam neovisan o Cobu slijedi isti opći put, ali s direktnom reakcijom između cink-tiolata i N5-MeTHF.[13][14]

Mehanizam enzima zavisi od konstantne regeneracije Co(I) u klipu, ali to nije uvek zagarantovano. Umjesto toga, svakih 1–2000 katalitičkih obrta, Co(I) može biti oksidiran u Co(II), što bi trajno ugasilo katalitičku aktivnost. Zaseban protein, metionin-sintazna reduktaza, katalizira regeneraciju Co(I) i obnavljanje enzimske aktivnosti. Budući da oksidacija cob-Co(I) neizbježno isključuje aktivnost metionin-sintaze zavisnu od Cob-a, defekti ili nedostaci metionin-sintazne reduktaze uključeni su u neke od asociranih bolesti za nedostatak metionin-sintaze o kojima se raspravlja u nastavku. Dva enzima formiraju mrežu čistača koja se vidi dolje lijevo.[15]
Genetika[uredi | uredi izvor]
Prema nekim izvorima, identificirano je nekoliko polimorfizama u MTR genu:
- 2756D→G (Asp919Gly)
Klinički značaj[uredi | uredi izvor]
Mutacije u genu MTR identificirane su kao osnovni uzrok nedostatka metilkobalaminu komplementarne grupe G ili nedostatka metilkobalamina cblG tipa.[5] Nedostatak ili deregulacija enzima zbog manjka metionin-sintazne reduktaze može direktno rezultirati kod povišenih nivoa homocisteina (hiperhomocisteinemija), što je povezano sa sljepoćom, neurološkim simptomima i urođenim defektima. Većina slučajeva nedostatka metionin-sintaze je simptomska u roku od dvije godine od rođenja sa mnogim pacijentima koji brzo razvijaju tešku encefalopatiju.[16] Jedna od posljedica smanjene aktivnosti metionin-sintaze koja se može mjeriti rutinskim kliničkim testovima krvi je megaloblastna anemija.
Također pogledajte[uredi | uredi izvor]
- Metiltransferaza
- Arakawinov sindrom II
- 5-Metiltetrahidrofolat (5-Me-THF, 5-Me-H4F, 5-MTHF)
- Betain-homocistein S-metiltransferaza
Reference[uredi | uredi izvor]
- ^ a b c GRCh38: Ensembl release 89: ENSG00000116984 - Ensembl, maj 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000021311 - Ensembl, maj 2017
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ a b "MTR 5-methyltetrahydrofolate-homocysteine methyltransferase (Homo sapiens)". Entrez. 19. 5. 2009. Pristupljeno 24. 5. 2009.
- ^ Li YN, Gulati S, Baker PJ, Brody LC, Banerjee R, Kruger WD (decembar 1996). "Cloning, mapping and RNA analysis of the human methionine synthase gene". Human Molecular Genetics. 5 (12): 1851–8. doi:10.1093/hmg/5.12.1851. PMID 8968735.
- ^ Banerjee RV, Matthews RG (mart 1990). "Cobalamin-dependent methionine synthase". FASEB Journal. 4 (5): 1450–9. doi:10.1096/fasebj.4.5.2407589. hdl:2027.42/154369. PMID 2407589. S2CID 8210250.
- ^ a b Zydowsky, T. M. (1986). "Stereochemical analysis of the methyl transfer catalyzed by cobalamin-dependent methionine synthase from Escherichia coli B". Journal of the American Chemical Society. 108 (11): 3152–3153. doi:10.1021/ja00271a081.
- ^ "UniProt, Q99707" (jezik: engleski). Pristupljeno 14. 12. 2021.
- ^ Pejchal R, Ludwig ML (februar 2005). "Cobalamin-independent methionine synthase (MetE): a face-to-face double barrel that evolved by gene duplication". PLOS Biology. 3 (2): e31. doi:10.1371/journal.pbio.0030031. PMC 539065. PMID 15630480.
- ^ Evans JC, Huddler DP, Hilgers MT, Romanchuk G, Matthews RG, Ludwig ML (mart 2004). "Structures of the N-terminal modules imply large domain motions during catalysis by methionine synthase". Proceedings of the National Academy of Sciences of the United States of America. 101 (11): 3729–36. Bibcode:2004PNAS..101.3729E. doi:10.1073/pnas.0308082100. PMC 374312. PMID 14752199.
- ^ Hesse H, Hoefgen R (juni 2003). "Molecular aspects of methionine biosynthesis". Trends in Plant Science. 8 (6): 259–62. doi:10.1016/S1360-1385(03)00107-9. PMID 12818659.
- ^ Zhang Z, Tian C, Zhou S, Wang W, Guo Y, Xia J, Liu Z, Wang B, Wang X, Golding BT, Griff RJ, Du Y, Liu J (decembar 2012). "Mechanism-based design, synthesis and biological studies of N⁵-substituted tetrahydrofolate analogs as inhibitors of cobalamin-dependent methionine synthase and potential anticancer agents". European Journal of Medicinal Chemistry. 58: 228–36. doi:10.1016/j.ejmech.2012.09.027. PMID 23124219.
- ^ Matthews, R. G.; Smith, A. E.; Zhou, Z. S.; Taurog, R. E.; Bandarian, V.; Evans, J. C.; Ludwig, M. (2003). "Cobalamin-Dependent and Cobalamin-Independent Methionine Synthases: Are There Two Solutions to the Same Chemical Problem?". Helvetica Chimica Acta. 86 (12): 3939. doi:10.1002/hlca.200390329.
- ^ Wolthers KR, Scrutton NS (juni 2007). "Protein interactions in the human methionine synthase-methionine synthase reductase complex and implications for the mechanism of enzyme reactivation". Biochemistry. 46 (23): 6696–709. doi:10.1021/bi700339v. PMID 17477549.
- ^ Outteryck O, de Sèze J, Stojkovic T, Cuisset JM, Dobbelaere D, Delalande S, Lacour A, Cabaret M, Lepoutre AC, Deramecourt V, Zéphir H, Fowler B, Vermersch P (juli 2012). "Methionine synthase deficiency: a rare cause of adult-onset leukoencephalopathy". Neurology. 79 (4): 386–8. doi:10.1212/WNL.0b013e318260451b. PMID 22786600. S2CID 207121496.
Dopunska literatura[uredi | uredi izvor]
- Ludwig ML, Matthews RG (1997). "Structure-based perspectives on B12-dependent enzymes". Annual Review of Biochemistry. 66: 269–313. doi:10.1146/annurev.biochem.66.1.269. PMID 9242908.
- Matthews RG, Sheppard C, Goulding C (april 1998). "Methylenetetrahydrofolate reductase and methionine synthase: biochemistry and molecular biology" (PDF). European Journal of Pediatrics. 157 Suppl 2: S54–9. doi:10.1007/PL00014305. PMID 9587027. S2CID 8709190.
- Garovic-Kocic V, Rosenblatt DS (august 1992). "Methionine auxotrophy in inborn errors of cobalamin metabolism". Clinical and Investigative Medicine. 15 (4): 395–400. PMID 1516297.
- O'Connor DL, Moriarty P, Picciano MF (1992). "The impact of iron deficiency on the flux of folates within the mammary gland". International Journal for Vitamin and Nutrition Research. Internationale Zeitschrift für Vitamin- und Ernährungsforschung. Journal International de Vitaminologie et de Nutrition. 62 (2): 173–80. PMID 1517041.
- Everman BW, Koblin DD (mart 1992). "Aging, chronic administration of ethanol, and acute exposure to nitrous oxide: effects on vitamin B12 and folate status in rats". Mechanisms of Ageing and Development. 62 (3): 229–43. doi:10.1016/0047-6374(92)90109-Q. PMID 1583909. S2CID 11766691.
- Vassiliadis A, Rosenblatt DS, Cooper BA, Bergeron JJ (august 1991). "Lysosomal cobalamin accumulation in fibroblasts from a patient with an inborn error of cobalamin metabolism (cblF complementation group): visualization by electron microscope radioautography". Experimental Cell Research. 195 (2): 295–302. doi:10.1016/0014-4827(91)90376-6. PMID 2070814.
- Li YN, Gulati S, Baker PJ, Brody LC, Banerjee R, Kruger WD (decembar 1996). "Cloning, mapping and RNA analysis of the human methionine synthase gene". Human Molecular Genetics. 5 (12): 1851–8. doi:10.1093/hmg/5.12.1851. PMID 8968735.
- Gulati S, Baker P, Li YN, Fowler B, Kruger W, Brody LC, Banerjee R (decembar 1996). "Defects in human methionine synthase in cblG patients". Human Molecular Genetics. 5 (12): 1859–65. doi:10.1093/hmg/5.12.1859. PMID 8968736.
- Leclerc D, Campeau E, Goyette P, Adjalla CE, Christensen B, Ross M, Eydoux P, Rosenblatt DS, Rozen R, Gravel RA (decembar 1996). "Human methionine synthase: cDNA cloning and identification of mutations in patients of the cblG complementation group of folate/cobalamin disorders". Human Molecular Genetics. 5 (12): 1867–74. doi:10.1093/hmg/5.12.1867. PMID 8968737.
- Chen LH, Liu ML, Hwang HY, Chen LS, Korenberg J, Shane B (februar 1997). "Human methionine synthase. cDNA cloning, gene localization, and expression". The Journal of Biological Chemistry. 272 (6): 3628–34. doi:10.1074/jbc.272.6.3628. PMID 9013615.
- Wilson A, Leclerc D, Saberi F, Campeau E, Hwang HY, Shane B, Phillips JA, Rosenblatt DS, Gravel RA (august 1998). "Functionally null mutations in patients with the cblG-variant form of methionine synthase deficiency". American Journal of Human Genetics. 63 (2): 409–14. doi:10.1086/301976. PMC 1377317. PMID 9683607.
- Salomon O, Rosenberg N, Zivelin A, Steinberg DM, Kornbrot N, Dardik R, Inbal A, Seligsohn U (2002). "Methionine synthase A2756G and methylenetetrahydrofolate reductase A1298C polymorphisms are not risk factors for idiopathic venous thromboembolism". The Hematology Journal. 2 (1): 38–41. doi:10.1038/sj.thj.6200078. PMID 11920232.
- Watkins D, Ru M, Hwang HY, Kim CD, Murray A, Philip NS, Kim W, Legakis H, Wai T, Hilton JF, Ge B, Doré C, Hosack A, Wilson A, Gravel RA, Shane B, Hudson TJ, Rosenblatt DS (juli 2002). "Hyperhomocysteinemia due to methionine synthase deficiency, cblG: structure of the MTR gene, genotype diversity, and recognition of a common mutation, P1173L". American Journal of Human Genetics. 71 (1): 143–53. doi:10.1086/341354. PMC 384971. PMID 12068375.
- De Marco P, Calevo MG, Moroni A, Arata L, Merello E, Finnell RH, Zhu H, Andreussi L, Cama A, Capra V (2002). "Study of MTHFR and MS polymorphisms as risk factors for NTD in the Italian population". Journal of Human Genetics. 47 (6): 319–24. doi:10.1007/s100380200043. PMID 12111380.
- Doolin MT, Barbaux S, McDonnell M, Hoess K, Whitehead AS, Mitchell LE (novembar 2002). "Maternal genetic effects, exerted by genes involved in homocysteine remethylation, influence the risk of spina bifida". American Journal of Human Genetics. 71 (5): 1222–6. doi:10.1086/344209. PMC 385102. PMID 12375236.
- Zhu H, Wicker NJ, Shaw GM, Lammer EJ, Hendricks K, Suarez L, Canfield M, Finnell RH (mart 2003). "Homocysteine remethylation enzyme polymorphisms and increased risks for neural tube defects". Molecular Genetics and Metabolism. 78 (3): 216–21. doi:10.1016/S1096-7192(03)00008-8. PMID 12649067.
Vanjski linkovi[uredi | uredi izvor]
- GeneReviews/NCBI/NIH/UW entry on Disorders of Intracellular Cobalamin Metabolism
- ENZYME: EC 2.1.1.13 Arhivirano 22. 6. 2011. na Wayback Machine
- 5-Methyltetrahydrofolate-Homocysteine S-Methyltransferase na US National Library of Medicine Medical Subject Headings (MeSH)





