Progesteron
| Progesteron | |
|---|---|
  | |
| Općenito | |
| Hemijski spoj | Progesteron |
| Molekularna formula | C=21 H=30 O=2 C21H30o2 |
| CAS registarski broj | 57-83-0 |
| SMILES | O=C4\C=C2/[C@]([C@H]1CC[C@@]3([C@@H](C(=O)C)CC[C@H]3[C@@H]1CC2)C)(C)CC4 |
| InChI | 1/C21H30O2/c1-13(22)17-6-7-18-16-5-4-14-12-15(23) 8-10-20(14,2)19(16)9-11-21(17,18) 3/h12,16-19H,4-11H2,1-3H3/t16-,17+,18-,19-,20-,21+/m0/s1 |
| Kratki opis | Produžena apsorpcija |
| Osobine1 | |
| Molarna masa | 314.46 |
| Tačka topljenja | 126 |
| Rastvorljivost | Rastvorljiv, polu-život: približno 25-50 sati |
| Rizičnost | |
| NFPA 704 | |
| 1 Gdje god je moguće korištene su SI jedinice. Ako nije drugačije naznačeno, dati podaci vrijede pri standardnim uslovima. | |
Progesteron ili P4 (pregn-4-en-3,20-dion) je C-21 steroidni hormon koji učestvuje u ženskom menstruacijskom ciklusu, pomaganju trudnoće i embriogeneze čovjeka i drugih vrsta sisara.[1][2]
Progesteron pripada progestogenskoj klasi hormona. Glavni prirodni predstavnik ljudskih progestogena. Proizvodi se od biljaka porodice jam povrća, u koje spada i balkanska dioskoreja (Dioscorea balcanica). Ove biljke proizvode velike količine steroida diosgenina, koji se laboratorijski pretvara u progesteron.
Otkriće i hemijski sasatav
[uredi | uredi izvor]Progesteron su međusobno nezavisno otkrile četiri grupe istraživača.[3][4][5][6]
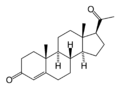
Kao i ostali steroidi, progesteron se sastoji od četiri međusobno kondenzirana ciklična ugljikovodika. Sadrži ketonsku funkcijsku grupu, kao i dvije metilne grane. Poput svih steroidnih hormona, hidrofoban je.
Sinteza
[uredi | uredi izvor]Biosinteza
[uredi | uredi izvor]
Dolje: Progesteron je važan u sintezu aldosterona (mineralokortikoida), kao što je 17-hidroksiprogesteron za kortizol (glukokortikoid), i androstendion za spolne steroide.
Kod životinja, progesteron (6), kao i svi drugi steroidni hormoni, sintetiziran se iz pregnenolona (3), koji je izveden iz holesterola (1). Holesterol (1) se dvostruko oksidira, dajući 20,22-dihidroksiholesterol (2). Ovaj vicinski diol se zatim oksidira uz gubitak bočnog lanca počevši od pozicije C-22 i formira pregnenolon (3). Ova reakcija je katalizirana Citohromom P450scc. Konverzija pregnenolona u progesteron se odvija u dva koraka. Prvo, 3-hidroksilna grupa oksidira u keto grupu (4), a zatim se dvostruka veza premješta na C-4, sa C-5 putem reakcije keto/enolne tautomerizacije.[7] Ovu reakciju katalizira 3-beta-HSD (3 beta-hidroksi steroid dehidrogenaza/delta(5)-delta(4)izomeraza). Progesteron je prekursor za mineralokortikoid aldosteron, a nakon pretvorbe do 17-hidroksi progesterona (još jednog prirodnog progestogena) u kortizol i androstendion. Androstendion se može konvertirati u testosteron, estron i estradiol. Kvasci imaju sposobnost sinteze i pregenolon i progesterona .[8]
Laboratorijska pretraga
[uredi | uredi izvor]

Rasel Earl Marker je razvio (1940.) ekonomičnu polusintezu progesterona iz biljnog steroida diosgenina izoliranog iz jama, za farmaceutsku kompaniju Parke-Davis. Poznata je kao Markerova degradacija. Objavljeno je i nekoliko drugih semi-sinteza koje počinju na raznim steroidima progesterona. Npr., kortizon se, primjenom jodotrimetilsilana, može simultano deoksigenirati na C-17 i C-21 pozicije, u hloroformu. Tako nastaje 11-keto-progesteron (ketogestin), koji se zatim reducira na pozicije-11 i daje progesteron.[11] Potpunu sintezu progesterona je objavio Wiliem Samer Johnson, 1971. Počinje reakcijom fosfonijum soli 7 sa fenil litijumom , što daje fosfonijum ilid 8. Ilid 8 reagira sa aldehidom i proizvodi alken 9. Ketalne zaštitne grupe 9 hidroliziraju pa nastaje diketon 10, koji se zatim ciklizira da bi se formirao ciklopentenon 11. Keton 11 reaguje sa metil litijumom i daje tercijarni alkohol 12, koji se onda tretira kiselinom, dajući tercijarni katjon 13. Ključni korak sinteze je ciklizacija π-kationa 13 u kojoj se B-, C-, i D-prstenovi steroida simultano oblikuju i proizvode 14. To liči na kationsku ciklizacijsku reakciju koja se primjenjuje u biosintezi steroida, po čemu se naziva biomimetikom. U slijedećem koraku enol ortoestar hidrolizira i proizvodi keton 15. Ciklopentenski A-prsten se otvara oksidacijom sa ozonom i daje 16. Na kraju, diketon 17 prolazi kroz intramolekulsku aldolnu kondenzaciju, primjenom vodenog rastvora kalij-hidroksida i nastaje progesteron.
Reference
[uredi | uredi izvor]- ^ Hall J. E., Guyton A. C. (2006): Textbook of medical physiology, 11th edition. Elsevier Saunders, St. Louis, Mo, ISBN 0-7216-0240-1.
- ^ Dewick P. M. (2002): Medicinal natural products: a biosynthetic approach. Wiley, ISBN 978-0-471-49641-0.
- ^ Allen W. M. (1935): The isolation of crystalline progestin. Science, 82 (2118): 89-93.
- ^ Butenandt A., Westphal U . (1934): Zur Isolierung und Charakterisierung des Corpusluteum-Hormons. Berichte Deutsche chemische Gesellschaft, 67: 1440-1442.
- ^ Hartmann M., Wettstein A. (1934): Ein krystallisiertes Hormon aus Corpus luteum. Helvetica Chimica Acta, 17: 878-882.
- ^ Slotta K. H., Ruschig H., Fels E. (1934): Reindarstellung der Hormone aus dem Corpusluteum. Berichte Deutsche chemische Gesellschaft, 67: 1270-1273.
- ^ Dewick, Paul M. (2002). Medicinal natural products: a biosynthetic approach. New York: Wiley. str. 244. ISBN 978-0-471-49641-0. CS1 održavanje: nepreporučeni parametar (link)
- ^ Duport C, Spagnoli R, Degryse E, Pompon D (1998.). "Self-sufficient biosynthesis of pregnenolone and progesterone in engineered yeast". Nat. Biotechnol. 16 (2): 186–9. Provjerite vrijednost datuma u parametru:
|year=(pomoć)CS1 održavanje: više imena: authors list (link) - ^ Marker RE, Krueger J (1940). "Sterols. CXII. Sapogenins. XLI. The Preparation of Trillin and its Conversion to Progesterone". J. Am. Chem. Soc. 62 (12): 3349–3350. doi:10.1021/ja01869a023.
- ^ Johnson WS, Gravestock MB, McCarry BE (1971). "Acetylenic bond participation in biogenetic-like olefinic cyclizations. II. Synthesis of dl-progesterone". J. Am. Chem. Soc. 93 (17): 4332–4.CS1 održavanje: više imena: authors list (link)
- ^ Numazawa M., Nagaoka M., Kunitama Y. (1986): Regiospecific deoxygenation of the dihydroxyacetone moiety at C-17 of corticoid steroids with iodotrimethylsilane. Chem. Pharm. Bull., 34 (9): 3722-3726: http://www.journalarchive.jst.go.jp/english/jnlabstract_en.php?cdjournal=cpb1958&cdvol=34&noissue=9&startpage=3722 Arhivirano 9. 12. 2012. na: Archive.today.
Vanjski linkovi
[uredi | uredi izvor]- Progesterone na US National Library of Medicine Medical Subject Headings (MeSH)
- https://web.archive.org/web/20080618062909/http://users.rcn.com/jkimball.ma.ultranet/BiologyPages/P/Progesterone.html: Progesterone
- http://www.pms-menopause-progesterone.org/progesterone/ Arhivirano 4. 3. 2016. na Wayback Machine : Progesterone Resource Center *http://www.lawleybasecamp.com/media/pdf/condition-booklets/Progesterone_Booklet.pdf
