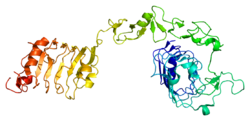Receptor insulinolikog faktora rasta 1
Receptor Insulinolikog faktora rasta 1 (IGF-1) jest protein ćelijske površine koji je kod ljudi kodiran genom IGF-1 sa hromosoma 15. To je transmembranski receptor koji se aktivira hormonom koji se zove insulinoliki faktor rasta 1 (IGF-1) i srodnim hormonom zvanim IGF-2. Pripada velikoj klasi tirozin-kinaznih receptora. Ovaj receptor posreduje u efektima IGF-1, koji je polipeptidni proteinski hormon, po molekulskoj sličan strukturi insulinu. IGF-1 ima važnu ulogu u rastu i nastavlja da ima anaboličke efekte kod odraslih – što znači da može izazvati hipertrofiju skeletnih mišića i drugih ciljnih tkiva. Miševi kojima nedostaje receptor IGF-1 uginu kasno u razvoju i pokazuju dramatično smanjenje tjelesne mase. Ovo svedoči o snažnom dejstvu ovog receptora koji podstiče rast.
Struktura[uredi | uredi izvor]

Dvije alfa podjedinice i dvije beta podjedinice čine IGF-1 receptor. I α i β podjedinice se sintetiziraju iz jednog prekursora iRNK. Prekursor je zatim glikoziliran, proteolitski cijepan i umrežen cisteinskim vezama kako bi se formirao funkcionalni transmembranski αβ lanac.[5] α lanci se nalaze ekstracelularno, dok β podjedinica pokriva membranu i odgovorna je za intracelularnu transdukciju signala nakon stimulacije liganda. Zreli IGF-1R ima molekularnu težinu od približno 320 kDa.[1] Receptor je član porodice koja se sastoji od insulinski receptor i IGF-2R (i njihovi odgovarajući ligandi IGF-1 i IGF-2), zajedno sa nekoliko proteina koji se vezuju za IGF.
IGF-1R i insulinski receptor imaju vezujuće mjesto za ATP, koji se koristi za obezbeđivanje fosfata za autofosforilaciju. Postoji 60% homologije između IGF-1R i insulinskog receptora. Strukture autofosforilacionih kompleksa tirozinskih ostataka 1.165 i 1.166 identifikovane su unutar kristalnog domena kinaze IGF1R.[6]
Kao odgovor na vezivanje liganda, α lanci indukuju autofosforilaciju tirozina β lanaca. Ovaj događaj pokreće kaskadu unutarćelijske signalizacije koja, iako je specifična za tip ćelije, često podstiče preživljavanje i proliferaciju ćelije.[7][8]
Članovi porodice[uredi | uredi izvor]
Receptori tirozin-kinaze, uključujući receptor IGF-1, posreduju u njihovoj aktivnosti izazivajući dodavanje fosfatne grupe određenim tirozinima na određene proteine unutar ćelije. Ovaj dodatak fosfata indukuje takozvane kaskade "ćelijske signalizacije" - a uobičajeni rezultat aktivacije IGF-1 receptora je preživljavanje i proliferacija u ćelijama kompetentnim za mitozu i rast (hipertrofija) u tkivima kao što je skeletni i srčani mišić.
Aminokiselinska sekvenca[uredi | uredi izvor]
Dužina polipeptidnog lanca je 1.367 aminokiseline, a molekulska težina 154.793 Da.[7]
| 10 | 20 | 30 | 40 | 50 | ||||
|---|---|---|---|---|---|---|---|---|
| MKSGSGGGSP | TSLWGLLFLS | AALSLWPTSG | EICGPGIDIR | NDYQQLKRLE | ||||
| NCTVIEGYLH | ILLISKAEDY | RSYRFPKLTV | ITEYLLLFRV | AGLESLGDLF | ||||
| PNLTVIRGWK | LFYNYALVIF | EMTNLKDIGL | YNLRNITRGA | IRIEKNADLC | ||||
| YLSTVDWSLI | LDAVSNNYIV | GNKPPKECGD | LCPGTMEEKP | MCEKTTINNE | ||||
| YNYRCWTTNR | CQKMCPSTCG | KRACTENNEC | CHPECLGSCS | APDNDTACVA | ||||
| CRHYYYAGVC | VPACPPNTYR | FEGWRCVDRD | FCANILSAES | SDSEGFVIHD | ||||
| GECMQECPSG | FIRNGSQSMY | CIPCEGPCPK | VCEEEKKTKT | IDSVTSAQML | ||||
| QGCTIFKGNL | LINIRRGNNI | ASELENFMGL | IEVVTGYVKI | RHSHALVSLS | ||||
| FLKNLRLILG | EEQLEGNYSF | YVLDNQNLQQ | LWDWDHRNLT | IKAGKMYFAF | ||||
| NPKLCVSEIY | RMEEVTGTKG | RQSKGDINTR | NNGERASCES | DVLHFTSTTT | ||||
| SKNRIIITWH | RYRPPDYRDL | ISFTVYYKEA | PFKNVTEYDG | QDACGSNSWN | ||||
| MVDVDLPPNK | DVEPGILLHG | LKPWTQYAVY | VKAVTLTMVE | NDHIRGAKSE | ||||
| ILYIRTNASV | PSIPLDVLSA | SNSSSQLIVK | WNPPSLPNGN | LSYYIVRWQR | ||||
| QPQDGYLYRH | NYCSKDKIPI | RKYADGTIDI | EEVTENPKTE | VCGGEKGPCC | ||||
| ACPKTEAEKQ | AEKEEAEYRK | VFENFLHNSI | FVPRPERKRR | DVMQVANTTM | ||||
| SSRSRNTTAA | DTYNITDPEE | LETEYPFFES | RVDNKERTVI | SNLRPFTLYR | ||||
| IDIHSCNHEA | EKLGCSASNF | VFARTMPAEG | ADDIPGPVTW | EPRPENSIFL | ||||
| KWPEPENPNG | LILMYEIKYG | SQVEDQRECV | SRQEYRKYGG | AKLNRLNPGN | ||||
| YTARIQATSL | SGNGSWTDPV | FFYVQAKTGY | ENFIHLIIAL | PVAVLLIVGG | ||||
| LVIMLYVFHR | KRNNSRLGNG | VLYASVNPEY | FSAADVYVPD | EWEVAREKIT | ||||
| MSRELGQGSF | GMVYEGVAKG | VVKDEPETRV | AIKTVNEAAS | MRERIEFLNE | ||||
| ASVMKEFNCH | HVVRLLGVVS | QGQPTLVIME | LMTRGDLKSY | LRSLRPEMEN | ||||
| NPVLAPPSLS | KMIQMAGEIA | DGMAYLNANK | FVHRDLAARN | CMVAEDFTVK | ||||
| IGDFGMTRDI | YETDYYRKGG | KGLLPVRWMS | PESLKDGVFT | TYSDVWSFGV | ||||
| VLWEIATLAE | QPYQGLSNEQ | VLRFVMEGGL | LDKPDNCPDM | LFELMRMCWQ | ||||
| YNPKMRPSFL | EIISSIKEEM | EPGFREVSFY | YSEENKLPEP | EELDLEPENM | ||||
| ESVPLDPSAS | SSSLPLPDRH | SGHKAENGPG | PGVLVLRASF | DERQPYAHMN | ||||
| GGRKNERALP | LPQSSTC |
Funkcija[uredi | uredi izvor]
Embrionski razvoj[uredi | uredi izvor]
Tokom embrionskog razvoja, put IGF-1R je uključen u pupoljke udova koji se razvijaju.
Dojenje[uredi | uredi izvor]
IGFR signalni put je od ključnog značaja za normalan razvoj tkiva mliječne žlijezde tokom trudnoća i dojenja. Tokom trudnoće dolazi do intenzivne proliferacije epitelnih ćelija koje formiraju kanal i tkivo žlijezde. Nakon odbijanja, ćelije prolaze kroz apoptozu i svo tkivo je uništeno. Nekoliko faktora rasta i hormona uključeno je u ovaj ukupni proces, a vjeruje se da IGF-1R ima ulogu u diferencijaciji ćelija i ključnu ulogu u inhibiciji apoptoze dok se odvikavanje ne završi.
Insulinska signalizacija[uredi | uredi izvor]
IGF-1 se vezuje za najmanje dva receptora ćelijske površine: IGF1 receptor (IGFR) i insulinski receptor. Čini se da je IGF-1 receptor "fiziološki" receptor - on veže IGF-1 sa znatno većim afinitetom nego što veže insulin.[9] Poput insulinskog receptora, receptor IGF-1 je receptor tirozin kinaze—što znači da signalizira izazivanjem dodavanja molekula fosfata na određene tirozine. IGF-1 aktivira insulinski receptor na približno 10% jačine insulina. Dio ove signalizacije može biti putem heterodimera IGF1R/insulinskih receptora (razlog za konfuziju je to što studije vezivanja pokazuju da IGF-1 veže inzulinski receptor 100 puta slabije od insulina, ali to nije u korelaciji sa stvarnom snagom IGF-a -1 in vivo kod izazivanja fosforilacije insulinskog receptora i hipoglikemije).
Starenje[uredi | uredi izvor]
Studije na ženkama miševa su pokazale da i supraočno jezgro (SON) i parakomorsko jezgro (PVN) gube otprilike jednu trećinu imunoreaktivnih ćelija IGF-1R normalnim starenjem. Također, stari miševi sa kalorijskim ograničenjem (CR) izgubili su veći broj neimunoreaktivnih IGF-1R ćelija dok su zadržali sličan broj IGF-1R imunoreaktivnih ćelija u poređenju sa starim Al miševima. Shodno tome, stari-CR miševi pokazuju veći procent imunoreaktivnih ćelija IGF-1R, što odražava povećanu osetljivost hipotalamusa na IGF-1 u poređenju sa miševima koji normalno stare.[10][11]
Kraniosinostoza[uredi | uredi izvor]
Mutacije u IGF1R su povezane sa kraniosinostozom.[12]
Veličina tijela[uredi | uredi izvor]
Pokazalo se da IGF-1R ima značajan uticaj na veličinu tijela kod malih pasmina pasa.[13] "Nesinonimni SNP na hr3:44,706,389 koji mijenja visoko konzervirani arginin na aminokiselini 204 u histidin" povezuje se s posebno malom veličinom tijela. "Predviđa se da će ova mutacija spriječiti stvaranje nekoliko vodikovih veza unutar domena bogatog cisteinom vanćelijske podjedinice receptora koja veže ligand. Devet od 13 sićušnih pasmina pasa nosi mutaciju i mnogi psi su homozigoti za nju." Pokazalo se da i manje jedinke unutar nekoliko malih i srednjih rasa nose ovu mutaciju.
Miševi koji nose samo jednu funkcionalnu kopiju IGF-1R su normalni, ali pokazuju smanjenje tjelesne mase od ~15%. Takođe se pokazalo da IGF-1R reguliše veličinu tijela kod pasa. Mutirana verzija ovog gena nalazi se u nizu malih pasmina pasa.[13]
Inaktivacija/delecija gena[uredi | uredi izvor]
Delecija gena za receptor IGF-1 kod miševa dovodi do smrtonosnosti tokom ranog embrionskog razvoja, i iz tog razloga, neosetljivost na IGF-1, za razliku od slučaja neosetljivosti na hormon rasta (GH) (Laronov sindrom), nije uočen u ljudskoj populaciji.[14]
Klinički značaj[uredi | uredi izvor]
Rak[uredi | uredi izvor]
IGF-1R je uključen u nekoliko karcinoma,[15][16] uključujući rak dojke, prostate i pluća. U nekim slučajevima njegova antiapoptotska svojstva omogućavaju ćelijama raka da se odupru citotoksičnim svojstvima hemoterapeutskih lijekova ili radioterapije. Kod raka dojke, gdje se inhibitori EGFR kao što je erlotinib koriste za inhibiciju signalnog puta EGFR-a. IGF-1R daje rezistenciju formiranjem jedne polovine heterodimera (vidi opis Transdukcija EGFR signala na stranici erlotinib), omogućavajući da se EGFR signalizacija nastavi u prisustvu odgovarajućeg inhibitora. Ovaj proces se naziva preslušavanjem između EGFR i IGF-1R. Dalje je impliciran u raku dojke povećanjem metastatskog potencijala originalnog tumora dajući sposobnost promicanja vaskularizacije.
Povećani nivoi IGF-IR su izraženi u većini primarnih i metastatskih tumora pacijenata sa karcinomom prostate.[17] Dokazi sugeriraju da je IGF-IR signalizacija potrebna za preživljavanje i rast kada ćelije raka prostate napreduju do nezavisnosti od androgena.[18] Osim toga, kada se ovjekovečene ćelije raka prostate koje oponašaju uznapredovalu bolest tretiraju ligandom IGF-1R, IGF-1, ćelije postaju pokretljivije.[19] Čini se da su članovi porodice IGF receptora i njihovi ligandi također uključeni u kancerogenezu tumora dojke kod pasa.[20][21] IGF1R se pojačava u nekoliko tipova raka na osnovu analize TCGA podataka, a amplifikacija gena bi mogla biti jedan mehanizam za prekomjernu ekspresiju IGF1R kod raka.[22]
Ćelije raka pluća stimulirane pomoću glukokortikoida su inducirane u reverzibilno stanje mirovanja koje je ovisilo o IGF-1R i njegovim pratećim signalnim putevima preživljavanja.[23]
Inhibitori[uredi | uredi izvor]
Zbog sličnosti struktura IGF-1R i insulinskog receptora (IR), posebno u regionima mjesta vezanja ATP i regiona tirozin kinaze, sinteza selektivnih inhibitora IGF-1R je teška. U sadašnjim istraživanjima istaknute su tri glavne klase inhibitora:
- Tirfostin kao što je AG538[24] i AG1024. Oni su u ranom pretkliničkom testiranju. Ne smatra se da su ATP-kompetitivni, iako se koriste u EGFR kao što je opisano u QSAR studijama. Oni pokazuju određenu selektivnost prema IGF-1R preko IR.
- Derivati pirolo(2,3-d)-pirimidina kao što je NVP-AEW541, koji je izumio Novartis, koji pokazuju daleko veću (100 puta) selektivnost prema IGF-1R u odnosu na IR.[25]
- Monoklonska antitijela su vjerovatno najspecifičniji i najperspektivniji terapeutski spojevi. Teprotumumab je nova terapija koja pokazuje značajnu korist za očne bolesti štitne žlijezde.
Interakcije[uredi | uredi izvor]
Nađeno je da receptor Insulinolikog faktora rasta 1 ima interakciju sa:
Regulacija[uredi | uredi izvor]
Postoje dokazi koji ukazuju na to da je IGF1R negativno reguliran putem mikroRNK miR-7.[42]
Također pogledajte[uredi | uredi izvor]
Reference[uredi | uredi izvor]
- ^ a b c GRCh38: Ensembl release 89: ENSG00000140443 - Ensembl, maj 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000005533 - Ensembl, maj 2017
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ Gregory CW, DeGeorges A, Sikes RA (2001). "The IGF axis in the development and progression of prostate cancer". Recent Research Developments in Cancer: 437–462. ISBN 81-7895-002-2.
- ^ Xu Q, Malecka KL, Fink L, Jordan EJ, Duffy E, Kolander S, Peterson JR, Dunbrack RL (decembar 2015). "Identifying three-dimensional structures of autophosphorylation complexes in crystals of protein kinases". Science Signaling. 8 (405): rs13. doi:10.1126/scisignal.aaa6711. PMC 4766099. PMID 26628682.
- ^ a b Jones JI, Clemmons DR (februar 1995). "Insulin-like growth factors and their binding proteins: biological actions". Endocrine Reviews. 16 (1): 3–34. doi:10.1210/edrv-16-1-3. PMID 7758431.
- ^ LeRoith D, Werner H, Beitner-Johnson D, Roberts CT (april 1995). "Molecular and cellular aspects of the insulin-like growth factor I receptor". Endocrine Reviews. 16 (2): 143–63. doi:10.1210/edrv-16-2-143. PMID 7540132.
- ^ Hawsawi Y, El-Gendy R, Twelves C, Speirs V, Beattie J (decembar 2013). "Insulin-like growth factor - oestradiol crosstalk and mammary gland tumourigenesis" (PDF). Biochimica et Biophysica Acta (BBA) - Reviews on Cancer. 1836 (2): 345–53. doi:10.1016/j.bbcan.2013.10.005. PMID 24189571.
- ^ Saeed O, Yaghmaie F, Garan SA, Gouw AM, Voelker MA, Sternberg H, Timiras PS (februar 2007). "Insulin-like growth factor-1 receptor immunoreactive cells are selectively maintained in the paraventricular hypothalamus of calorically restricted mice". International Journal of Developmental Neuroscience. 25 (1): 23–8. doi:10.1016/j.ijdevneu.2006.11.004. PMID 17194562. S2CID 5828689.
- ^ Yaghmaie F, Saeed O, Garan SA, Voelker MA, Gouw AM, Freitag W, Sternberg H, Timiras PS (novembar 2006). "Age-dependent loss of insulin-like growth factor-1 receptor immunoreactive cells in the supraoptic hypothalamus is reduced in calorically restricted mice". International Journal of Developmental Neuroscience. 24 (7): 431–6. doi:10.1016/j.ijdevneu.2006.08.008. PMID 17034982. S2CID 22533403.
- ^ Cunningham ML, Horst JA, Rieder MJ, Hing AV, Stanaway IB, Park SS, Samudrala R, Speltz ML (januar 2011). "IGF1R variants associated with isolated single suture craniosynostosis". American Journal of Medical Genetics. Part A. 155A (1): 91–7. doi:10.1002/ajmg.a.33781. PMC 3059230. PMID 21204214.
- ^ a b Hoopes BC, Rimbault M, Liebers D, Ostrander EA, Sutter NB (decembar 2012). "The insulin-like growth factor 1 receptor (IGF1R) contributes to reduced size in dogs". Mammalian Genome. 23 (11–12): 780–90. doi:10.1007/s00335-012-9417-z. PMC 3511640. PMID 22903739.
- ^ Harris JR, Lippman ME, Osborne CK, Morrow M (28. 3. 2012). Diseases of the Breast. Lippincott Williams & Wilkins. str. 88–. ISBN 978-1-4511-4870-1.
- ^ Warshamana-Greene GS, Litz J, Buchdunger E, García-Echeverría C, Hofmann F, Krystal GW (februar 2005). "The insulin-like growth factor-I receptor kinase inhibitor, NVP-ADW742, sensitizes small cell lung cancer cell lines to the effects of chemotherapy". Clinical Cancer Research. 11 (4): 1563–71. doi:10.1158/1078-0432.CCR-04-1544. PMID 15746061.
- ^ Jones HE, Goddard L, Gee JM, Hiscox S, Rubini M, Barrow D, Knowlden JM, Williams S, Wakeling AE, Nicholson RI (decembar 2004). "Insulin-like growth factor-I receptor signalling and acquired resistance to gefitinib (ZD1839; Iressa) in human breast and prostate cancer cells". Endocrine-Related Cancer. 11 (4): 793–814. doi:10.1677/erc.1.00799. hdl:11392/523178. PMID 15613453. S2CID 19466790.
- ^ Hellawell GO, Turner GD, Davies DR, Poulsom R, Brewster SF, Macaulay VM (maj 2002). "Expression of the type 1 insulin-like growth factor receptor is up-regulated in primary prostate cancer and commonly persists in metastatic disease". Cancer Research. 62 (10): 2942–50. PMID 12019176.
- ^ Krueckl SL, Sikes RA, Edlund NM, Bell RH, Hurtado-Coll A, Fazli L, Gleave ME, Cox ME (decembar 2004). "Increased insulin-like growth factor I receptor expression and signaling are components of androgen-independent progression in a lineage-derived prostate cancer progression model". Cancer Research. 64 (23): 8620–9. doi:10.1158/0008-5472.CAN-04-2446. PMID 15574769.
- ^ Yao H, Dashner EJ, van Golen CM, van Golen KL (april 2006). "RhoC GTPase is required for PC-3 prostate cancer cell invasion but not motility". Oncogene. 25 (16): 2285–96. doi:10.1038/sj.onc.1209260. PMID 16314838.
- ^ Klopfleisch R, Hvid H, Klose P, da Costa A, Gruber AD (decembar 2010). "Insulin receptor is expressed in normal canine mammary gland and benign adenomas but decreased in metastatic canine mammary carcinomas similar to human breast cancer". Veterinary and Comparative Oncology. 8 (4): 293–301. doi:10.1111/j.1476-5829.2009.00232.x. PMID 21062411.
- ^ Klopfleisch R, Lenze D, Hummel M, Gruber AD (novembar 2010). "Metastatic canine mammary carcinomas can be identified by a gene expression profile that partly overlaps with human breast cancer profiles". BMC Cancer. 10: 618. doi:10.1186/1471-2407-10-618. PMC 2994823. PMID 21062462.
- ^ Chen Y, McGee J, Chen X, Doman TN, Gong X, Zhang Y, Hamm N, Ma X, Higgs RE, Bhagwat SV, Buchanan S, Peng SB, Staschke KA, Yadav V, Yue Y, Kouros-Mehr H (2014). "Identification of druggable cancer driver genes amplified across TCGA datasets". PLOS ONE. 9 (5): e98293. Bibcode:2014PLoSO...998293C. doi:10.1371/journal.pone.0098293. PMC 4038530. PMID 24874471.
- ^ Prekovic S, Schuurman K, Mayayo-Peralta I, Manjón AG, Buijs M, Yavuz S, Wellenstein MD, Barrera A, Monkhorst K, Huber A, Morris B (juli 2021). "Glucocorticoid receptor triggers a reversible drug-tolerant dormancy state with acquired therapeutic vulnerabilities in lung cancer". Nature Communications. 12 (1): 4360. Bibcode:2021NatCo..12.4360P. doi:10.1038/s41467-021-24537-3. PMC 8285479 Provjerite vrijednost parametra
|pmc=(pomoć). PMID 34272384 Provjerite vrijednost parametra|pmid=(pomoć). - ^ Blum G, Gazit A, Levitzki A (decembar 2000). "Substrate competitive inhibitors of IGF-1 receptor kinase". Biochemistry. 39 (51): 15705–12. doi:10.1021/bi001516y. PMID 11123895.
- ^ "Archived copy" (PDF). Arhivirano s originala (PDF), 4. 3. 2016. Pristupljeno 18. 7. 2012.CS1 održavanje: arhivirana kopija u naslovu (link)
- ^ Taya S, Inagaki N, Sengiku H, Makino H, Iwamatsu A, Urakawa I, Nagao K, Kataoka S, Kaibuchi K (novembar 2001). "Direct interaction of insulin-like growth factor-1 receptor with leukemia-associated RhoGEF". The Journal of Cell Biology. 155 (5): 809–20. doi:10.1083/jcb.200106139. PMC 2150867. PMID 11724822.
- ^ Arbet-Engels C, Tartare-Deckert S, Eckhart W (februar 1999). "C-terminal Src kinase associates with ligand-stimulated insulin-like growth factor-I receptor". The Journal of Biological Chemistry. 274 (9): 5422–8. doi:10.1074/jbc.274.9.5422. PMID 10026153.
- ^ a b c Sehat B, Andersson S, Girnita L, Larsson O (juli 2008). "Identification of c-Cbl as a new ligase for insulin-like growth factor-I receptor with distinct roles from Mdm2 in receptor ubiquitination and endocytosis". Cancer Research. 68 (14): 5669–77. doi:10.1158/0008-5472.CAN-07-6364. PMID 18632619.
- ^ Rotem-Yehudar R, Galperin E, Horowitz M (august 2001). "Association of insulin-like growth factor 1 receptor with EHD1 and SNAP29". The Journal of Biological Chemistry. 276 (35): 33054–60. doi:10.1074/jbc.M009913200. PMID 11423532.
- ^ a b Vecchione A, Marchese A, Henry P, Rotin D, Morrione A (maj 2003). "The Grb10/Nedd4 complex regulates ligand-induced ubiquitination and stability of the insulin-like growth factor I receptor". Molecular and Cellular Biology. 23 (9): 3363–72. doi:10.1128/mcb.23.9.3363-3372.2003. PMC 153198. PMID 12697834.
- ^ a b c Dey BR, Frick K, Lopaczynski W, Nissley SP, Furlanetto RW (juni 1996). "Evidence for the direct interaction of the insulin-like growth factor I receptor with IRS-1, Shc, and Grb10". Molecular Endocrinology. 10 (6): 631–41. doi:10.1210/mend.10.6.8776723. PMID 8776723.
- ^ He W, Rose DW, Olefsky JM, Gustafson TA (mart 1998). "Grb10 interacts differentially with the insulin receptor, insulin-like growth factor I receptor, and epidermal growth factor receptor via the Grb10 Src homology 2 (SH2) domain and a second novel domain located between the pleckstrin homology and SH2 domains". The Journal of Biological Chemistry. 273 (12): 6860–7. doi:10.1074/jbc.273.12.6860. PMID 9506989.
- ^ Morrione A, Valentinis B, Li S, Ooi JY, Margolis B, Baserga R (juli 1996). "Grb10: A new substrate of the insulin-like growth factor I receptor". Cancer Research. 56 (14): 3165–7. PMID 8764099.
- ^ a b Mañes S, Mira E, Gómez-Mouton C, Zhao ZJ, Lacalle RA, Martínez-A C (april 1999). "Concerted activity of tyrosine phosphatase SHP-2 and focal adhesion kinase in regulation of cell motility". Molecular and Cellular Biology. 19 (4): 3125–35. doi:10.1128/mcb.19.4.3125. PMC 84106. PMID 10082579.
- ^ a b Tartare-Deckert S, Sawka-Verhelle D, Murdaca J, Van Obberghen E (oktobar 1995). "Evidence for a differential interaction of SHC and the insulin receptor substrate-1 (IRS-1) with the insulin-like growth factor-I (IGF-I) receptor in the yeast two-hybrid system". The Journal of Biological Chemistry. 270 (40): 23456–60. doi:10.1074/jbc.270.40.23456. PMID 7559507.
- ^ Mothe I, Delahaye L, Filloux C, Pons S, White MF, Van Obberghen E (decembar 1997). "Interaction of wild type and dominant-negative p55PIK regulatory subunit of phosphatidylinositol 3-kinase with insulin-like growth factor-1 signaling proteins" (PDF). Molecular Endocrinology. 11 (13): 1911–23. doi:10.1210/mend.11.13.0029. PMID 9415396. Arhivirano s originala (PDF), 16. 6. 2022. Pristupljeno 11. 4. 2023.
- ^ a b Seely BL, Reichart DR, Staubs PA, Jhun BH, Hsu D, Maegawa H, Milarski KL, Saltiel AR, Olefsky JM (august 1995). "Localization of the insulin-like growth factor I receptor binding sites for the SH2 domain proteins p85, Syp, and GTPase activating protein". The Journal of Biological Chemistry. 270 (32): 19151–7. doi:10.1074/jbc.270.32.19151. PMID 7642582.
- ^ Santen RJ, Song RX, Zhang Z, Kumar R, Jeng MH, Masamura A, Lawrence J, Berstein L, Yue W (juli 2005). "Long-term estradiol deprivation in breast cancer cells up-regulates growth factor signaling and enhances estrogen sensitivity". Endocrine-Related Cancer. 12. 12 Suppl 1: S61-73. doi:10.1677/erc.1.01018. PMID 16113100. S2CID 18995886.
- ^ Dey BR, Spence SL, Nissley P, Furlanetto RW (septembar 1998). "Interaction of human suppressor of cytokine signaling (SOCS)-2 with the insulin-like growth factor-I receptor". The Journal of Biological Chemistry. 273 (37): 24095–101. doi:10.1074/jbc.273.37.24095. PMID 9727029.
- ^ Dey BR, Furlanetto RW, Nissley P (novembar 2000). "Suppressor of cytokine signaling (SOCS)-3 protein interacts with the insulin-like growth factor-I receptor". Biochemical and Biophysical Research Communications. 278 (1): 38–43. doi:10.1006/bbrc.2000.3762. PMID 11071852.
- ^ Craparo A, Freund R, Gustafson TA (april 1997). "14-3-3 (epsilon) interacts with the insulin-like growth factor I receptor and insulin receptor substrate I in a phosphoserine-dependent manner". The Journal of Biological Chemistry. 272 (17): 11663–9. doi:10.1074/jbc.272.17.11663. PMID 9111084.
- ^ Jiang L, Liu X, Chen Z, Jin Y, Heidbreder CE, Kolokythas A, Wang A, Dai Y, Zhou X (novembar 2010). "MicroRNA-7 targets IGF1R (insulin-like growth factor 1 receptor) in tongue squamous cell carcinoma cells". The Biochemical Journal. 432 (1): 199–205. doi:10.1042/BJ20100859. PMC 3130335. PMID 20819078.
Dopunska literatura[uredi | uredi izvor]
- Benito M, Valverde AM, Lorenzo M (maj 1996). "IGF-I: a mitogen also involved in differentiation processes in mammalian cells". The International Journal of Biochemistry & Cell Biology. 28 (5): 499–510. doi:10.1016/1357-2725(95)00168-9. PMID 8697095.
- Butler AA, Yakar S, Gewolb IH, Karas M, Okubo Y, LeRoith D (septembar 1998). "Insulin-like growth factor-I receptor signal transduction: at the interface between physiology and cell biology". Comparative Biochemistry and Physiology. Part B, Biochemistry & Molecular Biology. 121 (1): 19–26. doi:10.1016/S0305-0491(98)10106-2. PMID 9972281.
- Zhang X, Yee D (2001). "Tyrosine kinase signalling in breast cancer: insulin-like growth factors and their receptors in breast cancer". Breast Cancer Research. 2 (3): 170–5. doi:10.1186/bcr50. PMC 138771. PMID 11250706.
- Gross JM, Yee D (decembar 2003). "The type-1 insulin-like growth factor receptor tyrosine kinase and breast cancer: biology and therapeutic relevance". Cancer and Metastasis Reviews. 22 (4): 327–36. doi:10.1023/A:1023720928680. PMID 12884909. S2CID 35963688.
- Adams TE, McKern NM, Ward CW (juni 2004). "Signalling by the type 1 insulin-like growth factor receptor: interplay with the epidermal growth factor receptor". Growth Factors. 22 (2): 89–95. doi:10.1080/08977190410001700998. PMID 15253384. S2CID 86844427.
- Surmacz E, Bartucci M (septembar 2004). "Role of estrogen receptor alpha in modulating IGF-I receptor signaling and function in breast cancer". Journal of Experimental & Clinical Cancer Research. 23 (3): 385–94. PMID 15595626.
- Wood AW, Duan C, Bern HA (2005). Insulin-like growth factor signaling in fish. International Review of Cytology. 243. str. 215–85. doi:10.1016/S0074-7696(05)43004-1. ISBN 9780123646477. PMID 15797461.
- Sarfstein R, Maor S, Reizner N, Abramovitch S, Werner H (juni 2006). "Transcriptional regulation of the insulin-like growth factor-I receptor gene in breast cancer". Molecular and Cellular Endocrinology. 252 (1–2): 241–6. doi:10.1016/j.mce.2006.03.018. PMID 16647191. S2CID 24895685.
Vanjski linkovi[uredi | uredi izvor]
- IGF-1 Receptor na US National Library of Medicine Medical Subject Headings (MeSH)
- P08069