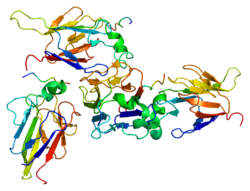
CHEK2
CHEK2 (kinaza 2 kontrolne tačke) jest gen supresije tumora sa hromosoma 22, koji kod ljudi kodira protein CHK2. Protein je serin-treonin kinaza. CHK2 je uključen u popravak DNK, zaustavljan je ćelijskog ciklusa ili apoptozu, kao odgovor na oštećenje DNK. Mutacije gena CHEK2 povezane su sa širokim spektrom karcinoma.[5]
Lokacija gena
[uredi | uredi izvor]CHEK2 gen se nalazi na dugom (q) kraku hromosoma 22 na poziciji 12.1. Njegova lokacija na hromosomu 22 proteže se od baznog para 28,687.742 do baznog para 28,741.904.[5]
Aminokiselinska sekvenca
[uredi | uredi izvor]Dužina polipeptidnog lanca je 543 aminokiseline, a molekulska težina 60.915 Da.[6]
| 10 | 20 | 30 | 40 | 50 | ||||
|---|---|---|---|---|---|---|---|---|
| MSRESDVEAQ | QSHGSSACSQ | PHGSVTQSQG | SSSQSQGISS | SSTSTMPNSS | ||||
| QSSHSSSGTL | SSLETVSTQE | LYSIPEDQEP | EDQEPEEPTP | APWARLWALQ | ||||
| DGFANLECVN | DNYWFGRDKS | CEYCFDEPLL | KRTDKYRTYS | KKHFRIFREV | ||||
| GPKNSYIAYI | EDHSGNGTFV | NTELVGKGKR | RPLNNNSEIA | LSLSRNKVFV | ||||
| FFDLTVDDQS | VYPKALRDEY | IMSKTLGSGA | CGEVKLAFER | KTCKKVAIKI | ||||
| ISKRKFAIGS | AREADPALNV | ETEIEILKKL | NHPCIIKIKN | FFDAEDYYIV | ||||
| LELMEGGELF | DKVVGNKRLK | EATCKLYFYQ | MLLAVQYLHE | NGIIHRDLKP | ||||
| ENVLLSSQEE | DCLIKITDFG | HSKILGETSL | MRTLCGTPTY | LAPEVLVSVG | ||||
| TAGYNRAVDC | WSLGVILFIC | LSGYPPFSEH | RTQVSLKDQI | TSGKYNFIPE | ||||
| VWAEVSEKAL | DLVKKLLVVD | PKARFTTEEA | LRHPWLQDED | MKRKFQDLLS | ||||
| EENESTALPQ | VLAQPSTSRK | RPREGEAEGA | ETTKRPAVCA | AVL |
Struktura proteina
[uredi | uredi izvor]CHEK2 protein kodiran genom CHEK2 je serin treonin kinaza. Protein se sastoji od 543 aminokiseline i sljedećih domena:
- N-terminalni SQ/TQ domen klastera (SCD)
- Centralni replikacijskoj viljušci-pridruženi domen (FHA)
- C-terminalni domen serin/treonin kinaze (KD)
SCD domen sadrži višestruke SQ/TQ motive koji služe kao mjesta fosforilacija, kao odgovor na DNK oštećenje. Najznačajnije i najčešće fosforilirano mjesto je Thr68.[7]
CHK2 se pojavljuje kao monomer u svom neaktivnom stanju. Međutim, u slučaju oštećenja DNK, SCD fosforilacija uzrokuje CHK2 dimerizaciju. Fosforilirani Thr68 (lociran na SCD) stupa u interakciju sa FHA domenom da bi formirao proteinski dimer. Nakon što protein dimerizira, KD se aktivira autofosforilacijom. Jednom kada se KD aktivira, dimer CHK2 se disocira.[7]
Funkcija i mehanizam
[uredi | uredi izvor]Gen CHEK2 kodira kinazu kontrolne tačke 2 (CHK2), protein koji djeluje kao tumorski supresor. CHK2 regulira ćelijsku diobu i ima sposobnost da spriječi prebrzu ili nekontrolisanu podjelu ćelija.[5]
Kada DNK prođe dvolančani prekid, CHK2 se aktivira. Konkretno, protein porodica fosfatidilinozitol-kinaza aktiviran oštećenjem DNK (PIKK) ATM fosforilira mjesto Thr68 i aktivira CHK2.[7] Jednom aktiviran, CHK2 fosforilira nizvodne ciljeve, uključujući CDC25 fosfataze, odgovorne za defosforilaciju i aktiviranje ciklin ovisne kinaze (CDK-a). Dakle, CHK2 inhibicija CDC25 fosfataze sprečava ulazak ćelije u mitozu. Nadalje, CHK2 protein je u interakciji sa nekoliko drugih proteina, uključujući p53. Stabilizacija p53 pomoću CHK2 dovodi do zaustavljanja ćelijskog ciklusa u fazi G1. Nadalje, poznato je da CHK2 fosforilizira transkripcijski faktor ćelijskog ciklusa E2F1 i leukemijski promijelocitni protein (PML) uključen u apoptoze (programiranu ćelijsku smrt).
Povezanost sa rakom
[uredi | uredi izvor]CHK2 protein ima ključnu ulogu u kontrolnoj tački oštećenja DNK. Stoga su mutacije gena CHEK2 označene kao uzroci širokog spektra karcinoma.
Godine 1999. otkriveno je da genetičke varijacije CHEK2 odgovaraju nasljednoj sklonosti ka raku.[8]
Bell et al. (1999) otkrili su tri mutacije zametne linije CHEK2 među četiri slučaja Li–Fraumenijevog sindroma (LFS) i 18 porodica sličnih tom sindromu (LFL). Od vremena ovog otkrića, dvije od tri varijante (delecija u domenu kinaze u egzonu 10 i misens mutacija u FHA domenu u egzona 3) povezane su sa nasljednom osjetljivošću na rak dojke, kao i druge tipove raka.[9]
Osim početnih spekulacija, skrining pacijenata sa LFS i LFL nije otkrio nikakve ili vrlo rijetke individualne misens varijante u CHEK2 genu. Dodatno, delecija u domenu kinaze na egzonu 10 je rijetka među LFS/LFL pacijentima. Dokazi iz ovih studija sugeriraju da CHEK2 nije gen predispozicije za Li-Fraumenijev sindrom.[9]
Rak dojke
[uredi | uredi izvor]Naslijeđene mutacije u genu CHEK2 povezane su s određenim slučajevima karcinoma dojke. Najvažnije, delecija jednog nukleotida u DNK, na poziciji 1.100 u egzonu 10 (1100delC) proizvodi nefunkcionalnu verziju CHK2 proteina, skraćenu na domen kinaze. Gubitak normalne funkcije proteina CHK2 dovodi do neregulirane diobe ćelija, akumuliranog oštećenja DNK i u mnogim slučajevima razvoja tumora.[5] Mutacija CHEK2*1100del je najčešća kod osoba istočnoevropskog i sjevernoevropskog porekla. Unutar ovih populacija mutacija CHEK2*1100delC viđa se kod 1/100 do 1/200 osoba. Međutim, u Sjevernoj Americi učestalost pada na 1/333 do 1/500. Mutacija je gotovo odsutna u Španiji i Indiji.[10] Studije pokazuju da CHEK2 1100delC odgovara dvostruko povećanom riziku od raka dojke i 10 puta povećanom riziku od raka dojke kod muškaraca.[11]
Mutacija CHEK2 poznata kao I157T varijanta domena FHA u egzonu 3 također je povezana s rakom dojke, ali s manjim rizikom od mutacije CHEK2*1100delC. U SAD-u, procijenjeni udio raka dojke koji se pripisuje ovoj varijanti je oko 1,2%.[9]
Još dvije genske mutacije CHEK2, CHEK2*S428F, aminokiselinska supstitucija u domenu kinaze u egzonu 11 i CHEK2*P85L, supstitucija aminokiselina u N-terminalnoj regiji (egzon 1) pronađene su u populaciji Aškenazi Jevreja.[10] Takođe je opisana sugestija o mutaciji osnivača Hispanskog porekla.[12]
Ostali karcinomi
[uredi | uredi izvor]Mutacije na CHEK2 pronađene su u nasljednim i nenasljednim slučajevima raka. Studije povezuju mutaciju sa slučajevima raka prostate, pluća, debelog crijeva, bubrega i tiroidne žlijezde. Povezane su i sa određenim tumorima mozga i osteosarkomom.[5]
Za razliku od mutacija BRCA1 i BRCA2, čini se da mutacije CHEK2 ne uzrokuju povišeni rizik za karcinom jajnika.[11] Međutim, veliki učinak u asocijacijama u cijelom genomu za pločasti karcinom pluća opisana je za rijetku varijantu u CHEK2 (p. Ile157Thr, rs17879961, OR = 0,38).[13]
Mejoza
[uredi | uredi izvor]CHEK2 regulira napredovanje ćelijskog ciklusa i sklapanje vretena tokom sazrevanja mišjih oocita i ranog razvoja embriona.[14][15] Iako je CHEK2 nizvodni efektor ATM-kinaze koja reaguje prvenstveno na dvolančane prekide, može se aktivirati i ATR (ataxia-telangiectasia i Rad3 srodna) kinaza koja reaguje prvenstveno na jednolančane prekide. Kod miševa, CHEK2 je neophodan za nadzor oštećenja DNK u mejozi od ženki. Odgovor oocita na oštećenje dvostrukog lanca DNK uključuje hijerarhiju puteva u kojoj ATR-kinaza signalizira CHEK2, koji zatim aktivira proteine p53 i p63.[16]
Kod voćnih mušica roda Drosophila, zračenje ćelija germ-linije generira dvolančane prekide koji rezultiraju zaustavljanjem ćelijskog ciklusa i apoptozama. Drosophila CHEK2 homolog mnk i p53 ortolog dp53 potrebni su za veći dio ćelijske smrti u ranoj oogenezi kada dođe do selekcije oocita i mejotske rekombinacije.[17]
Interakcije
[uredi | uredi izvor]Pokazalo se da je CHEK2 u interakciji sa:
Reference
[uredi | uredi izvor]- ^ a b c GRCh38: Ensembl release 89: ENSG00000183765 - Ensembl, maj 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000029521 - Ensembl, maj 2017
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ a b c d e "CHEK2". Genetics Home Reference. august 2007.
- ^ "UniProt, O96017" (jezik: engleski). Pristupljeno 04-02-2022. Provjerite vrijednost datuma u parametru:
|access-date=(pomoć) - ^ a b c Cai Z, Chehab NH, Pavletich NP (septembar 2009). "Structure and activation mechanism of the CHK2 DNA damage checkpoint kinase". Molecular Cell. 35 (6): 818–29. doi:10.1016/j.molcel.2009.09.007. PMID 19782031.
- ^ Bell DW, Varley JM, Szydlo TE, Kang DH, Wahrer DC, Shannon KE, et al. (decembar 1999). "Heterozygous germ line hCHK2 mutations in Li-Fraumeni syndrome". Science. 286 (5449): 2528–31. doi:10.1126/science.286.5449.2528. PMID 10617473.
- ^ a b c Nevanlinna H, Bartek J (septembar 2006). "The CHEK2 gene and inherited breast cancer susceptibility". Oncogene. 25 (43): 5912–9. doi:10.1038/sj.onc.1209877. PMID 16998506.
- ^ a b Offit K, Garber JE (februar 2008). "Time to check CHEK2 in families with breast cancer?". Journal of Clinical Oncology. 26 (4): 519–20. doi:10.1200/JCO.2007.13.8503. PMID 18172189.
- ^ a b Meijers-Heijboer H, van den Ouweland A, Klijn J, Wasielewski M, de Snoo A, Oldenburg R, et al. (maj 2002). "Low-penetrance susceptibility to breast cancer due to CHEK2(*)1100delC in noncarriers of BRCA1 or BRCA2 mutations". Nature Genetics. 31 (1): 55–9. doi:10.1038/ng879. PMID 11967536. S2CID 195216803.
- ^ Weitzel JN, Neuhausen SL, Adamson A, Tao S, Ricker C, Maoz A, et al. (august 2019). "Pathogenic and likely pathogenic variants in PALB2, CHEK2, and other known breast cancer susceptibility genes among 1054 BRCA-negative Hispanics with breast cancer". Cancer. 125 (16): 2829–2836. doi:10.1002/cncr.32083. PMC 7376605. PMID 31206626.
- ^ Wang Y, McKay JD, Rafnar T, Wang Z, Timofeeva MN, Broderick P, et al. (juli 2014). "Rare variants of large effect in BRCA2 and CHEK2 affect risk of lung cancer". Nature Genetics. 46 (7): 736–41. doi:10.1038/ng.3002. PMC 4074058. PMID 24880342.
- ^ Dai XX, Duan X, Liu HL, Cui XS, Kim NH, Sun SC (februar 2014). "Chk2 regulates cell cycle progression during mouse oocyte maturation and early embryo development". Molecules and Cells. 37 (2): 126–32. doi:10.14348/molcells.2014.2259. PMC 3935625. PMID 24598997.
- ^ Ruth KS, Day FR, Hussain J, Martínez-Marchal A, Aiken CE, Azad A, et al. (august 2021). "Genetic insights into biological mechanisms governing human ovarian ageing". Nature. 596 (7872): 393–397. Bibcode:2021Natur.596..393R. doi:10.1038/s41586-021-03779-7. ISSN 0028-0836. PMC 7611832. PMID 34349265 Provjerite vrijednost parametra
|pmid=(pomoć). - ^ Bolcun-Filas E, Rinaldi VD, White ME, Schimenti JC (januar 2014). "Reversal of female infertility by Chk2 ablation reveals the oocyte DNA damage checkpoint pathway". Science. 343 (6170): 533–6. Bibcode:2014Sci...343..533B. doi:10.1126/science.1247671. PMC 4048839. PMID 24482479.
- ^ Shim HJ, Lee EM, Nguyen LD, Shim J, Song YH (2014). "High-dose irradiation induces cell cycle arrest, apoptosis, and developmental defects during Drosophila oogenesis". PLOS ONE. 9 (2): e89009. Bibcode:2014PLoSO...989009S. doi:10.1371/journal.pone.0089009. PMC 3923870. PMID 24551207.
- ^ Lee JS, Collins KM, Brown AL, Lee CH, Chung JH (mart 2000). "hCds1-mediated phosphorylation of BRCA1 regulates the DNA damage response". Nature. 404 (6774): 201–4. Bibcode:2000Natur.404..201L. doi:10.1038/35004614. PMID 10724175. S2CID 4345911.
- ^ Chabalier-Taste C, Racca C, Dozier C, Larminat F (decembar 2008). "BRCA1 is regulated by Chk2 in response to spindle damage". Biochimica et Biophysica Acta (BBA) - Molecular Cell Research. 1783 (12): 2223–33. doi:10.1016/j.bbamcr.2008.08.006. PMID 18804494.
- ^ Matsuoka S, Ballif BA, Smogorzewska A, McDonald ER, Hurov KE, Luo J, et al. (maj 2007). "ATM and ATR substrate analysis reveals extensive protein networks responsive to DNA damage". Science. 316 (5828): 1160–6. Bibcode:2007Sci...316.1160M. doi:10.1126/science.1140321. PMID 17525332. S2CID 16648052.
- ^ Lou Z, Minter-Dykhouse K, Wu X, Chen J (februar 2003). "MDC1 is coupled to activated CHK2 in mammalian DNA damage response pathways". Nature. 421 (6926): 957–61. Bibcode:2003Natur.421..957L. doi:10.1038/nature01447. PMID 12607004. S2CID 4411622.
- ^ Adamson AW, Beardsley DI, Kim WJ, Gao Y, Baskaran R, Brown KD (mart 2005). "Methylator-induced, mismatch repair-dependent G2 arrest is activated through Chk1 and Chk2". Molecular Biology of the Cell. 16 (3): 1513–26. doi:10.1091/mbc.E04-02-0089. PMC 551512. PMID 15647386.
- ^ Brown KD, Rathi A, Kamath R, Beardsley DI, Zhan Q, Mannino JL, Baskaran R (januar 2003). "The mismatch repair system is required for S-phase checkpoint activation". Nature Genetics. 33 (1): 80–4. doi:10.1038/ng1052. PMID 12447371. S2CID 20616220.
- ^ Chen XB, Melchionna R, Denis CM, Gaillard PH, Blasina A, Van de Weyer I, et al. (novembar 2001). "Human Mus81-associated endonuclease cleaves Holliday junctions in vitro". Molecular Cell. 8 (5): 1117–27. doi:10.1016/s1097-2765(01)00375-6. PMID 11741546.
- ^ Tsvetkov L, Xu X, Li J, Stern DF (mart 2003). "Polo-like kinase 1 and Chk2 interact and co-localize to centrosomes and the midbody". The Journal of Biological Chemistry. 278 (10): 8468–75. doi:10.1074/jbc.M211202200. PMID 12493754.
- ^ Bahassi EM, Conn CW, Myer DL, Hennigan RF, McGowan CH, Sanchez Y, Stambrook PJ (septembar 2002). "Mammalian Polo-like kinase 3 (Plk3) is a multifunctional protein involved in stress response pathways". Oncogene. 21 (43): 6633–40. doi:10.1038/sj.onc.1205850. PMID 12242661.
Dopunska literatura
[uredi | uredi izvor]- Caspari T (april 2000). "How to activate p53". Current Biology. 10 (8): R315-7. doi:10.1016/S0960-9822(00)00439-5. PMID 10801407. S2CID 17342787.
- McGowan CH (juni 2002). "Checking in on Cds1 (Chk2): A checkpoint kinase and tumor suppressor". BioEssays. 24 (6): 502–11. doi:10.1002/bies.10101. PMID 12111733. S2CID 6654874.
- Honrado E, Osorio A, Palacios J, Benitez J (septembar 2006). "Pathology and gene expression of hereditary breast tumors associated with BRCA1, BRCA2 and CHEK2 gene mutations". Oncogene. 25 (43): 5837–45. doi:10.1038/sj.onc.1209875. PMID 16998498. S2CID 20960561.
- Nevanlinna H, Bartek J (septembar 2006). "The CHEK2 gene and inherited breast cancer susceptibility". Oncogene. 25 (43): 5912–9. doi:10.1038/sj.onc.1209877. PMID 16998506.
- Peng CY, Graves PR, Thoma RS, Wu Z, Shaw AS, Piwnica-Worms H (septembar 1997). "Mitotic and G2 checkpoint control: regulation of 14-3-3 protein binding by phosphorylation of Cdc25C on serine-216". Science. 277 (5331): 1501–5. doi:10.1126/science.277.5331.1501. PMID 9278512.
- Lykidis A, Jackson PD, Rock CO, Jackowski S (decembar 1997). "The role of CDP-diacylglycerol synthetase and phosphatidylinositol synthase activity levels in the regulation of cellular phosphatidylinositol content". The Journal of Biological Chemistry. 272 (52): 33402–9. doi:10.1074/jbc.272.52.33402. PMID 9407135.
- Lindsay HD, Griffiths DJ, Edwards RJ, Christensen PU, Murray JM, Osman F, et al. (februar 1998). "S-phase-specific activation of Cds1 kinase defines a subpathway of the checkpoint response in Schizosaccharomyces pombe". Genes & Development. 12 (3): 382–95. doi:10.1101/gad.12.3.382. PMC 316487. PMID 9450932.
- Matsuoka S, Huang M, Elledge SJ (decembar 1998). "Linkage of ATM to cell cycle regulation by the Chk2 protein kinase". Science. 282 (5395): 1893–7. Bibcode:1998Sci...282.1893M. doi:10.1126/science.282.5395.1893. PMID 9836640.
- Martinho RG, Lindsay HD, Flaggs G, DeMaggio AJ, Hoekstra MF, Carr AM, Bentley NJ (decembar 1998). "Analysis of Rad3 and Chk1 protein kinases defines different checkpoint responses". The EMBO Journal. 17 (24): 7239–49. doi:10.1093/emboj/17.24.7239. PMC 1171070. PMID 9857181.
- Blasina A, de Weyer IV, Laus MC, Luyten WH, Parker AE, McGowan CH (januar 1999). "A human homologue of the checkpoint kinase Cds1 directly inhibits Cdc25 phosphatase". Current Biology. 9 (1): 1–10. doi:10.1016/S0960-9822(99)80041-4. PMID 9889122. S2CID 18008732.
- Brown AL, Lee CH, Schwarz JK, Mitiku N, Piwnica-Worms H, Chung JH (mart 1999). "A human Cds1-related kinase that functions downstream of ATM protein in the cellular response to DNA damage". Proceedings of the National Academy of Sciences of the United States of America. 96 (7): 3745–50. Bibcode:1999PNAS...96.3745B. doi:10.1073/pnas.96.7.3745. PMC 22365. PMID 10097108.
- Chaturvedi P, Eng WK, Zhu Y, Mattern MR, Mishra R, Hurle MR, et al. (juli 1999). "Mammalian Chk2 is a downstream effector of the ATM-dependent DNA damage checkpoint pathway". Oncogene. 18 (28): 4047–54. doi:10.1038/sj.onc.1202925. PMID 10435585. S2CID 23907734.
- Ouyang B, Li W, Pan H, Meadows J, Hoffmann I, Dai W (oktobar 1999). "The physical association and phosphorylation of Cdc25C protein phosphatase by Prk". Oncogene. 18 (44): 6029–36. doi:10.1038/sj.onc.1202983. PMID 10557092.
- Dunham I, Shimizu N, Roe BA, Chissoe S, Hunt AR, Collins JE, et al. (decembar 1999). "The DNA sequence of human chromosome 22". Nature. 402 (6761): 489–95. Bibcode:1999Natur.402..489D. doi:10.1038/990031. PMID 10591208.
- Bell DW, Varley JM, Szydlo TE, Kang DH, Wahrer DC, Shannon KE, et al. (decembar 1999). "Heterozygous germ line hCHK2 mutations in Li-Fraumeni syndrome". Science. 286 (5449): 2528–31. doi:10.1126/science.286.5449.2528. PMID 10617473.
- Chehab NH, Malikzay A, Appel M, Halazonetis TD (februar 2000). "Chk2/hCds1 functions as a DNA damage checkpoint in G(1) by stabilizing p53". Genes & Development. 14 (3): 278–88. doi:10.1101/gad.14.3.278. PMC 316357. PMID 10673500.
- Hirao A, Kong YY, Matsuoka S, Wakeham A, Ruland J, Yoshida H, et al. (mart 2000). "DNA damage-induced activation of p53 by the checkpoint kinase Chk2". Science. 287 (5459): 1824–7. Bibcode:2000Sci...287.1824H. doi:10.1126/science.287.5459.1824. PMID 10710310.
- Lee JS, Collins KM, Brown AL, Lee CH, Chung JH (mart 2000). "hCds1-mediated phosphorylation of BRCA1 regulates the DNA damage response". Nature. 404 (6774): 201–4. Bibcode:2000Natur.404..201L. doi:10.1038/35004614. PMID 10724175. S2CID 4345911.
- Zhou BB, Chaturvedi P, Spring K, Scott SP, Johanson RA, Mishra R, et al. (april 2000). "Caffeine abolishes the mammalian G(2)/M DNA damage checkpoint by inhibiting ataxia-telangiectasia-mutated kinase activity". The Journal of Biological Chemistry. 275 (14): 10342–8. doi:10.1074/jbc.275.14.10342. PMID 10744722. S2CID 4240483.
Vanjski linkovi
[uredi | uredi izvor]- Educational resources Arhivirano 13. 4. 2010. na Wayback Machine
- Gene Reviews
- Gene Tests
- CHEK2 protein, human na US National Library of Medicine Medical Subject Headings (MeSH)
- Lokacija ljudskog genoma CDS1 i stranica sa detaljima o genu CDS1 u UCSC Genome Browseru.
- Lokacija ljudskog genoma CHEK2 i stranica sa detaljima o genu CHEK2 u UCSC Genome Browseru.
Ovaj članak uključuje tekst iz Nacionalne medicinske biblioteke Sjedinjenih Država, koji je u javnom vlasništvu.