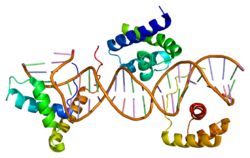
SOX2
SRY-kutija 2 (spolno determinirajuća regija 2 Y) znana i kao SOX2, je transkripcijski faktor neophodan za održavanje samoobnavljanja ili pluripotencije, nediferenciranih embrionskih matičnih ćelija. To je protein koji je kod ljudi kodiran genom SOX2 sa hromosoma 3. Sox2 ima ključnu ulogu u održavanju embrionskih i nerv nih matičnih ćelija.[5]
Sox2 je član Sox porodice transkripcijskih faktora, za koje se pokazalo da imaju ključne uloge u mnogim fazama sisarskog razvoja. Ovaj protein porodica dijeli visoko konzervirane DNK vezujuće domene poznate kao HMG kutija (eng. skr. od High-mobility group = visoko pokretna grupa) domena koje sadrže po približno 80 aminokiselina.[5]
Sox2 uveliko obećava u istraživanju koje uključuje indukovanu pluripotenciju, novo i vrlo obećavajuće polje regenerativne medicine.[6]
Aminokiselinska sekvenca
[uredi | uredi izvor]Dužina polipeptidnog lanca je 317 aminokiselina, а molekulska težina 34.310 Da.[7]
| 10 | 20 | 30 | 40 | 50 | ||||
|---|---|---|---|---|---|---|---|---|
| MYNMMETELK | PPGPQQTSGG | GGGNSTAAAA | GGNQKNSPDR | VKRPMNAFMV | ||||
| WSRGQRRKMA | QENPKMHNSE | ISKRLGAEWK | LLSETEKRPF | IDEAKRLRAL | ||||
| HMKEHPDYKY | RPRRKTKTLM | KKDKYTLPGG | LLAPGGNSMA | SGVGVGAGLG | ||||
| AGVNQRMDSY | AHMNGWSNGS | YSMMQDQLGY | PQHPGLNAHG | AAQMQPMHRY | ||||
| DVSALQYNSM | TSSQTYMNGS | PTYSMSYSQQ | GTPGMALGSM | GSVVKSEASS | ||||
| SPPVVTSSSH | SRAPCQAGDL | RDMISMYLPG | AEVPEPAAPS | RLHMSQHYQS | ||||
| GPVPGTAING | TLPLSHM |
Funkcija
[uredi | uredi izvor]Pluripotencija matičnih ćelija
[uredi | uredi izvor]LIF (leukemija-inhibitorni faktor) signalizacija, koja održava pluripotenciju u mišjim embrionskim matičnim ćelijama, aktivira Sox2 nizvodno od JAK-STAT signalnog puta i naknadnu aktivaciju Klf4 (člana porodica Kruppelovih faktora). Oct-4, Sox2 i Nanog pozitivno regulišu transkripciju svih proteina pluripotentnih kola u LIF putu.[8]
NPM1, regulator transkripcije uključen u proliferaciju ćelija, pojedinačno formira komplekse sa Sox2, Oct4 i Nanog u embrionskim matičnim ćelijama.[9] Ova tri faktora pluripotencije doprinose složenoj molekulnoj mreži koja reguliše niz gena koji kontrolišu pluripotenciju. Sox2 se kooperativno vezuje za DNK sa Oct4 na nepalindromskim sekvencama, kako bi aktivirao transkripciju ključnih faktora pluripotencije.[10] Iznenađujuće, regulacija Oct4-Sox2 pojačivača može se dogoditi bez Sox2, vjerovatno zbog ekspresije drugih Sox proteina. Međutim, grupa istraživača je zaključila da je primarna uloga Sox2 u embrionskim matičnim ćelijama kontrola ekspresije Oct4 i da oboje održavaju vlastitu ekspresiju kada se eksprimiraju istovremeno.[11]
U eksperimentu koji je uključivao embrionske matične ćelije miša, otkriveno je da je Sox2 u sprezi sa Oct4, c-Myc i Klf4 dovoljan za proizvodnju induciranih pluripotentnih matičnih ćelija.[12] Otkriće da je ekspresija samo četiri transkripcijska faktora neophodna da bi se izazvala pluripotencija omogućilo je da se buduća istraživanja regenerativne medicine sprovedu s obzirom na manje manipulacije.
Gubitak pluripotencije reguliše se hipermetilacijom nekih mjesta vezanja Sox2 i Oct4 u muškim zametnim ćelijama[13] i posttranskripcijsku supresiju Sox2 od strane miR134.[14]
Različiti nivoi Sox2 utiču na sudbinu diferencijacije embrionskih matičnih ćelija. Sox2 inhibira diferencijaciju u mezendermni zametni sloj i promovira diferencijaciju u nervni ektodermni zametni sloj.[15] Npm1/Sox2 kompleksi se održavaju kada se diferencijacija inducira duž ektodermne loze, naglašavajući važnu funkcionalnu ulogu Sox2 u diferencijaciji ektoderma.[9]
Studija sprovedena u Milanu, Italija, pokazala je, kroz razvoj nokaut modela, da nedostatak Sox2 dovodi do nervnih malformacija i konačno smrti fetusa, dodatno naglašavajući vitalnu ulogu Sox2 u embrionskom razvoju.[16]
Nervne matične ćelije
[uredi | uredi izvor]U neurogenezi, Sox2 se eksprimira kroz ćelije u razvoju u nervnoj cijevi, kao i u proliferirajućim progenitorima centralnog nervnog sistema. Međutim, Sox2 je reguliran tokom konačnog ćelijskog ciklusa progenitora tokom diferencijacije, kada postanu post mitotski.[17] Ćelije koje eksprimiraju Sox2 sposobne su i za proizvodnju ćelija koje su identične sebi i za diferencirane tipove neuronskih ćelija, dva neophodna obilježja matičnih ćelija. Tako signali koji kontrolišu ekspresiju Sox2 u pretpostavljenom neuronskom odjeljku, kao što je signalizacija Notch, kontroliraju koju veličinu neuronski odjeljak konačno dostiže.[18] Proliferacija Sox2+ nerve matične ćelije može stvoriti neuronske prekursore kao i populaciju nervnih matičnih ćelija Sox2+.[19] Razlike u veličini mozga između vrsta stoga se odnose na kapacitet različitih vrsta da održe ekspresiju SOX2 u nervnim sistemima u razvoju. Razlika u veličini mozga između ljudi i majmuna, naprimjer, povezana je s mutacijama u genu Asb11, koji je uzvodni aktivator SOX2 u nervnom sistemu u razvoju..[20]
Inducirana pluripotencija je moguća korištenjem odraslih nervnih matičnih ćelija, koje eksprimiraju više razine Sox2 i c-Myc od embrionsskih matičnih ćelija. Stoga su samo dva egzogena faktora, od kojih je jedan nužno Oct4, dovoljna za indukciju pluripotentnih iz nervnih matičnih ćelija, smanjujući komplikacije i rizike povezane s uvođenjem više faktora za izazivanje pluripotencije..[21]
Deformacije oka
[uredi | uredi izvor]Mutacije u ovom genu su povezane s bilateralnom anoftalmijom, teškim strukturnim deformitetom oka.[22]
U razvoju pluća, Sox2 kontrolira morfogenezu grananja bronhijskog stabla i diferencijaciju epitela disajnih puteva. Prekomjerna ekspresija uzrokuje povećanje neuroendokrinih, želučanih/crijevnih i baznih ćelija.[23] U normalnim uslovima, Sox2 je kritičan za održavanje samoobnavljanja i odgovarajućeg udjela bazalnih ćelija u trahejskom epitelu odraslih. Međutim, njegova prekomjerna ekspresija dovodi do ekstenzivne epitelne hiperplazije i na kraju do karcinoma u plućima miševa u razvoju i odraslih miševa.[24]
U karcinomu pločastih ćelija, genske amplifikacije često ciljaju na regiju 3q26.3. Gen za Sox2 leži unutar ovog regiona, što efektivno karakteriše Sox2 kao onkogen, iako je kod adenokarcinoma jednjaka gubitak Sox2 snažno povezan sa lošijom prognozom, efektivno karakterišući Sox2 kao supresor tumora. Stoga je pošteno reći da je funkcija SOX2 kod raka plejotropna.[25] Sox2 je ključni faktor povećane regulacije u karcinomu skvamoznih čelija pluća, usmjeravajući mnoge gene uključene u progresiju tumora. Prekomjerna ekspresija Sox2 sarađuje s gubitkom ekspresije Lkb1 za podsticanje skvamoznog karcinoma pluća kod miševa.[26] Njegova prekomjerna ekspresija također aktivira ćelijsku migraciju i rast, nezavisan od sidrišta.[27]
Ekspresija Sox2 se također nalazi u visokom stepenu raka prostate i podstiče rast raka prostate otpornog na kastraciju.[28]
Ektopijska ekspresija SOX2 može biti povezana sa abnormalnom diferencijacijom ćelija kolorekumskog karcinoma.[29]
Pokazalo se da je Sox2 relevantan u razvoju rezistencije na tamoksifen kod raka dojke.[30]
U glioblastoma multiforme, Sox2 je dobro uspostavljen faktor transkripcije matičnih ćelija potreban za indukciju i održavanje svojstava stabljike glioblastomskih ćelija raka.[31][32]
Regulacija hormonom štitnjače
[uredi | uredi izvor]Postoje tri elementa odgovora hormona štitnjače (TRE) u regionu uzvodno od promotora Sox2. Ova regija je poznata kao regija pojačivača. Studije su sugerirale da tiroidni hormon (T3) kontrolira ekspresiju Sox2 preko regije pojačivača. Ekspresija TRα1 (receptora tiroidnog hormona) je povećana u proliferirajućim i migrirajućim nervnim matičnim ćelijama. Stoga se sugerira da transkripcijska represija Sox2, posredovana signalnom osovinom hormona štitnjače, omogućava privrženost neuronskih matičnih ćelija i migraciju iz subkomorske zone. Nedostatak hormona štitnjače, posebno tokom prvog trimestra, dovest će do abnormalnog razvoja centralnog nervnog sistema.[33]
Dodatno u prilog ovom zaključku ide i činjenica da hipotireoza tokom fetusnog razvoja može rezultirati raznim neurološkim nedostacima, uključujući kretenizam, koji karakterizira zaostajanje u fizičkom razvoju i mentalna retardacija.[33]
Hipotireoza može nastati iz mnoštva uzroka i obično se liječi hormonskim tretmanima kao što je često korišteni levotiroksin.[34]
Interakcije
[uredi | uredi izvor]Pokazalo se da SOX2 reaguje sa PAX6,[35] NPM1,[8] i Oct4.[10] Za SOX2 nađeno je da učestvuje u regulaciji Rex1 sa Oct3/4.[36]
Reference
[uredi | uredi izvor]- ^ a b c GRCh38: Ensembl release 89: ENSG00000181449 - Ensembl, maj 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000074637 - Ensembl, maj 2017
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ a b "SOX2". NCBI.
- ^ Rizzino A (2009). "Sox2 and Oct-3/4: a versatile pair of master regulators that orchestrate the self-renewal and pluripotency of embryonic stem cells". Wiley Interdisciplinary Reviews: Systems Biology and Medicine. 1 (2): 228–36. doi:10.1002/wsbm.12. PMC 2794141. PMID 20016762.
- ^ "UniProt, P48431" (jezik: engleski). Pristupljeno 9. 11. 2021.
- ^ a b Niwa H, Ogawa K, Shimosato D, Adachi K (juli 2009). "A parallel circuit of LIF signalling pathways maintains pluripotency of mouse ES cells". Nature. 460 (7251): 118–22. Bibcode:2009Natur.460..118N. doi:10.1038/nature08113. PMID 19571885. S2CID 4382543.
- ^ a b Johansson H, Simonsson S (novembar 2010). "Core transcription factors, Oct4, Sox2 and Nanog, individually form complexes with nucleophosmin (Npm1) to control embryonic stem (ES) cell fate determination". Aging. 2 (11): 815–22. doi:10.18632/aging.100222. PMC 3006024. PMID 21076177.
- ^ a b Chambers I, Tomlinson SR (juli 2009). "The transcriptional foundation of pluripotency". Development. 136 (14): 2311–22. doi:10.1242/dev.024398. PMC 2729344. PMID 19542351.
- ^ Masui S, Nakatake Y, Toyooka Y, Shimosato D, Yagi R, Takahashi K, Okochi H, Okuda A, Matoba R, Sharov AA, Ko MS, Niwa H (juni 2007). "Pluripotency governed by Sox2 via regulation of Oct3/4 expression in mouse embryonic stem cells". Nature Cell Biology. 9 (6): 625–35. doi:10.1038/ncb1589. PMID 17515932. S2CID 24074525.
- ^ Takahashi K, Yamanaka S (august 2006). "Induction of pluripotent stem cells from mouse embryonic and adult fibroblast cultures by defined factors". Cell. 126 (4): 663–76. doi:10.1016/j.cell.2006.07.024. hdl:2433/159777. PMID 16904174. S2CID 1565219.
- ^ Imamura M, Miura K, Iwabuchi K, Ichisaka T, Nakagawa M, Lee J, Kanatsu-Shinohara M, Shinohara T, Yamanaka S (2006). "Transcriptional repression and DNA hypermethylation of a small set of ES cell marker genes in male germline stem cells". BMC Developmental Biology. 6: 34. doi:10.1186/1471-213X-6-34. PMC 1564388. PMID 16859545.
- ^ Tay Y, Zhang J, Thomson AM, Lim B, Rigoutsos I (oktobar 2008). "MicroRNAs to Nanog, Oct4 and Sox2 coding regions modulate embryonic stem cell differentiation". Nature. 455 (7216): 1124–8. Bibcode:2008Natur.455.1124T. doi:10.1038/nature07299. PMID 18806776. S2CID 4330178.
- ^ Thomson M, Liu SJ, Zou LN, Smith Z, Meissner A, Ramanathan S (juni 2011). "Pluripotency factors in embryonic stem cells regulate differentiation into germ layers". Cell. 145 (6): 875–89. doi:10.1016/j.cell.2011.05.017. PMC 5603300. PMID 21663792.
- ^ Ferri AL, Cavallaro M, Braida D, Di Cristofano A, Canta A, Vezzani A, Ottolenghi S, Pandolfi PP, Sala M, DeBiasi S, Nicolis SK (august 2004). "Sox2 deficiency causes neurodegeneration and impaired neurogenesis in the adult mouse brain". Development. 131 (15): 3805–19. doi:10.1242/dev.01204. PMID 15240551.
- ^ Graham V, Khudyakov J, Ellis P, Pevny L (august 2003). "SOX2 functions to maintain neural progenitor identity". Neuron. 39 (5): 749–65. doi:10.1016/S0896-6273(03)00497-5. PMID 12948443. S2CID 17162323.
- ^ Liu P, Verhaar AP, Peppelenbosch MP (januar 2019). "Signaling Size: Ankyrin and SOCS Box-Containing ASB E3 Ligases in Action". Trends in Biochemical Sciences. 44 (1): 64–74. doi:10.1016/j.tibs.2018.10.003. PMID 30446376.
- ^ Suh H, Consiglio A, Ray J, Sawai T, D'Amour KA, Gage FH (novembar 2007). "In vivo fate analysis reveals the multipotent and self-renewal capacities of Sox2+ neural stem cells in the adult hippocampus". Cell Stem Cell. 1 (5): 515–28. doi:10.1016/j.stem.2007.09.002. PMC 2185820. PMID 18371391.
- ^ Diks SH, Bink RJ, van de Water S, Joore J, van Rooijen C, Verbeek FJ, den Hertog J, Peppelenbosch MP, Zivkovic D (14. 8. 2006). "The novel gene asb11: a regulator of the size of the neural progenitor compartment". Journal of Cell Biology. 174 (4): 581–592. doi:10.1083/jcb.200601081. PMC 2064263. PMID 16893969.
- ^ Kim JB, Zaehres H, Wu G, Gentile L, Ko K, Sebastiano V, Araúzo-Bravo MJ, Ruau D, Han DW, Zenke M, Schöler HR (juli 2008). "Pluripotent stem cells induced from adult neural stem cells by reprogramming with two factors". Nature. 454 (7204): 646–50. Bibcode:2008Natur.454..646K. doi:10.1038/nature07061. PMID 18594515. S2CID 4318637.
- ^ "Entrez Gene: SOX2 SRY (sex determining region Y)-box 2".
- ^ Gontan C, de Munck A, Vermeij M, Grosveld F, Tibboel D, Rottier R (maj 2008). "Sox2 is important for two crucial processes in lung development: branching morphogenesis and epithelial cell differentiation". Developmental Biology. 317 (1): 296–309. doi:10.1016/j.ydbio.2008.02.035. PMID 18374910.
- ^ Lu Y, Futtner C, Rock JR, Xu X, Whitworth W, Hogan BL, Onaitis MW (2010). "Evidence that SOX2 overexpression is oncogenic in the lung". PLOS ONE. 5 (6): e11022. Bibcode:2010PLoSO...511022L. doi:10.1371/journal.pone.0011022. PMC 2883553. PMID 20548776.
- ^ van Olphen SH, Biermann K, Shapiro J, Wijnhoven BP, Toxopeus EL, van der Gaast A, Stoop HA, van Lanschot JJ, Spaander MC, Bruno MJ, Looijenga LH (2017). "P53 and SOX2 Protein Expression Predicts Esophageal Adenocarcinoma in Response to Neoadjuvant Chemoradiotherapy". Annals of Surgery. 265 (2): 347–355. doi:10.1097/SLA.0000000000001625. PMID 28059963. S2CID 19544093.
- ^ Mukhopadhyay A, Berrett KC, Kc U, Clair PM, Pop SM, Carr SR, Witt BL, Oliver TG (juli 2014). "Sox2 cooperates with Lkb1 loss in a mouse model of squamous cell lung cancer". Cell Reports. 8 (1): 40–9. doi:10.1016/j.celrep.2014.05.036. PMC 4410849. PMID 24953650.
- ^ Hussenet T, Dali S, Exinger J, Monga B, Jost B, Dembelé D, Martinet N, Thibault C, Huelsken J, Brambilla E, du Manoir S (2010). "SOX2 is an oncogene activated by recurrent 3q26.3 amplifications in human lung squamous cell carcinomas". PLOS ONE. 5 (1): e8960. Bibcode:2010PLoSO...5.8960H. doi:10.1371/journal.pone.0008960. PMC 2813300. PMID 20126410.
- ^ Kregel S, Kiriluk KJ, Rosen AM, Cai Y, Reyes EE, Otto KB, Tom W, Paner GP, Szmulewitz RZ, Vander Griend DJ (2013). "Sox2 is an androgen receptor-repressed gene that promotes castration-resistant prostate cancer". PLOS ONE. 8 (1): e53701. Bibcode:2013PLoSO...853701K. doi:10.1371/journal.pone.0053701. PMC 3543364. PMID 23326489.
- ^ Tani Y, Akiyama Y, Fukamachi H, Yanagihara K, Yuasa Y (april 2007). "Transcription factor SOX2 up-regulates stomach-specific pepsinogen A gene expression". Journal of Cancer Research and Clinical Oncology. 133 (4): 263–9. doi:10.1007/s00432-006-0165-x. PMID 17136346. S2CID 33410257.
- ^ Piva M, Domenici G, Iriondo O, Rábano M, Simões BM, Comaills V, Barredo I, López-Ruiz JA, Zabalza I, Kypta R, Vivanco Md (januar 2014). "Sox2 promotes tamoxifen resistance in breast cancer cells". EMBO Molecular Medicine. 6 (1): 66–79. doi:10.1002/emmm.201303411. PMC 3936493. PMID 24178749.
- ^ Miyazono, Kohei; Miyazawa, Keiji; Takahashi, Masamichi; Ino, Yasushi; Todo, Tomoki; Ikushima, Hiroaki (6. 11. 2009). "Autocrine TGF-β Signaling Maintains Tumorigenicity of Glioma-Initiating Cells through Sry-Related HMG-Box Factors". Cell Stem Cell (jezik: engleski). 5 (5): 504–514. doi:10.1016/j.stem.2009.08.018. ISSN 1934-5909. PMID 19896441.
- ^ Gangemi, Rosaria Maria Rita; Griffero, Fabrizio; Marubbi, Daniela; Perera, Marzia; Capra, Maria Cristina; Malatesta, Paolo; Ravetti, Gian Luigi; Zona, Gian Luigi; Daga, Antonio (25. 10. 2008). "SOX2 silencing in glioblastoma tumor-initiating cells causes stop of proliferation and loss of tumorigenicity". Stem Cells. 27 (1): 40–48. doi:10.1634/stemcells.2008-0493. ISSN 1549-4918. PMID 18948646. S2CID 19125999.
- ^ a b López-Juárez A, Remaud S, Hassani Z, Jolivet P, Pierre Simons J, Sontag T, Yoshikawa K, Price J, Morvan-Dubois G, Demeneix BA (maj 2012). "Thyroid hormone signaling acts as a neurogenic switch by repressing Sox2 in the adult neural stem cell niche". Cell Stem Cell. 10 (5): 531–43. doi:10.1016/j.stem.2012.04.008. PMID 22560077.
- ^ Wisse B. Hypothyroidism: MedlinePlus Medical Encyclopedia. U.S National Library of Medicine. Pristupljeno 10. 4. 2014.
- ^ Aota S, Nakajima N, Sakamoto R, Watanabe S, Ibaraki N, Okazaki K (maj 2003). "Pax6 autoregulation mediated by direct interaction of Pax6 protein with the head surface ectoderm-specific enhancer of the mouse Pax6 gene". Developmental Biology. 257 (1): 1–13. doi:10.1016/S0012-1606(03)00058-7. PMID 12710953.
- ^ Shi W, Wang H, Pan G, Geng Y, Guo Y, Pei D (august 2006). "Regulation of the pluripotency marker Rex-1 by Nanog and Sox2". Journal of Biological Chemistry. 281 (33): 23319–25. doi:10.1074/jbc.M601811200. PMID 16714766.
Dopunska literatura
[uredi | uredi izvor]- Kamachi Y, Uchikawa M, Kondoh H (april 2000). "Pairing SOX off: with partners in the regulation of embryonic development". Trends in Genetics. 16 (4): 182–7. doi:10.1016/S0168-9525(99)01955-1. PMID 10729834.
- Schepers GE, Teasdale RD, Koopman P (august 2002). "Twenty pairs of sox: extent, homology, and nomenclature of the mouse and human sox transcription factor gene families". Developmental Cell. 3 (2): 167–70. doi:10.1016/S1534-5807(02)00223-X. PMID 12194848.
- Hever AM, Williamson KA, van Heyningen V (juni 2006). "Developmental malformations of the eye: the role of PAX6, SOX2 and OTX2". Clinical Genetics. 69 (6): 459–70. doi:10.1111/j.1399-0004.2006.00619.x. PMID 16712695. S2CID 5676139.
- Yuan H, Corbi N, Basilico C, Dailey L (novembar 1995). "Developmental-specific activity of the FGF-4 enhancer requires the synergistic action of Sox2 and Oct-3". Genes & Development. 9 (21): 2635–45. doi:10.1101/gad.9.21.2635. PMID 7590241.
- Stevanovic M, Zuffardi O, Collignon J, Lovell-Badge R, Goodfellow P (oktobar 1994). "The cDNA sequence and chromosomal location of the human SOX2 gene". Mammalian Genome. 5 (10): 640–2. doi:10.1007/BF00411460. PMID 7849401. S2CID 10841620.
- Bonaldo MF, Lennon G, Soares MB (septembar 1996). "Normalization and subtraction: two approaches to facilitate gene discovery". Genome Research. 6 (9): 791–806. doi:10.1101/gr.6.9.791. PMID 8889548.
- Helland R, Berglund GI, Otlewski J, Apostoluk W, Andersen OA, Willassen NP, Smalås AO (januar 1999). "High-resolution structures of three new trypsin-squash-inhibitor complexes: a detailed comparison with other trypsins and their complexes". Acta Crystallographica Section D. 55 (Pt 1): 139–48. doi:10.1107/S090744499801052X. PMID 10089404.
- Güre AO, Stockert E, Scanlan MJ, Keresztes RS, Jäger D, Altorki NK, Old LJ, Chen YT (april 2000). "Serological identification of embryonic neural proteins as highly immunogenic tumor antigens in small cell lung cancer". Proceedings of the National Academy of Sciences of the United States of America. 97 (8): 4198–203. Bibcode:2000PNAS...97.4198G. doi:10.1073/pnas.97.8.4198. PMC 18195. PMID 10760287.
- Ambrosetti DC, Schöler HR, Dailey L, Basilico C (juli 2000). "Modulation of the activity of multiple transcriptional activation domains by the DNA binding domains mediates the synergistic action of Sox2 and Oct-3 on the fibroblast growth factor-4 enhancer". The Journal of Biological Chemistry. 275 (30): 23387–97. doi:10.1074/jbc.M000932200. PMID 10801796.
- Kamachi Y, Uchikawa M, Tanouchi A, Sekido R, Kondoh H (maj 2001). "Pax6 and SOX2 form a co-DNA-binding partner complex that regulates initiation of lens development". Genes & Development. 15 (10): 1272–86. doi:10.1101/gad.887101. PMC 313803. PMID 11358870.
- Fantes J, Ragge NK, Lynch SA, McGill NI, Collin JR, Howard-Peebles PN, Hayward C, Vivian AJ, Williamson K, van Heyningen V, FitzPatrick DR (april 2003). "Mutations in SOX2 cause anophthalmia". Nature Genetics. 33 (4): 461–3. doi:10.1038/ng1120. PMID 12612584.
- Wiebe MS, Nowling TK, Rizzino A (maj 2003). "Identification of novel domains within Sox-2 and Sox-11 involved in autoinhibition of DNA binding and partnership specificity". Journal of Biological Chemistry. 278 (20): 17901–11. doi:10.1074/jbc.M212211200. PMID 12637543.
- Aota S, Nakajima N, Sakamoto R, Watanabe S, Ibaraki N, Okazaki K (maj 2003). "Pax6 autoregulation mediated by direct interaction of Pax6 protein with the head surface ectoderm-specific enhancer of the mouse Pax6 gene". Developmental Biology. 257 (1): 1–13. doi:10.1016/S0012-1606(03)00058-7. PMID 12710953.
- Schepers G, Wilson M, Wilhelm D, Koopman P (juli 2003). "SOX8 is expressed during testis differentiation in mice and synergizes with SF1 to activate the Amh promoter in vitro". Journal of Biological Chemistry. 278 (30): 28101–8. doi:10.1074/jbc.M304067200. PMID 12732652.
- Reményi A, Lins K, Nissen LJ, Reinbold R, Schöler HR, Wilmanns M (august 2003). "Crystal structure of a POU/HMG/DNA ternary complex suggests differential assembly of Oct4 and Sox2 on two enhancers". Genes & Development. 17 (16): 2048–59. doi:10.1101/gad.269303. PMC 196258. PMID 12923055.
- Williams DC, Cai M, Clore GM (januar 2004). "Molecular basis for synergistic transcriptional activation by Oct1 and Sox2 revealed from the solution structure of the 42-kDa Oct1.Sox2.Hoxb1-DNA ternary transcription factor complex". Journal of Biological Chemistry. 279 (2): 1449–57. doi:10.1074/jbc.M309790200. PMID 14559893.
- Tsukamoto T, Inada K, Tanaka H, Mizoshita T, Mihara M, Ushijima T, Yamamura Y, Nakamura S, Tatematsu M (mart 2004). "Down-regulation of a gastric transcription factor, Sox2, and ectopic expression of intestinal homeobox genes, Cdx1 and Cdx2: inverse correlation during progression from gastric/intestinal-mixed to complete intestinal metaplasia". Journal of Cancer Research and Clinical Oncology. 130 (3): 135–45. doi:10.1007/s00432-003-0519-6. PMID 14655050. S2CID 19831132.
Vanjski linkovi
[uredi | uredi izvor]- Young Lab- Core Transcriptional Regulatory Circuitry in Human Embryonic Stem Cells
- GeneReviews/NCBI/NIH/UW entry on SOX2-related eye disorders
- Generating iPS Cells from MEFS through Forced Expression of Sox-2, Oct-4, c-Myc, and Klf4 (Journal of Visualized Experiments) Arhivirano 9. 4. 2008. na Wayback Machine
- GeneReviews/NCBI/NIH/UW entry on Anophthalmia / Microphthalmia Overview
- P48431
- P48432