SMAD4
SMAD4 ili član 4 porodice SMAD, reaktori majke protiv dekapentaplegijskog homologa 4 ili DPC4 (deletirani-4 u raku gušterače) je visoko konzervirani protein, u svim metazoama. Pripada porodici SMAD proteinskih faktora transkripcije, koji deluju kao posrednici u transmisiji TGF-β signala. Porodica citokina TGFβ regulira kritične procese tokom životnog ciklusa metazoa, sa važnim ulogama tokom razvoja embrion a, homeostaza tkiva, regeneracije i imunske regulacije .[5]
Dužina polipeptidnog lanca je 552 aminokiseline, sa molekulskom težinom od 60.439.[6].
SMAD 4 pripada grupi ko-SMAD (koposrednik SMAD), drugoj klasi SMAD porodice. SMAD4 je jedini poznati ko-SMAD u većini metazoa. Također pripada i proteina porodice Darwin, koji moduliraju članove superporodice porodica TGFβ, porodice proteina od kojih svi imaju ulogu u regulaciji ćelijskih odgovora. SMAD4 sisara je homolog proteina rakcije majke protiv dekapentaplegika kod Drosophila, zvanih Medeja.[7]
SMAD4 stupa u interakciju s R-Smad-ima, kao što su SMAD2, SMAD3, SMAD1, SMAD5 i SMAD8 (također zvani SMAD9), da bi formirao heterotrimerne komplekse. U jedru, kompleks SMAD4 i dva R-SMADS vežu se za DNK i reguliraju ekspresiju različitih gena, ovisno o ćelijskom kontekstu.[7] Unutarćelijske reakcije koje uključuju SMAD4, na površini ćelija pokreću vezanje faktora rasta iz porodice TGFβ. Sekvenca unutarćelijskih reakcija koja uključuje SMAD naziva se SMAD-ni put ili put transformirajućeg faktora rasta beta (TGF-β), jer sekvenca započinje ćelijskim prepoznavanjem TGF-β.
Gen
[uredi | uredi izvor]Kod sisara SMAD4 kodiran je genom koji se nalazi na hromosomu 18. Kod ljudi, gen SMAD4 sadrži 54-829 baznih parova i nalazi se od para br. 51,030.212 do para 51,085.041, u regiji q21,1 hromosoma 18.[8][9]

Protein
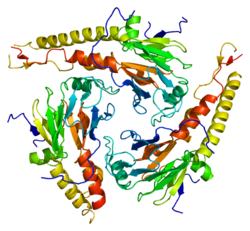
[uredi | uredi izvor]SMAD4 je 552-aminokiselinski polipeptid molekulske težine 60.439 Da. SMAD4 ima dva funkcionalna domena poznat kao MH1 i MH2.

Kompleks dva SMAD3 (ili dva SMAD2) i jedan SMAD4, direktno se veže za DNK interakcijom njihovih MH1 domena. Ovi kompleksi se upućuju na odgovarajuća mjesta u genomu pomoću transkripcijskih faktora, koji definiraju ćelijskuu lozu (LDTF) određujući kontekst-zavisnu prirodu djelovanja TGF-β. Rani uvidi u specifičnost vezanja DNK za Smad-proteine proizašli su iz pregleda za vezanje oligonukleotida, koji su identificirali palindromski dupleks 5'-GTCTAGAC-3', kao vezujuću sekvencu visokog afiniteta za SMAD3 i SMAD4 MH1 domene.[10] Ostali motivi su također identificirani u promotorima i pojačivačima. Ova dodatna mjesta sadrže motiv CAGCC i konsenzusne sekvence GGC (GC) | (CG), potonje poznate i kao 5GC mjesta.[11] Motivi 5GC su visoko predstavljeni kao klasteri lokacija, u SMAD-vezanim regijama širom genoma. Ovi klasteri mogu sadržavati i CAG (AC) | (CC) mjesta. Kompleks SMAD3 / SMAD4 također se veže za elemente promotorskih gena koji reagiraju na TPA i imaju motivske sekvence TGAGTCAG.[12]
Strukture
[uredi | uredi izvor]Aminokiselinska sekvenca
[uredi | uredi izvor]| 10 | 20 | 30 | 40 | 50 | ||||
|---|---|---|---|---|---|---|---|---|
| MDNMSITNTP | TSNDACLSIV | HSLMCHRQGG | ESETFAKRAI | ESLVKKLKEK | ||||
| KDELDSLITA | ITTNGAHPSK | CVTIQRTLDG | RLQVAGRKGF | PHVIYARLWR | ||||
| WPDLHKNELK | HVKYCQYAFD | LKCDSVCVNP | YHYERVVSPG | IDLSGLTLQS | ||||
| NAPSSMMVKD | EYVHDFEGQP | SLSTEGHSIQ | TIQHPPSNRA | STETYSTPAL | ||||
| LAPSESNATS | TANFPNIPVA | STSQPASILG | GSHSEGLLQI | ASGPQPGQQQ | ||||
| NGFTGQPATY | HHNSTTTWTG | SRTAPYTPNL | PHHQNGHLQH | HPPMPPHPGH | ||||
| YWPVHNELAF | QPPISNHPAP | EYWCSIAYFE | MDVQVGETFK | VPSSCPIVTV | ||||
| DGYVDPSGGD | RFCLGQLSNV | HRTEAIERAR | LHIGKGVQLE | CKGEGDVWVR | ||||
| CLSDHAVFVQ | SYYLDREAGR | APGDAVHKIY | PSAYIKVFDL | RQCHRQMQQQ | ||||
| AATAQAAAAA | QAAAVAGNIP | GPGSVGGIAP | AISLSAAAGI | GVDDLRRLCI | ||||
| LRMSFVKGWG | PDYPRQSIKE | TPCWIEIHLH | RALQLLDEVL | HTMPIADPQP | ||||
| LD |
- Simboli
C: Cistein
D: Asparaginska kiselina
E: Glutaminska kiselina
F: Fenilalanin
G: Glicin
H: Histidin
I: Izoleucin
K: Lizin
L: Leucin
M: Metionin
N: Asparagin
P: Prolin
Q: Glutamin
R: Arginin
S: Serin
T: Treonin
V: Valin
W: Triptofan
Y: Tirozin
Kompleksi domena MH1 sa motivima DNK
[uredi | uredi izvor]Prva struktura SMAD4 vezana za DNK bio je kompleks s palindromskim motivom GTCTAGAC..[13] Nedavno su određene i strukture SMAD4 MH1 domena, vezane za nekoliko 5GC motiva. U svim kompleksima, interakcija s DNK uključuje kunzerviranu β-ukosnicu MH1 domena. Ukosnica je djelimično fleksibilna u rastvoru, pa sa visokim stupanjem konformacijske fleksibilnosti omogućava prepoznavanje različitih sekvenci od 5 bp. Do efikasne interakcije sa GC-mjestima dolazi samo ako se G-nukleotid nalazi duboko u glavnom skupu i uspostavlja vodikove veze sa guaninskom grupom Arg81. Ova interakcija olakšava komplementarni površinski kontakt između ukosnice koja veže Smad DNK i glavne račve DNK. Druge direktne interakcije uključuju Lys88 i Gln83. Kristalna struktura rendgenskih zraka SMAD4 MH1 domena kod Trichoplax adhaerens , vezanih za motiv GGCGC, ukazuje na visoku konzerviranost ove interakcije u metazoama.[11]



Kompleksi domena MH2
[uredi | uredi izvor]Domen MH2, koji odgovara C-kraju, odgovorna je za prepoznavanje receptora i povezivanje s drugim SMAD-ovima. Interakcija je sa R-SMADS MH2 domenom i formira heterodimere i heterotrimere. Neke tumorske mutacije otkrivene u SMAD4 pojačavaju interakcije između MH1 i MH2 domena.[14]
Nomenklatura i porijeklo imena
[uredi | uredi izvor]SMAD-ovi su visoko konzervirani po vrstama, posebno na N-terminalu MH1-domena i C-terminalu MH2-domena. SMAD-ovi proteini su homolozi i proteina MADkod Drosophila i protein SMA Caenorhabditis elegans. Ime je kombinacija oboje. Tokom istraživanja Drosophila utvrđeno je da mutacija gena MAD kod reakcije majke potiskuje gen dekapentaplegije u embrionu. Dodana je fraza "majke protiv", jer majke često formiraju strukture koje se protive raznim pitanjima, npr. majke protiv vožnje u pijanom stanju (MADD), što odražava "poboljšanje majčinog učinka dpp" [15] i zasnovano na tradiciji neobičnog imenovanja unutar istraživačke zajednice.[16] SMAD4 je poznat i kao DPC4, JIP ili MADH4.
Funkcija i mehanizam djelovanja
[uredi | uredi izvor]SMAD4 je protein definiran kao bitni efektor u SMAD putu. SMAD4 služi kao posrednik između ivanćelijskih faktora rasta iz porodice TGFβ i gena unutar ćelijsog jedra. Skraćenica ko u ko-SMAD znači zajednički posrednik (koposrednik) . SMAD4 je također definiran kao pretvarač signala.
U TGF-β putu, TGF-β dimere prepoznaje transmembranski receptor, poznat kao receptor tipa II. Kada se receptor tipa II aktivira vezanjem TGF-β, fosforilira receptor tipa I. Receptor tipa I je također receptor na površini ćelije. Ovaj receptor zatim fosforilira SMAD-ove (R-SMAD), reguliran unutarćelijskim receptorima kao što su SMAD2 ili SMAD3. Fosforilirani R-SMAD-ovi se zatim vežu za SMAD4. Asocijacija R-SMAD-SMAD4 je heteromerni kompleks. Ovaj će se kompleks premjestiti iz citoplazme u jedro: to je translokacija. Sa R-SMAD-ovima, SMAD4 može stvarati heterotrimerne, heteroheksamerne ili heterodimerne komplekse.
SMAD4 je supstrat Erk/MAPK-kinaze.[17] and GSK3.[18] Stimulacija puta FGF (faktor rasta fibroblasta) dovodi do fosforilacije SMAD4, pomoću Erk kanonskog MAPK-mjesta, smeštenog na treonin 277. Ova fosforilacija ima dvostruki učinak na aktivnost SMAD4. Prvo, omogućava da dostigne svoj vrhunac transkripcijske aktivnosti, aktiviranjem faktorom rasta reguliranog domena za aktivaciju transkripcije koja se nalazi u regiji SMAD4 linkera, SAD (Smad-Activation Domain)).[19] Drugo, MAPK primari SMAD4-a za GSK3 posredovane fosforilacije koje uzrokuju inhibiciju transkripcije, a takođe generiraju fosfodegron koji se koristi kao mjesto pristajanja ubikvitinskih E3-ligaza beta-transducin ponavljajućih sadržaja (beta-TrCP), koji poliubikvitinira SMAD4 i razgrađuje ga u proteasomu.[20] Predložena je fosforilacija SMAD4 GSK3 za regulaciju stabilnosti proteina, tokom napredovanja gušteračinog raka i karcinoma debelog crijeva.[21]
U jedru, heteromerni kompleks veže promotore i stupa u interakciju s transkripcijskim aktivatorima. Kompleksi SMAD3/SMAD4 mogu direktno vezati SBE. Ove asocijacije su slabe i trebaju dodatne faktore transkripcije, kao što su članovi porodice AP-1, TFE3 i FoxG1, za regulaciju ekspresije gena.[22]
Mnogi ligandi TGFβ-a koriste ovaj put, a zatim je SMAD4 uključen u mnoge ćelijske funkcije kao što su diferencijacija, apoptoza, gastrulacija, embriogeneza i ćelijski ciklus.
Klinički značaj
[uredi | uredi izvor]Genetički eksperimenti poput nokaut-gena (KO), koji se sastoje u modificiranju ili inaktivaciji gena, mogu se izvesti kako bi se vidjeli efekti disfunkcionalnog SMAD4 na ispitivani organizam. Eksperimenti se često izvode na kućnom mišu (Mus musculus).
Pokazano je da u mišjem KO SMAD4 , zrnaste ćelije, koje luče hormone i faktore rasta tokom razvoja oocita, podvrgavaju se prijevremenoj luteinizaciji i izražavaju niže nivoe receptora za stimuliranje folikula (FSHR) i viši nivoi receptora luteinizirajućeg hormona (LHR). To je dijelom moguće zbog oštećenja efekata morfogenetskog proteina kostiju-7, jer BMP-7 koristi signalni put SMAD4.[23][24]
Delecije u genima koji kodiraju SMAD1 i SMAD5 također su povezane sa metastaznim tumorima granulastih ćelija kod miševa.[25]
SMAD4 je često mutiran kod mnogih karcinoma. Mutacija se može naslijediti ili steći tokom životnog vijeka. Ako se naslijedi, utiče i na somatske ćelije i na ćelije reproduktivnih organa. Ako se mutacija SMAD 4 stekne (de novo), postojat će samo u određenim somatskim ćelijama. Zapravo, SMAD 4 ne sintetiziraju sve ćelije. Protein je prisutan u ćelijama organa kao što su koža, gušterača, debelo crijevo, maternica i u epitelu. Takođe ga proizvode i fibroblasti.
Funkcionalni SMAD 4 sudjeluje u regulaciji puta transdukcije TGF-β signala, koji negativno regulira rast epitelnih ćelija i vanćelijski matriks (ECM). Kada se promijeni struktura SMAD 4, ekspresija gena uključenih u rast ćelija više nije regulirana i ćelijskaa proliferacija može trajati bez ikakve inhibicije. Veliki broj ćelijskih dioba dovodi do stvaranja tumora, a zatim do multiploidnih kolorektumskih karcinoma i karcinom pankreasa. Nalazi se inaktiviran u najmanje 50% karcinoma gušterače.[26]
Pokazalo se da somatske mutacije pronađene u humano ljudskom karcinomu domene MH1 SMAD 4 inhibiraju funkciju vezivanja DNK ovog domena.
Pronađen je i mutirani SMAD 4 kod osoba sa autosomno dominantnom bolešću sindrom juvenilne polipoze (JPS). JPS karakteriziraju hamartomatozni polipi u gastrointestinalnom traktu (GI). Ti polipi obično su benigni, ali su u većem riziku od razvoja gastrointestinalnog karcinoma, posebno karcinoma debelog crijeva. Utvrđeno je oko 60 mutacija koje uzrokuju JPS. Povezani su s proizvodnjom manjeg SMAD 4, s nedostajućim domenima koji sprečavaju protein da se veže za R-SMADS i stvara heteromerne komplekse.
Mutacije u SMAD4 (uglavnom supstitucije) mogu izazvati Myhreov sindrom, rijetki nasljedni poremećaj koji karakteriziraju mentalne smetnje, nizak rast, neobične crte lica i razne abnormalnosti kostiju.[27][28]
Reference
[uredi | uredi izvor]- ^ a b c GRCh38: Ensembl release 89: ENSG00000141646 - Ensembl, maj 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000024515 - Ensembl, maj 2017
- ^ "Human PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Mouse PubMed Reference:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ Massagué, Joan (2012). "TGFβ signalling in context". Nature Reviews Molecular Cell Biology (jezik: engleski). 13 (10): 616–630. doi:10.1038/nrm3434. ISSN 1471-0080. PMC 4027049. PMID 22992590.
- ^ "UniProt, Q13485". Pristupljeno September 12, 2017.
- ^ a b Massagué, J. (1998). "TGF-β SIGNAL TRANSDUCTION". Annual Review of Biochemistry. 67 (1): 753–791. doi:10.1146/annurev.biochem.67.1.753. ISSN 0066-4154. PMID 9759503.
- ^ "SMAD4 SMAD family member 4". Entrez Gene.
- ^ "SMAD 4". The Genetics Home Reference Website.
- ^ Zawel L, Dai JL, Buckhaults P, Zhou S, Kinzler KW, Vogelstein B, Kern SE (Mar 1998). "Human Smad3 and Smad4 are sequence-specific transcription activators". Molecular Cell. 1 (4): 611–617. doi:10.1016/s1097-2765(00)80061-1. PMID 9660945.
- ^ a b Martin-Malpartida, Pau; Batet, Marta; Kaczmarska, Zuzanna; Freier, Regina; Gomes, Tiago; Aragón, Eric; Zou, Yilong; Wang, Qiong; Xi, Qiaoran (12. 12. 2017). "Structural basis for genome wide recognition of 5-bp GC motifs by SMAD transcription factors". Nature Communications (jezik: engleski). 8 (1): 2070. Bibcode:2017NatCo...8.2070M. doi:10.1038/s41467-017-02054-6. ISSN 2041-1723. PMC 5727232. PMID 29234012.
- ^ Zhang, Ying; Feng, Xin-Hua; Derynck, Rik (1998). "Smad3 and Smad4 cooperate with c-Jun/c-Fos to mediate TGF-β-induced transcription". Nature. 394 (6696): 909–913. Bibcode:1998Natur.394..909Z. doi:10.1038/29814. ISSN 0028-0836. PMID 9732876. S2CID 4393852.
- ^ Baburajendran, Nithya; Jauch, Ralf; Tan, Clara Yueh Zhen; Narasimhan, Kamesh; Kolatkar, Prasanna R. (2011). "Structural basis for the cooperative DNA recognition by Smad4 MH1 dimers". Nucleic Acids Research. 39 (18): 8213–8222. doi:10.1093/nar/gkr500. ISSN 1362-4962. PMC 3185416. PMID 21724602.
- ^ Hata, Akiko; Lo, Roger S.; Wotton, David; Lagna, Giorgio; Massagué, Joan (1997). "Mutations increasing autoinhibition inactivate tumour suppressors Smad2 and Smad4". Nature. 388 (6637): 82–87. Bibcode:1997Natur.388R..82H. doi:10.1038/40424. ISSN 0028-0836. PMID 9214507. S2CID 4407819.
- ^ Sekelsky JJ, Newfeld SJ, Raftery LA, Chartoff EH, Gelbart WM (Mar 1995). "Genetic characterization and cloning of mothers against dpp, a gene required for decapentaplegic function in Drosophila melanogaster". Genetics. 139 (3): 1347–58. PMC 1206461. PMID 7768443.
- ^ White M (26. 9. 2014). "Sonic Hedgehog, DICER, and the Problem With Naming Genes". Pacific Standard.
- ^ Roelen BA, Cohen OS, Raychowdhury MK, Chadee DN, Zhang Y, Kyriakis JM, Alessandrini AA, Lin HY (Oct 2003). "Phosphorylation of threonine 276 in Smad4 is involved in transforming growth factor-beta-induced nuclear accumulation". American Journal of Physiology. Cell Physiology. 285 (4): C823–30. doi:10.1152/ajpcell.00053.2003. PMID 12801888.
- ^ Demagny H, Araki T, De Robertis EM (Oct 2014). "The tumor suppressor Smad4/DPC4 is regulated by phosphorylations that integrate FGF, Wnt, and TGF-β signaling". Cell Reports. 9 (2): 688–700. doi:10.1016/j.celrep.2014.09.020. PMID 25373906.
- ^ de Caestecker, Mark P. (2000). "The Smad4 Activation Domain (SAD) Is a Proline-rich, p300-dependent Transcriptional Activation Domain". The Journal of Biological Chemistry. 275 (3): 2115–2122. doi:10.1074/jbc.275.3.2115. PMID 10636916.
- ^ Demagny H, De Robertis EM (2015). "Smad4/DPC4: a Barrier against Tumor Progression driven by RTK/Ras/Erk and Wnt/GSK3 signaling". Molecular & Cellular Oncology. 3 (2): e989133. doi:10.4161/23723556.2014.989133. PMC 4905428. PMID 27308623.
- ^ Demagny H, De Robertis EM (2015). "Point Mutations in the Tumor Suppressor Smad4/DPC4 Enhance its Phosphorylation by GSK3 and Reversibly Inactivate TGF-β Signaling". Molecular & Cellular Oncology. 3 (1): e1025181. doi:10.1080/23723556.2015.1025181. PMC 4845174. PMID 27308538.
- ^ Inman GJ (Feb 2005). "Linking Smads and transcriptional activation". The Biochemical Journal. 386 (Pt 1): e1–e3. doi:10.1042/bj20042133. PMC 1134782. PMID 15702493.
- ^ Shi J, Yoshino O, Osuga Y, Nishii O, Yano T, Taketani Y (Mar 2010). "Bone morphogenetic protein 7 (BMP-7) increases the expression of follicle-stimulating hormone (FSH) receptor in human granulosa cells". Fertility and Sterility. 93 (4): 1273–9. doi:10.1016/j.fertnstert.2008.11.014. PMID 19108831.
- ^ Pangas SA, Li X, Robertson EJ, Matzuk MM (Jun 2006). "Premature luteinization and cumulus cell defects in ovarian-specific Smad4 knockout mice". Molecular Endocrinology. 20 (6): 1406–22. doi:10.1210/me.2005-0462. PMID 16513794.
- ^ Middlebrook BS, Eldin K, Li X, Shivasankaran S, Pangas SA (2009). "Smad1-Smad5 ovarian conditional knockout mice develop a disease profile similar to the juvenile form of human granulosa cell tumors". Endocrinology. 150 (12): 5208–17. doi:10.1210/en.2009-0644. PMC 2819741. PMID 19819941.
- ^ Cotran, Ramzi S.; Kumar, Vinay; Fausto, Nelson; Robbins, Stanley L.; Abbas, Abul K. (2005). Robbins and Cotran pathologic basis of disease (7th izd.). St. Louis, Mo: Elsevier Saunders. ISBN 0-7216-0187-1.
- ^ "Growth-Mental Deficiency Syndrome of Myhre". National Organization for rare disorders. Arhivirano s originala, 2. 4. 2015. Pristupljeno 6. 6. 2021.
- ^ Caputo V, Bocchinfuso G, Castori M, Traversa A, Pizzuti A, Stella L, Grammatico P, Tartaglia M (Jul 2014). "Novel SMAD4 mutation causing Myhre syndrome". American Journal of Medical Genetics Part A. 164A (7): 1835–40. doi:10.1002/ajmg.a.36544. PMID 24715504. S2CID 5294309.
Dopunska literatura
[uredi | uredi izvor]- Miyazono K (2000). "TGF-beta signaling by Smad proteins". Cytokine & Growth Factor Reviews. 11 (1–2): 15–22. doi:10.1016/S1359-6101(99)00025-8. PMID 10708949.
- Wrana JL, Attisano L (2000). "The Smad pathway". Cytokine & Growth Factor Reviews. 11 (1–2): 5–13. doi:10.1016/S1359-6101(99)00024-6. PMID 10708948.
- Verschueren K, Huylebroeck D (2000). "Remarkable versatility of Smad proteins in the nucleus of transforming growth factor-beta activated cells". Cytokine & Growth Factor Reviews. 10 (3–4): 187–99. doi:10.1016/S1359-6101(99)00012-X. PMID 10647776.
- Massagué J (1998). "TGF-beta signal transduction". Annual Review of Biochemistry. 67: 753–91. doi:10.1146/annurev.biochem.67.1.753. PMID 9759503.
- Klein-Scory S, Zapatka M, Eilert-Micus C, Hoppe S, Schwarz E, Schmiegel W, Hahn SA, Schwarte-Waldhoff I (2008). "High-level inducible Smad4-reexpression in the cervical cancer cell line C4-II is associated with a gene expression profile that predicts a preferential role of Smad4 in extracellular matrix composition". BMC Cancer. 7: 209. doi:10.1186/1471-2407-7-209. PMC 2186346. PMID 17997817.
- Kalo E, Buganim Y, Shapira KE, Besserglick H, Goldfinger N, Weisz L, Stambolsky P, Henis YI, Rotter V (Dec 2007). "Mutant p53 attenuates the SMAD-dependent transforming growth factor beta1 (TGF-beta1) signaling pathway by repressing the expression of TGF-beta receptor type II". Molecular and Cellular Biology. 27 (23): 8228–42. doi:10.1128/MCB.00374-07. PMC 2169171. PMID 17875924.
- Aretz S, Stienen D, Uhlhaas S, Stolte M, Entius MM, Loff S, Back W, Kaufmann A, Keller KM, Blaas SH, Siebert R, Vogt S, Spranger S, Holinski-Feder E, Sunde L, Propping P, Friedl W (Nov 2007). "High proportion of large genomic deletions and a genotype phenotype update in 80 unrelated families with juvenile polyposis syndrome". Journal of Medical Genetics. 44 (11): 702–9. doi:10.1136/jmg.2007.052506. PMC 2752176. PMID 17873119.
- Ali S, Cohen C, Little JV, Sequeira JH, Mosunjac MB, Siddiqui MT (Oct 2007). "The utility of SMAD4 as a diagnostic immunohistochemical marker for pancreatic adenocarcinoma, and its expression in other solid tumors". Diagnostic Cytopathology. 35 (10): 644–8. doi:10.1002/dc.20715. PMID 17854080. S2CID 36682992.
- Milet J, Dehais V, Bourgain C, Jouanolle AM, Mosser A, Perrin M, Morcet J, Brissot P, David V, Deugnier Y, Mosser J (Oct 2007). "Common variants in the BMP2, BMP4, and HJV genes of the hepcidin regulation pathway modulate HFE hemochromatosis penetrance". American Journal of Human Genetics. 81 (4): 799–807. doi:10.1086/520001. PMC 2227929. PMID 17847004.
- Salek C, Benesova L, Zavoral M, Nosek V, Kasperova L, Ryska M, Strnad R, Traboulsi E, Minarik M (Jul 2007). "Evaluation of clinical relevance of examining K-ras, p16 and p53 mutations along with allelic losses at 9p and 18q in EUS-guided fine needle aspiration samples of patients with chronic pancreatitis and pancreatic cancer". World Journal of Gastroenterology. 13 (27): 3714–20. doi:10.3748/wjg.v13.i27.3714. PMC 4250643. PMID 17659731.
- Sebestyén A, Hajdu M, Kis L, Barna G, Kopper L (Sep 2007). "Smad4-independent, PP2A-dependent apoptotic effect of exogenous transforming growth factor beta 1 in lymphoma cells". Experimental Cell Research. 313 (15): 3167–74. doi:10.1016/j.yexcr.2007.05.028. PMID 17643425.
- Martin MM, Buckenberger JA, Jiang J, Malana GE, Knoell DL, Feldman DS, Elton TS (Sep 2007). "TGF-beta1 stimulates human AT1 receptor expression in lung fibroblasts by cross talk between the Smad, p38 MAPK, JNK, and PI3K signaling pathways". American Journal of Physiology. Lung Cellular and Molecular Physiology. 293 (3): L790–9. doi:10.1152/ajplung.00099.2007. PMC 2413071. PMID 17601799.
- Levy L, Howell M, Das D, Harkin S, Episkopou V, Hill CS (Sep 2007). "Arkadia activates Smad3/Smad4-dependent transcription by triggering signal-induced SnoN degradation". Molecular and Cellular Biology. 27 (17): 6068–83. doi:10.1128/MCB.00664-07. PMC 1952153. PMID 17591695.
- Grijelmo C, Rodrigue C, Svrcek M, Bruyneel E, Hendrix A, de Wever O, Gespach C (Aug 2007). "Proinvasive activity of BMP-7 through SMAD4/src-independent and ERK/Rac/JNK-dependent signaling pathways in colon cancer cells". Cellular Signalling. 19 (8): 1722–32. doi:10.1016/j.cellsig.2007.03.008. PMID 17478078.
- Sonegawa H, Nukui T, Li DW, Takaishi M, Sakaguchi M, Huh NH (Jul 2007). "Involvement of deterioration in S100C/A11-mediated pathway in resistance of human squamous cancer cell lines to TGFbeta-induced growth suppression". Journal of Molecular Medicine. 85 (7): 753–62. doi:10.1007/s00109-007-0180-7. PMID 17476473. S2CID 15667203.
- Sheikh AA, Vimalachandran D, Thompson CC, Jenkins RE, Nedjadi T, Shekouh A, Campbell F, Dodson A, Prime W, Crnogorac-Jurcevic T, Lemoine NR, Costello E (Jun 2007). "The expression of S100A8 in pancreatic cancer-associated monocytes is associated with the Smad4 status of pancreatic cancer cells". Proteomics. 7 (11): 1929–40. doi:10.1002/pmic.200700072. PMID 17469085.
- Popović Hadzija M, Korolija M, Jakić Razumović J, Pavković P, Hadzija M, Kapitanović S (Apr 2007). "K-ras and Dpc4 mutations in chronic pancreatitis: case series". Croatian Medical Journal. 48 (2): 218–24. PMC 2080529. PMID 17436386.
- Losi L, Bouzourene H, Benhattar J (maj 2007). "Loss of Smad4 expression predicts liver metastasis in human colorectal cancer". Oncology Reports. 17 (5): 1095–9. doi:10.3892/or.17.5.1095. PMID 17390050.
- Karlsson G, Blank U, Moody JL, Ehinger M, Singbrant S, Deng CX, Karlsson S (Mar 2007). "Smad4 is critical for self-renewal of hematopoietic stem cells". The Journal of Experimental Medicine. 204 (3): 467–74. doi:10.1084/jem.20060465. PMC 2137898. PMID 17353364.
- Takano S, Kanai F, Jazag A, Ijichi H, Yao J, Ogawa H, Enomoto N, Omata M, Nakao A (Mar 2007). "Smad4 is essential for down-regulation of E-cadherin induced by TGF-beta in pancreatic cancer cell line PANC-1". Journal of Biochemistry. 141 (3): 345–51. doi:10.1093/jb/mvm039. PMID 17301079.
Vanjski linkovi
[uredi | uredi izvor]- GeneReviews/NCBI/NIH/UW entry on Hereditary Hemorrhagic Telangiectasia
- GeneReviews/NCBI/NIH/UW entry on Juvenile Polyposis Syndrome
- SMAD4 gene variant database