Abiraterone acetate
 | |
| Dữ liệu lâm sàng | |
|---|---|
| Tên thương mại | Zytiga, Yonsa, v.v... |
| Đồng nghĩa | CB-7630; JNJ-212082; 17-(3-Pyridinyl)androsta-5,16-dien-3β-ol acetate |
| AHFS/Drugs.com | Chuyên khảo |
| MedlinePlus | a611046 |
| Giấy phép |
|
| Danh mục cho thai kỳ | |
| Dược đồ sử dụng | Uống (thuốc viên)[1] |
| Mã ATC | |
| Tình trạng pháp lý | |
| Tình trạng pháp lý | |
| Dữ liệu dược động học | |
| Sinh khả dụng | Không rõ, nhưng có thể đạt tối đa 50% khi dạ dày rỗng.[3] |
| Liên kết protein huyết tương | Abiraterone: ~99.8% (với albumin và α1-AGp)[1][3][2] |
| Chuyển hóa dược phẩm | Esterase, CYP3A4, SULT2A1[2] |
| Chất chuyển hóa | Abiraterone, khác[1][3] |
| Chu kỳ bán rã sinh học | Abiraterone: 12–24 giờ[1][3] |
| Bài tiết | Phân: 88%[1][2] Nước tiểu: 5%[1][2] |
| Các định danh | |
Tên IUPAC
| |
| Số đăng ký CAS |
|
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| Định danh thành phần duy nhất | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| ECHA InfoCard | 100.149.063 |
| Dữ liệu hóa lý | |
| Công thức hóa học | C26H33NO2 |
| Khối lượng phân tử | 391,56 g·mol−1 |
| Mẫu 3D (Jmol) | |
| Điểm nóng chảy | 144 đến 145 °C (291 đến 293 °F) [4] |
SMILES
| |
Định danh hóa học quốc tế
| |
| (kiểm chứng) | |
Abiraterone acetate, được bán dưới các nhãn hiệu Zytiga, Yonsa và một số tên gọi khác, là một antiandrogen được sử dụng trong điều trị ung thư tuyến tiền liệt.[1] Nó được chỉ định đặc biệt để sử dụng kết hợp với corticosteroid như prednison để điều trị ung thư tuyến tiền liệt kháng cắt tinh hoàn di căn (mCRPC) và trong điều trị ung thư tuyến tiền liệt nhạy cảm với cắt tinh hoàn nguy cơ di căn cao (mCSPC).[1] Nó được dùng bằng đường uống một lần mỗi ngày khi bụng đói.[1] Một công thức khác là Yonsa, có thể uống cùng hoặc không cùng thức ăn, với liều thấp hơn.[5]
Tác dụng phụ của abiraterone acetate bao gồm mệt mỏi, đau khớp, tăng huyết áp, buồn nôn, phù, hạ kali máu, bốc hỏa, tiêu chảy, nôn mửa, ho, nhức đầu, thiếu glucocorticoid, tăng aldosterone và nhiễm độc gan.[1] Thuốc là một chất ức chế tổng hợp androgen - cụ thể là chất ức chế CYP17A1 - và do đó ức chế sản xuất nội tiết tố androgen như testosterone và dihydrotestosterone trong cơ thể.[1] Làm như vậy, nó ngăn chặn tác động của các hormone này trong tuyến tiền liệt và các nơi khác trong cơ thể.[1] Abiraterone acetate là một tiền chất của abiraterone.[1]
Abiraterone acetate được mô tả lần đầu tiên vào năm 1993 và được giới thiệu sử dụng trong y tế vào năm 2011.[6][7][8] Nó đã được phê duyệt để điều trị mCRPC vào năm 2011 và sau đó đã được phê duyệt để điều trị mCSPC vào năm 2018.[9] Thuốc được bán trên thị trường rộng rãi trên toàn thế giới.[10] Nó có sẵn như là một loại thuốc gốc từ Apotex Corp, với chi phí tương tự.[11]
Sử dụng trong y tế
[sửa | sửa mã nguồn]Ung thư tuyến tiền liệt
[sửa | sửa mã nguồn]Abiraterone acetate được chỉ định để sử dụng kết hợp với prednison, một loại corticosteroid, như một phương pháp điều trị cho mCRPC (trước đây gọi là ung thư tuyến tiền liệt kháng hormone hoặc kháng hormone).[12][13][14][15] Đây là một dạng ung thư tuyến tiền liệt không đáp ứng với điều trị thiếu hụt androgen đầu tiên hoặc điều trị bằng thuốc đối kháng thụ thể androgen. Abiraterone acetate đã nhận được phê duyệt của FDA (28 tháng 4 năm 2011), EMA (23 tháng 9 năm 2011), MHRA (5 tháng 9 năm 2011) và TGA (1 tháng 3 năm 2012) cho chỉ định này.[12][13][14][15] Ở Úc, nó được bảo hiểm bởi Chương trình Phúc lợi Dược phẩm khi được sử dụng để điều trị ung thư tuyến tiền liệt kháng cắt tinh hoàn và được kết hợp với prednison/prednisolone (tùy theo các điều kiện như bệnh nhân hiện không được hóa trị liệu, kháng hoặc không dung nạp docetaxel, có tình trạng thể trạng theo phân loại của WHO <2 và bệnh của anh ta đã không tiến triển kể từ khi điều trị bằng abiraterone acetate do PBS trợ cấp đã bắt đầu).[16]
Abiraterone có thể hữu ích để ngăn ngừa sự bùng phát testosterone khi bắt đầu điều trị bằng thuốc hoạt hóa GnRH ở nam giới bị ung thư tuyến tiền liệt.[17]
Hiệu quả lâm sàng
[sửa | sửa mã nguồn]Một nghiên cứu giai đoạn III với các đối tượng trước đây được điều trị bằng docetaxel bắt đầu vào năm 2008.[18] Vào tháng 9 năm 2010, một hội đồng độc lập đã phát hiện ra rằng kết quả tạm thời ở những bệnh nhân trước đây được điều trị bằng docetaxel tốt hơn rất nhiều so với những người được điều trị bằng giả dược đến nỗi việc giữ một nửa số người tham gia nghiên cứu trên giả dược là không hợp lý và tất cả bệnh nhân bắt đầu dùng thuốc. Tỷ lệ sống sót chung đã tăng thêm 3,9 tháng trong nghiên cứu này (14,8 tháng so với 10,9 tháng đối với giả dược).[19]
Một nghiên cứu ngẫu nhiên, mù đôi, đối chứng giả dược ở giai đoạn III ở bệnh nhân ung thư tuyến tiền liệt cắt tinh hoàn nhưng không được hóa trị liệu đã được tích lũy vào tháng 4 năm 2009.[20][21] 1.088 người đàn ông đã dùng abiraterone acetate (1000 mg mỗi ngày) cộng với prednison (5 mg hai lần mỗi ngày), hoặc giả dược cộng với prednison. Thời gian sống không tiến triển bằng X quang trung bình là 16,5 tháng với abiraterone acetate + prednison và 8,3 tháng chỉ dùng prednison (Tỷ lệ may rủi (HR) = 0,53; khoảng tin cậy (CI) 95% = 0,45-0,62; Sau thời gian theo dõi trung bình 22,2 tháng, tỷ lệ sống sót cao hơn với abiraterone acetate + prednison (không đạt được trung vị) so với giả dược + prednison (27,2 tháng); HR = 0,75; CI 95% = 0,61-0,93; P = 0,01).[22]
Các dạng có sẵn
[sửa | sửa mã nguồn]Abiraterone acetate có sẵn ở dạng viên nén có vỏ 250 mg, 500 mg và 250 mg viên nén không vỏ.[1] Nó được sử dụng với liều 1.000 mg uống một lần mỗi ngày khi bụng đói, kết hợp với cắt bỏ tinh hoàn (thông qua liệu pháp tương tự GnRH hoặc cắt bỏ tinh hoàn) và kết hợp với 5 mg prednison uống hai lần mỗi ngày.[1]
Chống chỉ định
[sửa | sửa mã nguồn]Chống chỉ định bao gồm quá mẫn cảm với abiraterone acetate. Mặc dù các tài liệu nói rằng các phụ nữ đang hoặc có thể mang thai không nên dùng,[13][23] nhưng cũng không có lý do y tế nào để bất kỳ người phụ nữ nào cũng nên dùng nó. Phụ nữ đang mang thai thậm chí không nên chạm vào thuốc trừ khi họ đang đeo găng tay.[23] Các cảnh báo khác bao gồm suy gan nặng cơ bản, chứng tăng aldosterone, bệnh tim mạch bao gồm suy tim và tăng huyết áp, hạ kali máu không được điều trị và suy adrenocorticoid.[24]
Tác dụng phụ
[sửa | sửa mã nguồn]Tác dụng phụ theo tần suất: [12][13][14][15][24]
Rất phổ biến (tần suất> 10%):
Phổ biến (tần suất 1-10%):
Không phổ biến (tần suất 0,1-1%):
Hiếm (tần suất <0,1%):
- Viêm phế nang dị ứng
Quá liều
[sửa | sửa mã nguồn]Kinh nghiệm lâm sàng khi dùng quá liều abiraterone acetate còn hạn chế.[1] Không có thuốc giải độc đặc hiệu cho quá liều abiraterone acetate, và điều trị nên bao gồm các biện pháp hỗ trợ chung, bao gồm theo dõi chức năng tim và gan.[1]
Tương tác
[sửa | sửa mã nguồn]Abiraterone acetate là chất nền CYP3A4 và do đó không nên dùng đồng thời với các thuốc ức chế CYP3A4 mạnh như ketoconazole, itraconazole, clarithromycin, atazanavir, rifabutin, rifapentine, phenobarbital.[23][24] Nó cũng ức chế CYP1A2, CYP2C9 và CYP3A4 và tương tự không nên dùng đồng thời với cơ chất của bất kỳ enzym nào có chỉ số điều trị hẹp.[23][24]
Spironolactone thường có tác dụng chống androgen, nhưng bằng chứng thực nghiệm cho thấy nó hoạt động như một chất chủ vận thụ thể androgen trong môi trường thiếu androgen, có khả năng gây ra sự tăng sinh ung thư tuyến tiền liệt.[25] Điều này được hỗ trợ bởi các quan sát được mô tả trong một số báo cáo trường hợp.[26] Do đó, nên tránh dùng spironolactone ở những bệnh nhân ung thư tuyến tiền liệt bị tác dụng phụ liên quan đến điều trị bằng thuốc diệt nấm liên quan đến điều trị bằng Abiraterone acetate.
Dược lý
[sửa | sửa mã nguồn]Dược lực học
[sửa | sửa mã nguồn]
Hoạt động antiandrogen
[sửa | sửa mã nguồn]Abiraterone, chất chuyển hóa hoạt động của abiraterone acetate, ức chế CYP17A1, một enzyme hoạt tính kép gồm hoạt tính của 17α-hydroxylase và hoạt tính của 17,20 lyase. Abiraterone ức chế hoạt tính 17α-hydroxylase (IC50 = 2,5 nM) mạnh hơn sự ức chế hoạt tính 17,20-lyase (IC50 = 15 nM) [27][28] được biểu hiện ở các mô khối u tinh hoàn, tuyến thượng thận và tuyến tiền liệt. CYP17A1 xúc tác cho hai phản ứng tuần tự: (a) Chuyển hóa pregnenolone và progesterone thành các dẫn xuất 17α-hydroxy của chúng bằng hoạt tính 17α-hydroxylase của nó, (b) chuyển hóa 17-hydroxypregnenolone thành dehydroepiandrosterone (DHEA) và chuyển hóa 17-hydroxyprogesterone thành androstenedione bằng hoạt tính 17,20-lyase.[29] DHEA và androstenedione là các androgen và là tiền chất của testosterone. Ức chế hoạt động CYP17A1 của abiraterone acetate do đó làm giảm mức độ trong hệ tuần hoàn của các androgen như DHEA, testosterone và dihydrotestosterone (DHT). Abiraterone acetate, thông qua chất chuyển hóa abiraterone, có khả năng làm giảm mức testosterone tuần hoàn xuống dưới 1 ng/dL (nghĩa là không thể phát hiện) khi được bổ sung cho việc cắt tinh hoàn.[27][30] Các nồng độ này thấp hơn đáng kể so với nồng độ đạt được chỉ bằng cách cắt tinh hoàn (~ 20 ng/dL).[30] Việc bổ sung abiraterone acetate với cắt tinh hoàn đã làm giảm lượng DHT 85%, DHEA từ 97 đến 98% và androstenedione 77 đến 78% so với chỉ cắt tinh hoàn.[30] Cũng do tác dụng ức chế androgen nên abiraterone acetate làm giảm trọng lượng của tuyến tiền liệt, túi tinh và tinh hoàn.[31]
Abiraterone cũng hoạt động như một chất đối kháng một phần của thụ thể androgen (AR) và là chất ức chế các enzyme 3β-hydroxapseoid dehydrogenase (3β-HSD), CYP11B1 (steroid 11β-hydroxylase), CYP21A2 (Steroid 21-hydroxylase) CYP450 (ví dụ, CYP1A2, CYP2C9 và CYP3A4).[24][32][33][34] Ngoài abiraterone, một phần hoạt động của thuốc đã được tìm thấy là do một chất chuyển hóa có hiệu lực mạnh hơn, δ 4 -abiraterone (D4A), được hình thành từ abiraterone thông qua 3β-HSD.[35] D4A là một chất ức chế CYP17A1, 3β-hydroxysteroid dehydrogenase / Δ 5-4 isomerase, và 5α-reductase, và cũng được báo cáo là hoạt động như một chất đối kháng cạnh tranh của AR ở mức độ có thể so sánh với chất đối kháng mạnh enzalutamide.[35] Tuy nhiên, một sản phẩm chuyển hóa của D4A, 3-keto-5α-abiraterone, là chất chủ vận AR, và thúc đẩy tiến triển ung thư tuyến tiền liệt.[36] Sự hình thành của nó có thể bị chặn bằng cách sử dụng đồng thời dutasteride, một chất ức chế 5α-reductase mạnh và chọn lọc.[36]
Hoạt động estrogen
[sửa | sửa mã nguồn]Đã có sự quan tâm trong việc sử dụng abiraterone acetate để điều trị ung thư vú do khả năng hạ thấp mức estrogen.[37] Tuy nhiên, abiraterone đã được tìm thấy hoạt động như một chất hoạt hóa trực tiếp của thụ thể estrogen và gây ra sự tăng sinh của các tế bào ung thư vú người trong ống nghiệm.[37] Nếu abiraterone acetate được sử dụng trong điều trị ung thư vú, nó nên được kết hợp với một chất đối kháng thụ thể estrogen như Fulvestrant.[37] Mặc dù có đặc tính chống ung thư và estrogen, abiraterone acetate dường như không tạo ra nở vú như một tác dụng phụ.[38]
Các hoạt động khác
[sửa | sửa mã nguồn]Do ức chế sinh tổng hợp glucocorticoid, abiraterone acetate có thể gây thiếu hụt glucocorticoid, chứng tăng aldosterone và các tác dụng phụ liên quan.[39] Đây là lý do tại sao thuốc được kết hợp với prednison, một corticosteroid, phục vụ như một phương tiện thay thế glucocorticoid và ngăn ngừa tăng aldosterone.[40]
Abiraterone acetate, cùng với galeterone, đã được xác định là một chất ức chế sulfotransferase (SULT2A1, SULT2B1b, SULT1E1), tham gia vào sulfat hóa DHEA và các steroid cùng các hợp chất nội sinh khác, với các giá trị Ki trong phạm vi tiểu vi phân tử.[41]
Dược động học
[sửa | sửa mã nguồn]Sau khi uống, abiraterone acetate, dạng tiền dược trong chế phẩm thương mại, được chuyển thành dạng hoạt động, abiraterone. Chuyển đổi này có khả năng là qua trung gian esterase và không qua trung gian CYP. Uống cùng với thực phẩm làm tăng sự hấp thụ của thuốc và do đó có khả năng dẫn đến phơi nhiễm tăng và biến đổi cao; Thuốc nên được uống khi bụng đói ít nhất một giờ trước hoặc hai giờ sau khi ăn. Thuốc có liên kết với protein cao (> 99%) và được chuyển hóa ở gan bởi CYP3A4 và SULT2A1 thành các chất chuyển hóa không hoạt động. Thuốc được bài tiết qua phân (~88%) và nước tiểu (~5%), và có thời gian bán hủy cuối cùng là 12 ± 5 giờ.[23]
Hóa học
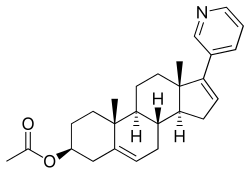
[sửa | sửa mã nguồn]Abiraterone acetate, còn được gọi là 17-(3-pyridinyl) androsta-5,16-dien-3β-ol acetate, là một steroid androstane tổng hợp và là một dẫn xuất của androstadienol (androsta-5,16-dien-3β-ol), một pheromone nội sinh. Nó đặc biệt là một dẫn xuất của androstadienol với một vòng pyridin được gắn ở vị trí C17 và một este axetat gắn vào nhóm hydroxyl C3β. Abiraterone acetate là este acetate C3β của abiraterone.
Lịch sử
[sửa | sửa mã nguồn]Đầu những năm 1990, Mike Jarman, Elaine Barrie và Gerry Potter thuộc Trung tâm Điều trị Ung thư của Trung tâm Nghiên cứu Ung thư Vương quốc Anh tại Viện Nghiên cứu Ung thư ở London đã bắt đầu phát triển các phương pháp điều trị thuốc điều trị ung thư tuyến tiền liệt. Với mô hình ức chế tổng hợp androgen không steroid ketoconazole như một mô hình, họ đã phát triển abiraterone, nộp bằng sáng chế vào năm 1993 và xuất bản bài báo đầu tiên mô tả nó vào năm sau.[6][42] Quyền thương mại hóa thuốc đã được giao cho BTG, một công ty chăm sóc sức khỏe chuyên khoa có trụ sở tại Anh. BTG sau đó đã cấp phép sản phẩm cho Cougar Biotech, bắt đầu phát triển sản phẩm thương mại.[43] Năm 2009, Cougar được Johnson & Johnson mua lại, công ty đã phát triển và bán sản phẩm thương mại và đang tiến hành các thử nghiệm lâm sàng liên tục để mở rộng sử dụng lâm sàng.[44]
Abiraterone acetate đã được Cục quản lý Thực phẩm và Dược phẩm Hoa Kỳ phê duyệt vào ngày 28 tháng 4 năm 2011.[7][8] Thông cáo báo chí của FDA đã đề cập đến một thử nghiệm lâm sàng giai đoạn III trong đó sử dụng abiraterone acetate có liên quan đến tỷ lệ sống trung bình là 14,8 tháng so với 10,9 tháng với giả dược; nghiên cứu đã được dừng lại sớm vì kết quả thành công.[45] Abiraterone acetate cũng được Cơ quan Dược phẩm Châu Âu cấp phép.[46] Cho đến tháng 5 năm 2012, Viện Y tế và Ưu tú Lâm sàng Quốc gia (NICE) đã không khuyến nghị sử dụng thuốc trong NHS với các lý do liên quan tới chi phí-hiệu quả. Quan điểm này đã bị đảo ngược khi nhà sản xuất nộp các mức chi phí sửa đổi.[47] Việc sử dụng hiện chỉ giới hạn ở nam giới đã nhận một chế độ hóa trị liệu có chứa docetaxel.[48][49] Vào tháng 5 năm 2019, Tòa phúc thẩm Liên bang Hoa Kỳ đã giữ nguyên quyết định của Hội đồng xét xử bằng sáng chế và Hội đồng phúc thẩm vô hiệu hóa bằng sáng chế về thuốc trị ung thư tuyến tiền liệt của Johnson & Johnson Zytiga.[50]
Xã hội và văn hoá
[sửa | sửa mã nguồn]Tên gốc
[sửa | sửa mã nguồn]Abiraterone acetate là tên gốc của thuốc và USAN, BANM và JAN, trong khi abiraterone là INN và BAN của abiraterone, dạng khử hoạt tính của nó.[10] Abiraterone acetate còn được biết đến với tên mã phát triển CB-7630 và JNJ-212082, trong khi CB-7598 là tên mã phát triển của abiraterone.[10][51]
Tính khả dụng
[sửa | sửa mã nguồn]Abiraterone acetate được bán rộng rãi trên toàn thế giới, bao gồm ở Hoa Kỳ, Canada, Vương quốc Anh, Ireland, những nơi khác ở Châu Âu, Úc, New Zealand, Châu Mỹ Latinh, Châu Á và Israel.[10]
Xem thêm
[sửa | sửa mã nguồn]Tham khảo
[sửa | sửa mã nguồn]- ^ a b c d e f g h i j k l m n o p q Janssen Biotech, Inc. “ZYTIGA Prescribing Information” (PDF). Horsham, PA: U.S. Food and Drug Administration.
- ^ a b c d “Meeting Library - Meeting Library”. meetinglibrary.asco.org. Bản gốc lưu trữ ngày 20 tháng 9 năm 2016. Truy cập ngày 30 tháng 6 năm 2019.
- ^ a b c d Benoist GE, Hendriks RJ, Mulders PF, Gerritsen WR, Somford DM, Schalken JA, van Oort IM, Burger DM, van Erp NP (tháng 11 năm 2016). “Pharmacokinetic Aspects of the Two Novel Oral Drugs Used for Metastatic Castration-Resistant Prostate Cancer: Abiraterone Acetate and Enzalutamide”. Clin Pharmacokinet. 55 (11): 1369–1380. doi:10.1007/s40262-016-0403-6. PMC 5069300. PMID 27106175.
- ^ Potter et al., 1995. J. Med. Chem. 38 (13): 2463–2471
- ^ “Sun Pharma Gets FDA Go-Ahead for Yonsa for Prostate Cancer”. BioSpace. Truy cập ngày 16 tháng 5 năm 2019.
- ^ a b “Where did abiraterone come from?”. Cancer Research UK. ngày 21 tháng 9 năm 2011. Bản gốc lưu trữ ngày 25 tháng 9 năm 2011. Truy cập ngày 28 tháng 9 năm 2011.
- ^ a b “Drugs@FDA - FDA Approved Drug Products - Zytiga”. www.fda.gov. United States Food and Drug Administration. Truy cập ngày 4 tháng 3 năm 2016.
- ^ a b “FDA approves Zytiga for late-stage prostate cancer” (Thông cáo báo chí). United States Food and Drug Administration. ngày 28 tháng 4 năm 2011.
- ^ NCI Staff. “Abiraterone Approved for Earlier Use in Men with Metastatic Prostate Cancer”. U.S. Department of Health and Human Services, National Institutes of Health, National Cancer Institute.
- ^ a b c d “Abiraterone”. Drugs.com.
- ^ “Generic Zytiga Availability”. Drugs.com.
- ^ a b c “Zytiga (abiraterone acetate) tablet [Janssen Biotech, Inc.]”. DailyMed. Janssen Biotech, Inc. tháng 9 năm 2013. Truy cập ngày 24 tháng 1 năm 2014.
- ^ a b c d “Zytiga: EPAR - Product Information” (PDF). European Medicines Agency. Janssen-Cilag International N.V. ngày 29 tháng 10 năm 2013. Bản gốc (PDF) lưu trữ ngày 17 tháng 6 năm 2018. Truy cập ngày 24 tháng 1 năm 2014.
- ^ a b c “Zytiga 250 mg tablets - Summary of Product Characteristics”. electronic Medicines Compendium. Janssen-Cilag Ltd. ngày 21 tháng 1 năm 2014. Bản gốc lưu trữ ngày 1 tháng 2 năm 2014. Truy cập ngày 24 tháng 1 năm 2014.
- ^ a b c “Zytiga abiraterone acetate product information” (PDF). TGA eBusiness Services. Janssen-Cilag Pty Ltd. ngày 1 tháng 3 năm 2012. Truy cập ngày 24 tháng 1 năm 2014.
- ^ “Pharmaceutical Benefits Scheme - Abiraterone”. Pharmaceutical Benefits Scheme. Truy cập ngày 24 tháng 1 năm 2014.
- ^ Pokuri VK, Nourkeyhani H, Betsy B, Herbst L, Sikorski M, Spangenthal E, Fabiano A, George S (tháng 7 năm 2015). “Strategies to Circumvent Testosterone Surge and Disease Flare in Advanced Prostate Cancer: Emerging Treatment Paradigms”. J Natl Compr Canc Netw. 13 (7): e49–55. doi:10.6004/jnccn.2015.0109. PMID 26150586.
- ^ Clinical trial number NCT00638690 for "Abiraterone Acetate in Castration-Resistant Prostate Cancer Previously Treated With Docetaxel-Based Chemotherapy" at ClinicalTrials.gov
- ^ de Bono JS, Logothetis CJ, Molina A, Fizazi K, North S, Chu L, Chi KN, Jones RJ, Goodman OB, Saad F, Staffurth JN, Mainwaring P, Harland S, Flaig TW, Hutson TE, Cheng T, Patterson H, Hainsworth JD, Ryan CJ, Sternberg CN, Ellard SL, Fléchon A, Saleh M, Scholz M, Efstathiou E, Zivi A, Bianchini D, Loriot Y, Chieffo N, Kheoh T, Haqq CM, Scher HI (tháng 5 năm 2011). “Abiraterone and increased survival in metastatic prostate cancer”. The New England Journal of Medicine. 364 (21): 1995–2005. doi:10.1056/NEJMoa1014618. PMC 3471149. PMID 21612468.
- ^ Clinical trial number NCT00887198 for "Abiraterone Acetate in Asymptomatic or Mildly Symptomatic Patients With Metastatic Castration-Resistant Prostate Cancer" at ClinicalTrials.gov
- ^ “BTG and Ortho Biotech's Prostate Cancer Trial Unblinded”. Genetic Engineering & Biotechnology News. ngày 10 tháng 9 năm 2010. Truy cập ngày 26 tháng 5 năm 2011.
- ^ Ryan CJ, Smith MR, de Bono JS, Molina A, Logothetis CJ, de Souza P, Fizazi K, Mainwaring P, Piulats JM, Ng S, Carles J, Mulders PF, Basch E, Small EJ, Saad F, Schrijvers D, Van Poppel H, Mukherjee SD, Suttmann H, Gerritsen WR, Flaig TW, George DJ, Yu EY, Efstathiou E, Pantuck A, Winquist E, Higano CS, Taplin ME, Park Y, Kheoh T, Griffin T, Scher HI, Rathkopf DE (tháng 1 năm 2013). “Abiraterone in metastatic prostate cancer without previous chemotherapy”. The New England Journal of Medicine. 368 (2): 138–148. doi:10.1056/NEJMoa1209096. PMC 3683570. PMID 23228172.
- ^ a b c d e “Zytiga prescribing information” (PDF). Janssen Biotech. tháng 5 năm 2012. Bản gốc (pdf) lưu trữ ngày 13 tháng 11 năm 2014. Truy cập ngày 4 tháng 3 năm 2016.
- ^ a b c d e “Zytiga (abiraterone) dosing, indications, interactions, adverse effects, and more”. Medscape Reference. WebMD. Truy cập ngày 24 tháng 1 năm 2014.
- ^ Luthy IA, Begin DJ, Labrie F (tháng 11 năm 1988). “Androgenic activity of synthetic progestins and spironolactone in androgen-sensitive mouse mammary carcinoma (Shionogi) cells in culture”. Journal of Steroid Biochemistry. 31 (5): 845–52. doi:10.1016/0022-4731(88)90295-6. PMID 2462135.
- ^ Dhondt B, Buelens S, Van Besien J, Beysens M, De Bleser E, Ost P, Lumen N (tháng 11 năm 2018). “Abiraterone and spironolactone in prostate cancer: a combination to avoid”. Acta Clinica Belgica: 1–6. doi:10.1080/17843286.2018.1543827. PMID 30477405.
- ^ a b Neidle S (ngày 30 tháng 9 năm 2013). Cancer Drug Design and Discovery. Academic Press. tr. 341–342. ISBN 978-0-12-397228-6.
- ^ Fernández-Cancio M, Camats N, Flück CE, Zalewski A, Dick B, Frey BM, Monné R, Torán N, Audí L, Pandey AV (tháng 4 năm 2018). “Mechanism of the Dual Activities of Human CYP17A1 and Binding to Anti-Prostate Cancer Drug Abiraterone Revealed by a Novel V366M Mutation Causing 17,20 Lyase Deficiency”. Pharmaceuticals. 11 (2): 37. doi:10.3390/ph11020037. PMID 29710837.
- ^ Attard G, Belldegrun AS, de Bono JS (tháng 12 năm 2005). “Selective blockade of androgenic steroid synthesis by novel lyase inhibitors as a therapeutic strategy for treating metastatic prostate cancer”. BJU International. 96 (9): 1241–6. doi:10.1111/j.1464-410X.2005.05821.x. PMID 16287438.
- ^ a b c Small EJ (tháng 11 năm 2014). “Can targeting the androgen receptor in localized prostate cancer provide insights into why men with metastatic castration-resistant prostate cancer die?”. Journal of Clinical Oncology. 32 (33): 3689–91. doi:10.1200/JCO.2014.57.8534. PMID 25311216.
Abiraterone acetate is a prodrug for abiraterone, a CYP17 inhibitor, which has the capacity to lower serum testosterone levels to less than 1 ng/dL (compared with levels closer to 20 ng/dL that are achieved with conventional ADT).19 [...] Relative to LHRHa alone, the addition of abiraterone resulted in an 85% decline in dihydrotestosterone (DHT) levels, a 97% to 98% decline in dehydroepiandrosterone (DHEA) levels, and a 77% to 78% decline in androstenedione levels.
- ^ Tindall DJ, James M (ngày 20 tháng 4 năm 2009). Androgen Action in Prostate Cancer. Springer Science & Business Media. tr. 748–. ISBN 978-0-387-69179-4.
- ^ Yin L, Hu Q (tháng 1 năm 2014). “CYP17 inhibitors--abiraterone, C17,20-lyase inhibitors and multi-targeting agents”. Nature Reviews. Urology. 11 (1): 32–42. doi:10.1038/nrurol.2013.274. PMID 24276076.
- ^ Malikova J, Brixius-Anderko S, Udhane SS, Parween S, Dick B, Bernhardt R, Pandey AV (tháng 11 năm 2017). “CYP17A1 inhibitor abiraterone, an anti-prostate cancer drug, also inhibits the 21-hydroxylase activity of CYP21A2”. The Journal of Steroid Biochemistry and Molecular Biology. 174: 192–200. doi:10.1016/j.jsbmb.2017.09.007. PMID 28893623.
- ^ Udhane SS, Dick B, Hu Q, Hartmann RW, Pandey AV (tháng 9 năm 2016). “Specificity of anti-prostate cancer CYP17A1 inhibitors on androgen biosynthesis”. Biochemical and Biophysical Research Communications. 477 (4): 1005–1010. doi:10.1016/j.bbrc.2016.07.019. PMID 27395338.
- ^ a b Li Z, Bishop AC, Alyamani M, Garcia JA, Dreicer R, Bunch D, Liu J, Upadhyay SK, Auchus RJ, Sharifi N (tháng 7 năm 2015). “Conversion of abiraterone to D4A drives anti-tumour activity in prostate cancer”. Nature. 523 (7560): 347–51. doi:10.1038/nature14406. PMC 4506215. PMID 26030522.
- ^ a b Li Z, Alyamani M, Li J, Rogacki K, Abazeed M, Upadhyay SK, Balk SP, Taplin ME, Auchus RJ, Sharifi N (tháng 5 năm 2016). “Redirecting abiraterone metabolism to fine-tune prostate cancer anti-androgen therapy” (PDF). Nature. 533 (7604): 547–51. doi:10.1038/nature17954. PMID 27225130.
- ^ a b c Capper CP, Larios JM, Sikora MJ, Johnson MD, Rae JM (tháng 5 năm 2016). “The CYP17A1 inhibitor abiraterone exhibits estrogen receptor agonist activity in breast cancer”. Breast Cancer Research and Treatment. 157 (1): 23–30. doi:10.1007/s10549-016-3774-3. PMID 27083183.
- ^ Alesini D, Iacovelli R, Palazzo A, Altavilla A, Risi E, Urbano F, Manai C, Passaro A, Magri V, Cortesi E (2013). “Multimodality treatment of gynecomastia in patients receiving antiandrogen therapy for prostate cancer in the era of abiraterone acetate and new antiandrogen molecules”. Oncology. 84 (2): 92–9. doi:10.1159/000343821. PMID 23128186.
- ^ Figg WD, Chau CH, Small EJ (ngày 14 tháng 9 năm 2010). Drug Management of Prostate Cancer. Springer Science & Business Media. tr. 97. ISBN 978-1-60327-829-4.
- ^ Rosenthal L, Burchum J (ngày 17 tháng 2 năm 2017). Lehne's Pharmacotherapeutics for Advanced Practice Providers - E-Book. Elsevier Health Sciences. tr. 936. ISBN 978-0-323-44779-9.
- ^ Yip CK, Bansal S, Wong SY, Lau AJ (tháng 4 năm 2018). “Identification of Galeterone and Abiraterone as Inhibitors of Dehydroepiandrosterone Sulfonation Catalyzed by Human Hepatic Cytosol, SULT2A1, SULT2B1b, and SULT1E1”. Drug Metabolism and Disposition. 46 (4): 470–482. doi:10.1124/dmd.117.078980. PMID 29436390.
- ^ “A new way to treat prostate cancer: The story of abiraterone”. The Institute of Cancer Research. ngày 10 tháng 9 năm 2012. Truy cập ngày 12 tháng 11 năm 2012.
- ^ “Abiraterone Acetate (CB7630)”. Cougar Biotechnology. Bản gốc lưu trữ ngày 7 tháng 9 năm 2008. Truy cập ngày 20 tháng 8 năm 2008.
- ^ “Johnson & Johnson Announces Definitive Agreement to Acquire Cougar Biotechnology, Inc” (Thông cáo báo chí). Cougar Biotechnology. ngày 11 tháng 5 năm 2009. Bản gốc lưu trữ ngày 29 tháng 5 năm 2009. Truy cập ngày 3 tháng 6 năm 2009.
- ^ “FDA Approval for Abiraterone Acetate”. U.S. Department of Health and Human Services, National Institutes of Health, National Cancer Institute. Bản gốc lưu trữ ngày 28 tháng 7 năm 2011. Truy cập ngày 30 tháng 6 năm 2019.
- ^ “EMA assessment of Zytiga (abiraterone)”. European Medicines Agency. Bản gốc lưu trữ ngày 20 tháng 6 năm 2018. Truy cập ngày 21 tháng 1 năm 2022.
- ^ “Prostate cancer (metastatic, castration resistant) - abiraterone (following cytoxic therapy): final appraisal determination guidance” (PDF). NICE guidance. ngày 15 tháng 5 năm 2012. Bản gốc (PDF) lưu trữ ngày 19 tháng 2 năm 2013.
- ^ “NICE technology appraisal guidance [TA259]”. NICE guidance. tháng 6 năm 2012.
- ^ “NICE appraisal of earlier treatment with abiraterone for prostate cancer”. NICE press release. ngày 14 tháng 8 năm 2014.
- ^ Bultman, Matthew. “Fed. Circ. Backs PTAB Ax Of J&J Prostate Cancer Drug Patent”. www.Law360.com. Truy cập ngày 16 tháng 5 năm 2019.
- ^ “Abiraterone acetate - Johnson & Johnson”. Adis Insight.
Liên kết ngoài
[sửa | sửa mã nguồn] GIẢM
50%
GIẢM
50%
 GIẢM
47%
GIẢM
47%
 GIẢM
26%
GIẢM
26%
![[Review Sách] 7 Định luật giảng dạy](https://down-bs-vn.img.susercontent.com/vn-11134207-7qukw-lidxs3ynamto6c.webp) GIẢM
12%
GIẢM
12%
 GIẢM
32%
GIẢM
32%
 GIẢM
22%
GIẢM
22%

![[Các tộc bài] Runick: Tiếng sấm truyền từ xứ sở Bắc Âu](https://ygoguidance.com/wp-content/uploads/2022/12/300589465_3270901226520339_9095435439554912729_n.jpg)

