Prasterone
 | |
 | |
| Dữ liệu lâm sàng | |
|---|---|
| Tên thương mại | Astenile, Cetovister, 17-Chetovis, Dastonil S, Deandros, Diandrone, Fidelin™, Hormobago, 17-Hormoforin, Intrarosa, 17-Ketovis, Mentalormon, Psicosterone[1] |
| Đồng nghĩa | EL-10; GL-701; KYH-3102; Androst-5-en-3β-ol-17-one; 3β-Hydroxyandrost-5-en-17-one; 5,6-Didehydroepiandrosterone;[2] Dehydroisoepiandrosterone[1] |
| Dược đồ sử dụng | By mouth, vaginal (insert), intramuscular injection (as prasterone enanthate), injection (as prasterone sodium sulfat) |
| Mã ATC | |
| Tình trạng pháp lý | |
| Tình trạng pháp lý |
|
| Dữ liệu dược động học | |
| Sinh khả dụng | 50%[3] |
| Chuyển hóa dược phẩm | Gan[3] |
| Chất chuyển hóa | • Androsterone[3] • Etiocholanolone[3] • DHEA sulfat[3] • Androstenedione[3] • Androstenediol[3] • Testosterone[3] • Dihydrotestosterone • Androstanediol[3] • Estrone • Estradiol |
| Chu kỳ bán rã sinh học | DHEA: 25 minutes[4] DHEA-S: 11 hours[4] |
| Bài tiết | Urine |
| Các định danh | |
Tên IUPAC
| |
| Số đăng ký CAS | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| Định danh thành phần duy nhất | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| Dữ liệu hóa lý | |
| Công thức hóa học | C19H28O2 |
| Khối lượng phân tử | 288.424 g/mol |
| Mẫu 3D (Jmol) | |
| Điểm nóng chảy | 148,5 °C (299,3 °F) |
SMILES
| |
Định danh hóa học quốc tế
| |
| (kiểm chứng) | |
Prasterone, còn được gọi là dehydroepiandrosterone (DHEA) và được bán dưới tên thương hiệu Intrarosa và Gynodian Depot số những người khác, là một loại thuốc cũng như thực phẩm bổ sung không kê đơn được sử dụng để điều chỉnh sự thiếu hụt DHEA do suy thượng thận hoặc tuổi già, là một thành phần của liệu pháp hormon mãn kinh, để điều trị quan hệ tình dục đau đớn do teo âm đạo và chuẩn bị cổ tử cung để sinh con, trong số các ứng dụng khác.[3][5] Nó được uống bằng miệng, bằng cách bôi lên da, qua âm đạo hoặc tiêm bắp.[5]
Tác dụng phụ của prasterone ở phụ nữ bao gồm các triệu chứng nam tính như da dầu, mụn trứng cá, tăng trưởng tóc, thay đổi giọng nói và tăng ham muốn tình dục, đau đầu, mất ngủ và những người khác.[3][5] Hợp chất này là một prohormone tự nhiên của androgen và estrogen và do đó là chất chủ vận của thụ thể androgen và estrogen, các mục tiêu sinh học tương ứng của androgen như testosterone và estrogen như estradiol.[3][6] Prasterone cũng có nhiều hoạt động riêng, bao gồm neurosteroid và các hoạt động khác.[6]
Prasterone được phát hiện vào năm 1934.[3][5] Một mối liên quan giữa mức độ DHEA và sự lão hóa đã được báo cáo lần đầu tiên vào năm 1965.[3][5] Các hợp chất bắt đầu được sử dụng như một loại thuốc vào cuối những năm 1970 và như là một bổ sung vào đầu những năm 1980.[3][5] Việc tiếp thị prasterone không cần kê đơn như một chất bổ sung được cho phép ở Hoa Kỳ nhưng bị cấm ở nhiều quốc gia khác.[3]
Sử dụng trong y tế
[sửa | sửa mã nguồn]Thiếu hụt
[sửa | sửa mã nguồn]DHEA và DHEA sulfat được sản xuất bởi tuyến thượng thận. Ở những người bị suy tuyến thượng thận như bệnh Addison, có thể thiếu hụt DHEA và DHEA sulfate. Ngoài ra, mức độ của các steroid này giảm trong suốt cuộc đời và thấp hơn 70 đến 80% ở người cao tuổi so với mức độ ở người trẻ tuổi. Prasterone có thể được sử dụng để tăng nồng độ sulfate DHEA và DHEA trong suy thượng thận và tuổi già. Mặc dù thiếu hụt các steroid này ở những người như vậy, nhưng lợi ích lâm sàng của việc bổ sung, nếu có, là không chắc chắn, và hiện tại không đủ bằng chứng để hỗ trợ việc sử dụng prasterone cho các mục đích đó.[7][8]
Mãn kinh
[sửa | sửa mã nguồn]Prasterone đôi khi được sử dụng như một androgen trong liệu pháp hormone mãn kinh.[9] Ngoài prasterone chính nó, một tiền chất este lâu dài của prasterone, prasterone enanthate, được sử dụng kết hợp với estradiol valerate để điều trị các triệu chứng mãn kinh dưới tên thương hiệu Gynodian Depot.[10][11][12][13][14][15]
| Tuyến đường | Thuốc | Các hình thức) | Tên thương hiệu chính | Liều dùng |
|---|---|---|---|---|
| Uống | Testosterone không làm mất đi một | Viên con nhộng | Hà Lan | 40 trận80 mg 1x / 1 trận2 ngày |
| Methyltestosterone b | Máy tính bảng | Metandren; Estratest | 0,5 sắt10 mg / ngày | |
| Normethandrone a, b | Máy tính bảng | Ginecoside | 5 mg / ngày | |
| Têrêxa a | Máy tính bảng | Sinh động | 1,25 2,52,5 mg / ngày | |
| Prasterone (<abbr title="<nowiki>dehydroepiandrosterone</nowiki>">DHEA) c | Máy tính bảng | <abbr title="<nowiki>Not applicable</nowiki>">Không có | 25 con100 mg / ngày | |
| Dưới lưỡi | Testosterone d | Máy tính bảng | <abbr title="<nowiki>Not applicable</nowiki>">Không có | 0,25 sắt0,5 mg / ngày |
| Methyltestosterone | Máy tính bảng | Metandren | 0,25 mg / ngày | |
| Xuyên da | Testosterone a | Vá | Xâm nhập | 150 con300 μg / ngày |
| Testosterone | Kem; Gel | AndroGel | năm con10 mg / ngày | |
| Âm đạo | Testosterone d | Kem; Gel | <abbr title="<nowiki>Not applicable</nowiki>">Không có | ? mg 1x / 1 Lần3 ngày |
| Testosterone d | Thuốc đạn | <abbr title="<nowiki>Not applicable</nowiki>">Không có | 1 mg 1x / 2 ngày | |
| Prasterone (<abbr title="<nowiki>dehydroepiandrosterone</nowiki>">DHEA) | Chèn | Intrarosa | 6,5 mg / ngày | |
| Tiêm bắp | Testosterone enanthate b | Dầu | Delatestryl; Kho nguyên thủy | 25 trận 100 mg 1x / 4 trận6 tuần |
| Testosterone cypionate b | Dầu | <abbr title="<nowiki>Depo-Testosterone</nowiki>">Depo-Testost.; Depo-Testadiol | 25 trận 100 mg 1x / 4 trận6 tuần | |
| Testosterone isobutyrate a, b | Nước | Femandren M, Folivirin | 25 trận50 mg 1x / 4 trận6 tuần | |
| Testosterone <abbr title="<nowiki>enanthate benzilic acid hydrazone</nowiki>">EBH b, e | Dầu | Climacteron | 150 mg 1x / 4 tuần8 | |
| Nandrolone decanoate | Dầu | Deca-Durabolin | 25 trận5050 1x / 6 trận12 tuần | |
| Prasterone làm từ thiện a, b | Dầu | Kho Gynodian | 200 mg 1x / 4 tuần6 | |
| Tiêm dưới da | Testosterone | Cấy ghép | Testopel | 50 con100 mg 1x / 3 trận6 tháng |
| Chú thích: a = Không có sẵn hoặc không còn có sẵn ở Hoa Kỳ. b = Một mình và/hoặc kết hợp với estrogen. c = Không kê đơn. d = Chỉ hợp chất. e = Ngưng. Nguồn: Xem mẫu. | ||||
Teo âm đạo
[sửa | sửa mã nguồn]Prasterone, dưới tên thương hiệu Intrarosa, được chấp thuận tại Hoa Kỳ trong một công thức chèn âm đạo để điều trị viêm âm đạo teo.[16][17] Cơ chế hoạt động của prasterone cho chỉ định này vẫn chưa được biết, mặc dù nó có thể liên quan đến sự chuyển hóa cục bộ của prasterone thành androgen và estrogen.[17]
Sinh con
[sửa | sửa mã nguồn]Khi muối natri của prasterone sulfat (tên thương hiệu Astenile, Mylis, Teloin),[18][19] một tiền chất este của prasterone, prasterone được sử dụng trong Nhật Bản như một tiêm để điều trị không đủ chín cổ tử cung và sự giãn nở cổ tử cung trong khi sinh con.[1][20][21][22][23][24][25]
Tác dụng phụ
[sửa | sửa mã nguồn]Prasterone được sản xuất tự nhiên trong cơ thể con người, nhưng tác dụng lâu dài của việc sử dụng nó phần lớn chưa được biết đến.[26][27] Trong ngắn hạn, một số nghiên cứu đã ghi nhận một vài tác dụng phụ. Trong một nghiên cứu của Chang et al., prasterone được dùng với liều 200 mg/ngày trong 24 tuần với hiệu ứng androgen nhẹ ghi nhận.[28] Một nghiên cứu khác sử dụng liều tới 400 mg/ngày trong 8 tuần với một vài sự kiện bất lợi được báo cáo.[29] Một nghiên cứu dài hạn theo dõi bệnh nhân dùng liều 50 mg prasterone cho 12 tháng với số lượng và mức độ nghiêm trọng của tác dụng phụ được báo cáo là nhỏ.[30] Một nghiên cứu khác cung cấp một liều 50 mg prasterone trong 10 tháng không có tác dụng phụ nghiêm trọng được báo cáo.[31]
Là một tiền chất hormone, đã có báo cáo về tác dụng phụ có thể gây ra bởi các chất chuyển hóa hormone của prasterone.[27][32]
Người ta không biết liệu prasterone có an toàn khi sử dụng lâu dài hay không. Một số nhà nghiên cứu tin rằng bổ sung prasterone thực sự có thể làm tăng nguy cơ ung thư vú, ung thư tuyến tiền liệt, bệnh tim, tiểu đường,[27] và đột quỵ. Prasterone có thể kích thích tăng trưởng khối u trong các loại ung thư nhạy cảm với hormone, chẳng hạn như một số loại ung thư vú, tử cung và tuyến tiền liệt.[27] Prasterone có thể làm tăng sưng tuyến tiền liệt ở nam giới bị tăng sản tuyến tiền liệt lành tính (BPH), một tuyến tiền liệt mở rộng.[26]
Prasterone là một hormone steroid. Liều cao có thể gây ra sự hung hăng, khó chịu, khó ngủ và sự phát triển của cơ thể hoặc lông mặt trên phụ nữ.[26] Nó cũng có thể ngăn chặn kinh nguyệt và giảm mức HDL (cholesterol "tốt"), có thể làm tăng nguy cơ mắc bệnh tim.[26] Các tác dụng phụ được báo cáo khác bao gồm mụn trứng cá, các vấn đề về nhịp tim, các vấn đề về gan, rụng tóc (từ da đầu) và da dầu. Nó cũng có thể làm thay đổi lượng đường trong máu của cơ thể.[26]
Prasterone có thể thúc đẩy kháng tamoxifen trong ung thư vú.[26] Nó cũng có thể làm tăng nguy cơ ung thư tử cung và tuyến tiền liệt do chuyển hóa thành estrogen và androgen tương ứng.[33] Bệnh nhân đang điều trị thay thế hormone có thể có nhiều tác dụng phụ liên quan đến estrogen hơn khi dùng prasterone. Bổ sung này cũng có thể can thiệp với các loại thuốc khác, và tương tác tiềm năng giữa nó và thuốc và thảo dược là có thể.[26]
Prasterone có thể không an toàn cho những người trải qua thai kỳ, cho con bú, tình trạng nhạy cảm với hormone, các vấn đề về gan, tiểu đường, trầm cảm hoặc rối loạn tâm trạng, hội chứng buồng trứng đa nang (PCOS) hoặc các vấn đề về cholesterol.[34]
Prasterone đã được báo cáo là có ít hoặc không có tác dụng phụ ngay cả ở liều lượng rất cao (ví dụ: 50 lần liều khuyến cáo không cần kê đơn).[33] Tuy nhiên, nó có thể gây ra nam tính và các tác dụng phụ androgen khác ở phụ nữ và gynecomastia và các tác dụng phụ estrogen khác ở nam giới.[33]
Dược lý
[sửa | sửa mã nguồn]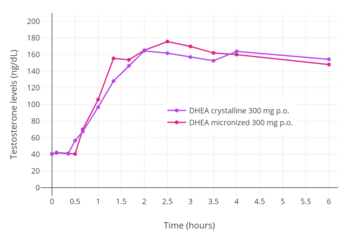

Prasterone được chuyển hóa thành androgen và estrogen trong cơ thể.[6][39] Nó được chuyển thành androstenedione bởi 3β-hydroxapseoid dehydrogenase (3β-HSD) và thành androstenediol bởi 17β-hydroxapseoid dehydrogenase (17β-HSD).[6][39] Sau đó, androstenedione và androstenediol có thể được chuyển đổi thành testosterone tương ứng bằng 17β-HSD và 3β-HSD.[6][39] Sau đó, testosterone có thể được chuyển hóa thành dihydrotestosterone bằng 5α-reductase.[6][39] Ngoài ra, androstenedione và testosterone có thể được chuyển đổi thành estrone và estradiol tương ứng bởi aromatase.[6][39] Prasterone cũng được chuyển hóa thành prasterone sulfat bằng steroid sulfotransferase (cụ thể là SULT1E1 và SULT2A1), do đó có thể được chuyển đổi trở lại thành prasterone bởi steroid sulfatase.[6][40] Sự chuyển đổi prasterone thành androgen và estrogen là đặc hiệu mô, xảy ra ở gan, mỡ, âm đạo, tuyến tiền liệt, da và nang lông, trong số các mô khác.[6][41]
Trong các nghiên cứu lâm sàng về bổ sung prasterone, liều lượng đã dao động từ 20 đến 1.600 mg mỗi ngày.[42] Ở những người bị suy thượng thận, liều uống từ 20 đến 50 mg / ngày prasterone đã được tìm thấy để khôi phục mức độ DHEA và DHEA-S về mức bình thường thấy ở những người trẻ tuổi khỏe mạnh.[42] Ngược lại, liều uống từ 100 đến 200 mg/ngày prasterone đã được tìm thấy dẫn đến mức độ siêu âm của DHEA và DHEA-S.[42] Với liều cao 1.600 mg/ngày uống trong 4 tuần, điều trị cho phụ nữ mãn kinh bằng prasterone đã được tìm thấy làm tăng nồng độ DHEA trong huyết thanh lên gấp 15 lần, testosterone tăng gấp 9 lần, DHEA-S, androstenedione và DHT đều tăng gấp 20 lần, và estrone và estradiol đều tăng gấp 2 lần gập lại.[43][44] Micronization của prasterone đã được tìm thấy để tăng đáng kể mức độ DHEA-S đạt được bằng cách uống nhưng không tạo ra sự thay đổi đáng kể về mức độ DHEA hoặc mức testosterone đạt được.[35]
Mặc dù prasterone có thể làm tăng đáng kể nồng độ testosterone ở phụ nữ, nhưng điều này không giống với trường hợp ở nam giới.[33] Một liều cao 1.600 mg/ngày prasterone ở nam giới cho 4 người tuần đã được tìm thấy để tăng mức độ DHEA và androstenedione nhưng không ảnh hưởng đáng kể đến mức độ testosterone.[33]
Hóa học
[sửa | sửa mã nguồn]Prasterone, còn được gọi là androst-5-en-3β-ol-17-one, là một steroid androstane tự nhiên và 17-ketosteroid. Nó có liên quan chặt chẽ về cấu trúc với androstenediol (androst-5-ene-3β, 17β-diol), androstenedione (androst-4-ene-3,17-dione) và testosterone (androst-4-en-17β-ol-3 -một). Prasterone là δ 5 (5 (6) -dehydrogenated) tương tự của epiandrosterone (5α-androstan-3β-ol-17-one), và còn được gọi là 5-dehydroepiandrosterone (DHEA 5) hoặc δ5-epiandrosterone. Một đồng phân vị trí của prasterone có thể có hoạt tính sinh học tương tự là 4-dehydroepiandrosterone (4-DHEA).[45]
Các dẫn xuất
[sửa | sửa mã nguồn]Prasterone được sử dụng về mặt y tế như este C3β prasterone enanthate và prasterone sulfat.[1] Chất tương tự demethyl C19 của prasterone là 19-nordehydroepiandrosterone (19-nor-DHEA), là một prohormone của nandrolone (19-nortestosterone).[46][47] Các 5α-giảm và δ1 (1 (2) - dehydrogenated) tương tự của prasterone là 1-dehydroepiandrosterone (DHEA 1 hoặc 1-androsterone), mà là một prohormone của 1-testosterone (δ1 -DHT hoặc dihydroboldenone).[48] Fluasterone (3β-dehydroxy-16α-fluoro-DHEA) là một dẫn xuất của prasterone với hoạt động tối thiểu hoặc không có nội tiết tố nhưng các hoạt động sinh học khác được bảo tồn.[43]
Lịch sử
[sửa | sửa mã nguồn]DHEA đã được phát hiện, thông qua phân lập từ nước tiểu nam, bởi Adolf Butenandt và Hans Dannenbaum vào năm 1934, và hợp chất được phân lập từ huyết tương người bởi Migeon và Plager vào năm 1954.[3][5] DHEA sulfate, este 3β- sulfat của DHEA, được phân lập từ nước tiểu vào năm 1944, và được Baulieu tìm thấy là hoocmon steroid dồi dào nhất trong huyết tương người năm 1954.[3][5] Từ khi được phát hiện vào năm 1934 cho đến năm 1959, DHEA đã được nhắc đến bởi một số tên khác nhau trong tài liệu, bao gồm dehydroandrosterone, transdehydroandrosterone, dehydroisoandrosterone và androstenolone.[5] Tên dehydroepiandrosterone, còn được gọi là DHEA, lần đầu tiên được Fieser đề xuất vào năm 1949, và sau đó trở thành tên được sử dụng phổ biến nhất của hormone.[5] Trong nhiều thập kỷ sau khi phát hiện ra, DHEA được coi là một hợp chất không hoạt động, chủ yếu phục vụ như một chất trung gian trong sản xuất androgen và estrogen từ cholesterol.[5] Năm 1965, một mối liên quan giữa mức độ sulfate DHEA và lão hóa đã được báo cáo bởi De Nee và Vermeulen.[3][5] Sau đó, DHEA đã trở thành mối quan tâm của cộng đồng khoa học và nhiều nghiên cứu đánh giá mối quan hệ giữa mức độ sulfate của DHEA và DHEA đã được tiến hành.[3][5]
Prasterone, INN được đề xuất và khuyến nghị INN của DHEA và thuật ngữ được sử dụng khi đề cập đến hợp chất này như một loại thuốc, được công bố lần lượt vào năm 1970 và 1978.[49][50] Sự kết hợp của 4 mg estradiol valates và 200 mg prasterone enanthate trong dung dịch dầu được giới thiệu để sử dụng trong liệu pháp hormon mãn kinh bằng cách tiêm intramusuclar dưới tên thương hiệu Gynodian Depot ở châu Âu vào năm 1978.[51][52][53][54] Vào đầu những năm 1980, prasterone trở thành có sẵn và được bán rộng rãi over-the-counter như một bổ sung không cần toa bác sĩ trong nước Mỹ, chủ yếu là giảm cân viện trợ.[3][5][55] Nó được mô tả như là một "loại thuốc thần kỳ", với các lợi ích chống lão hóa, chống béo phì và chống ung thư.[3] Điều này tiếp tục cho đến năm 1985, khi việc tiếp thị prasterone bị Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) cấm do thiếu bằng chứng về lợi ích sức khỏe và do sự an toàn và rủi ro lâu dài của hợp chất chưa được biết đến vào thời điểm đó.[3][5][55] Sau đó, prasterone một lần nữa trở nên có sẵn không cần kê đơn như một chất bổ sung chế độ ăn uống ở Hoa Kỳ sau khi thông qua Đạo luật Giáo dục và Sức khỏe Bổ sung Chế độ Ăn uống năm 1994.[3] Ngược lại, nó vẫn bị cấm như là một bổ sung ở Canada, Vương quốc Anh, Úc và New Zealand.[3][56]
Năm 2001, Genelabs đã nộp Đơn đăng ký thuốc mới của prasterone để điều trị bệnh lupus ban đỏ hệ thống (SLE) cho FDA.[3][57] Nó có các nhãn hiệu dự kiến Anastar, Aslera và Prestara.[3][57][58] Tuy nhiên, ứng dụng này đã không được chấp thuận và trong khi việc phát triển prasterone cho SLE ở cả Hoa Kỳ và Châu Âu tiếp tục cho đến năm 2010, thuốc cuối cùng không bao giờ được chấp thuận để điều trị tình trạng này.[3] Năm 2016, FDA đã phê duyệt prasterone trong một công thức gel nội nhãn để điều trị quan hệ tình dục đau đớn do teo âm hộ ở Hoa Kỳ dưới tên thương hiệu Intrarosa.[59][60] Đây là loại thuốc có chứa prasterone đầu tiên được FDA chấp thuận tại quốc gia này.[59]
Xã hội và văn hoá
[sửa | sửa mã nguồn]Tên gốc
[sửa | sửa mã nguồn]Prasterone là tên chung của DHEA trong tiếng Anh và tiếng Ý và INN, USAN và DCIT,[1][61][62][63] trong khi tên chung của nó là prasteronum trong tiếng Latin, prastérone trong tiếng Pháp và DCF của nó, và prasteron bằng tiếng Đức.[62]
Tiếp thị
[sửa | sửa mã nguồn]Tại Hoa Kỳ, prasterone hoặc prasterone sulfate đã được quảng cáo, dưới tên DHEA và DHEA-S, với tuyên bố rằng chúng có thể có lợi cho nhiều loại bệnh. Prasterone và prasterone sulfate có sẵn ở Hoa Kỳ, nơi chúng được bán dưới dạng thực phẩm bổ sung không cần kê đơn.[64]
Quy định
[sửa | sửa mã nguồn]Hoa Kỳ
[sửa | sửa mã nguồn]Prasterone là hợp pháp để bán ở Hoa Kỳ như là một bổ sung chế độ ăn uống. Nó hiện đang grandfathered nhập như một "Old ăn Ingredient" đang có bán trước năm 1994. Prasterone đặc biệt được miễn trừ khỏi Đạo luật kiểm soát steroid đồng hóa năm 1990 và 2004.[65] Nó bị cấm sử dụng trong thi đấu thể thao.
Nghiên cứu
[sửa | sửa mã nguồn]Sử dụng đồng hóa
[sửa | sửa mã nguồn]Một phân tích tổng hợp các nghiên cứu can thiệp cho thấy bổ sung prasterone ở người cao tuổi có thể tạo ra một tác động tích cực nhỏ nhưng có ý nghĩa đối với thành phần cơ thể phụ thuộc hoàn toàn vào chuyển đổi prasterone thành các chất chuyển hóa có hoạt tính sinh học như androgen hoặc estrogen.[66] Bằng chứng là không thuyết phục liên quan đến tác dụng của prasterone đối với sức mạnh ở người cao tuổi.[67] Ở những người đàn ông trung niên, không có tác dụng đáng kể nào của việc bổ sung prasterone lên khối lượng cơ thể, sức mạnh hoặc nồng độ testosterone được tìm thấy trong một thử nghiệm ngẫu nhiên có đối chứng giả dược.[68]
Xem thêm
[sửa | sửa mã nguồn]Tham khảo
[sửa | sửa mã nguồn]- ^ a b c d e J. Elks (ngày 14 tháng 11 năm 2014). The Dictionary of Drugs: Chemical Data: Chemical Data, Structures and Bibliographies. Springer. tr. 641–. ISBN 978-1-4757-2085-3.
- ^ James Devillers (ngày 27 tháng 4 năm 2009). Endocrine Disruption Modeling. CRC Press. tr. 339–. ISBN 978-1-4200-7636-3.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab Melanie Johns Cupp; Timothy S. Tracy (ngày 10 tháng 12 năm 2002). Dietary Supplements: Toxicology and Clinical Pharmacology. Springer Science & Business Media. tr. 123–147. ISBN 978-1-59259-303-3.
- ^ a b B.J. Oddens; A. Vermeulen (ngày 15 tháng 11 năm 1996). Androgens and the Aging Male. CRC Press. tr. 5–. ISBN 978-1-85070-763-9.
- ^ a b c d e f g h i j k l m n o Rutkowski K, Sowa P, Rutkowska-Talipska J, Kuryliszyn-Moskal A, Rutkowski R (tháng 7 năm 2014). “Dehydroepiandrosterone (DHEA): hypes and hopes”. Drugs. 74 (11): 1195–207. doi:10.1007/s40265-014-0259-8. PMID 25022952.
- ^ a b c d e f g h i Prough RA, Clark BJ, Klinge CM (tháng 4 năm 2016). “Novel mechanisms for DHEA action”. J. Mol. Endocrinol. 56 (3): R139–55. doi:10.1530/JME-16-0013. PMID 26908835.
- ^ Arlt, W (tháng 9 năm 2004). “Dehydroepiandrosterone and ageing”. Best Practice & Research. Clinical Endocrinology & Metabolism. 18 (3): 363–80. doi:10.1016/j.beem.2004.02.006. PMID 15261843.
- ^ Alkatib, AA; Cosma, M; Elamin, MB; Erickson, D; Swiglo, BA; Erwin, PJ; Montori, VM (tháng 10 năm 2009). “A systematic review and meta-analysis of randomized placebo-controlled trials of DHEA treatment effects on quality of life in women with adrenal insufficiency”. The Journal of Clinical Endocrinology and Metabolism. 94 (10): 3676–81. doi:10.1210/jc.2009-0672. PMID 19773400.
- ^ Rogerio A. Lobo (ngày 5 tháng 6 năm 2007). Treatment of the Postmenopausal Woman: Basic and Clinical Aspects. Academic Press. tr. 821–828. ISBN 978-0-08-055309-2.
- ^ https://www.drugs.com/international/gynodian-depot.html
- ^ J. Horsky; J. Presl (ngày 6 tháng 12 năm 2012). Ovarian Function and its Disorders: Diagnosis and Therapy. Springer Science & Business Media. tr. 146–. ISBN 978-94-009-8195-9.
- ^ D. Platt (ngày 6 tháng 12 năm 2012). Geriatrics 3: Gynecology · Orthopaedics · Anesthesiology · Surgery · Otorhinolaryngology · Ophthalmology · Dermatology. Springer Science & Business Media. tr. 6–. ISBN 978-3-642-68976-5.
- ^ S. Campbell (ngày 6 tháng 12 năm 2012). The Management of the Menopause & Post-Menopausal Years: The Proceedings of the International Symposium held in London 24–ngày 26 tháng 11 năm 1975 Arranged by the Institute of Obstetrics and Gynaecology, The University of London. Springer Science & Business Media. tr. 395–. ISBN 978-94-011-6165-7.
- ^ Carrie Bagatell; William J. Bremner (ngày 27 tháng 5 năm 2003). Androgens in Health and Disease. Springer Science & Business Media. tr. 277–. ISBN 978-1-59259-388-0.
- ^ Frigo P, Eppel W, Asseryanis E, Sator M, Golaszewski T, Gruber D, Lang C, Huber J (1995). “The effects of hormone substitution in depot form on the uterus in a group of 50 perimenopausal women--a vaginosonographic study”. Maturitas. 21 (3): 221–5. doi:10.1016/0378-5122(94)00893-c. PMID 7616871.
- ^ http://adisinsight.springer.com/drugs/800032054
- ^ a b https://www.accessdata.fda.gov/drugsatfda_docs/label/2016/208470s000lbl.pdf
- ^ https://www.drugs.com/international/mylis.html
- ^ “Prasterone vaginal - Kanebo - AdisInsight”.
- ^ John W. Blunt; Murray H. G. Munro (ngày 19 tháng 9 năm 2007). Dictionary of Marine Natural Products with CD-ROM. CRC Press. tr. 1075–. ISBN 978-0-8493-8217-8.
- ^ A. Kleemann; J. Engel; B. Kutscher; D. Reichert (ngày 14 tháng 5 năm 2014). Pharmaceutical Substances, 5th Edition, 2009: Syntheses, Patents and Applications of the most relevant APIs. Thieme. tr. 2441–2442. ISBN 978-3-13-179525-0.
- ^ Martin Negwer; Hans-Georg Scharnow (2001). Organic-chemical drugs and their synonyms: (an international survey). Wiley-VCH. tr. 1831. ISBN 978-3-527-30247-5.
3β-Hydroxyandrost-5-en-17-one hydrogen sulfate = (3β)-3-(Sulfooxy)androst-5-en-17-one. R: Sodium salt (1099-87-2). S: Astenile, Dehydroepiandrosterone sulfate sodium, DHA-S, DHEAS, KYH 3102, Mylis, PB 005, Prasterone sodium sulfate, Teloin
- ^ Jianqiu, Y (1992). “Clinical Application of Prasterone Sodium Sulfate”. Chinese Journal of New Drugs. 5: 015.
- ^ Sakaguchi M, Sakai T, Adachi Y, Kawashima T, Awata N (1992). “The biological fate of sodium prasterone sulfate after vaginal administration. I. Absorption and excretion in rats”. J. Pharmacobio-dyn. 15 (2): 67–73. doi:10.1248/bpb1978.15.67. PMID 1403604.
- ^ Sakai, T.; Sakaguchi, M.; Adachi, Y.; Kawashima, T.; Awata, N. (1992). “The Biological Fate of Sodium Prasterone Sulfate after Vaginal Administration II: Distribution after Single and Multiple Administration to Pregnant Rats”. 薬物動態. 7 (1): 87–101. doi:10.2133/dmpk.7.87.
- ^ a b c d e f g Ades TB biên tập (2009). DHEA. American Cancer Society Complete Guide to Complementary and Alternative Cancer Therapies (ấn bản thứ 2). American Cancer Society. tr. 729–33. ISBN 9780944235713.
- ^ a b c d Medscape (2010). “DHEA Oral”. Drug Reference. WebMD LLC. Truy cập ngày 18 tháng 2 năm 2010.
- ^ Chang DM, Lan JL, Lin HY, Luo SF (2002). “Dehydroepiandrosterone treatment of women with mild-to-moderate systemic lupus erythematosus: a multicenter randomized, double-blind, placebo-controlled trial”. Arthritis Rheum. 46 (11): 2924–27. doi:10.1002/art.10615. PMID 12428233.
- ^ Rabkin JG, McElhiney MC, Rabkin R, McGrath PJ, Ferrando SJ (2006). “Placebo-controlled trial of dehydroepiandrosterone (DHEA) for treatment of nonmajor depression in patients with HIV/AIDS”. Am J Psychiatry. 163 (1): 59–66. doi:10.1176/appi.ajp.163.1.59. PMID 16390890.
- ^ Brooke AM, Kalingag LA, Miraki-Moud F, Camacho-Hübner C, Maher KT, Walker DM, Hinson JP, Monson JP (2006). “Dehydroepiandrosterone improves psychological well-being in male and female hypopituitary patients on maintenance growth hormone replacement”. J Clin Endocrinol Metab. 91 (10): 3773–79. doi:10.1210/jc.2006-0316. PMID 16849414.
- ^ Villareal DT, Holloszy JO (2006). “DHEA enhances effects of weight training on muscle mass and strength in elderly women and men”. Am J Physiol Endocrinol Metab. 291 (5): E1003–08. doi:10.1152/ajpendo.00100.2006. PMID 16787962.
- ^ Medline Plus. “DHEA”. Drugs and Supplements Information. National Library of Medicine. Truy cập ngày 18 tháng 2 năm 2010.
- ^ a b c d e Douglas McKeag; James L. Moeller (2007). ACSM's Primary Care Sports Medicine. Lippincott Williams & Wilkins. tr. 616–. ISBN 978-0-7817-7028-6.
- ^ “DHEA: Side effects and safety”. WebMD. Truy cập ngày 24 tháng 7 năm 2012.
- ^ a b Casson PR, Straughn AB, Umstot ES, Abraham GE, Carson SA, Buster JE (tháng 2 năm 1996). “Delivery of dehydroepiandrosterone to premenopausal women: effects of micronization and nonoral administration”. Am. J. Obstet. Gynecol. 174 (2): 649–53. doi:10.1016/S0002-9378(96)70444-1. PMID 8623801.
- ^ Kuhl, Herbert; Taubert, Hans-Dieter (1987). Das Klimakterium – Pathophysiologie, Klinik, Therapie [The Climacteric – Pathophysiology, Clinic, Therapy] (bằng tiếng Đức). Stuttgart, Germany: Thieme Verlag. tr. 122. ISBN 978-3137008019.
- ^ Düsterberg B, Wendt H (1983). “Plasma levels of dehydroepiandrosterone and 17 beta-estradiol after intramuscular administration of Gynodian-Depot in 3 women”. Horm. Res. 17 (2): 84–9. doi:10.1159/000179680. PMID 6220949.
- ^ Rauramo L, Punnonen R, Kaihola LH, Grönroos M (tháng 1 năm 1980). “Serum oestrone, oestradiol and oestriol concentrations in castrated women during intramuscular oestradiol valerate and oestradiolbenzoate-oestradiolphenylpropionate therapy”. Maturitas. 2 (1): 53–8. doi:10.1016/0378-5122(80)90060-2. PMID 7402086.
- ^ a b c d e Carl A. Burtis; Edward R. Ashwood; David E. Bruns (ngày 14 tháng 10 năm 2012). Tietz Textbook of Clinical Chemistry and Molecular Diagnostics - E-Book. Elsevier Health Sciences. tr. 1856–. ISBN 978-1-4557-5942-2.
- ^ Mueller JW, Gilligan LC, Idkowiak J, Arlt W, Foster PA (2015). “The Regulation of Steroid Action by Sulfation and Desulfation”. Endocr. Rev. 36 (5): 526–63. doi:10.1210/er.2015-1036. PMC 4591525. PMID 26213785.
- ^ Labrie F, Martel C, Bélanger A, Pelletier G (tháng 4 năm 2017). “Androgens in women are essentially made from DHEA in each peripheral tissue according to intracrinology”. J. Steroid Biochem. Mol. Biol. 168: 9–18. doi:10.1016/j.jsbmb.2016.12.007. PMID 28153489.
- ^ a b c Paul M. Coates; M. Coates Paul; Marc Blackman; Marc R. Blackman, Gordon M. Cragg, Mark Levine, Jeffrey D. White, Joel Moss, Mark A. Levine (ngày 29 tháng 12 năm 2004). Encyclopedia of Dietary Supplements (Print). CRC Press. tr. 169–. ISBN 978-0-8247-5504-1.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- ^ a b Schwartz AG, Pashko LL (2004). “Dehydroepiandrosterone, glucose-6-phosphate dehydrogenase, and longevity”. Ageing Res. Rev. 3 (2): 171–87. doi:10.1016/j.arr.2003.05.001. PMID 15177053.
- ^ Mortola JF, Yen SS (1990). “The effects of oral dehydroepiandrosterone on endocrine-metabolic parameters in postmenopausal women”. J. Clin. Endocrinol. Metab. 71 (3): 696–704. doi:10.1210/jcem-71-3-696. PMID 2144295.
- ^ Edith Josephy; F. Radt (ngày 1 tháng 12 năm 2013). Elsevier's Encyclopaedia of Organic Chemistry: Series III: Carboisocyclic Condensed Compounds. Springer. tr. 2608–. ISBN 978-3-662-25863-7.
- ^ NSCA-National Strength & Conditioning Association (ngày 27 tháng 1 năm 2017). NSCA'S Essentials of Tactical Strength and Conditioning. Human Kinetics. tr. 130–. ISBN 978-1-4504-5730-9.
- ^ Detlef Thieme; Peter Hemmersbach (ngày 18 tháng 12 năm 2009). Doping in Sports. Springer Science & Business Media. tr. 137–. ISBN 978-3-540-79088-4.
- ^ Parr MK, Opfermann G, Geyer H, Westphal F, Sönnichsen FD, Zapp J, Kwiatkowska D, Schänzer W (2011). “Seized designer supplement named "1-Androsterone": identification as 3β-hydroxy-5α-androst-1-en-17-one and its urinary elimination”. Steroids. 76 (6): 540–7. doi:10.1016/j.steroids.2011.02.001. PMID 21310167.
- ^ “Bản sao đã lưu trữ” (PDF). Bản gốc (PDF) lưu trữ ngày 4 tháng 3 năm 2016. Truy cập ngày 29 tháng 6 năm 2019.
- ^ “Bản sao đã lưu trữ” (PDF). Bản gốc (PDF) lưu trữ ngày 4 tháng 3 năm 2016. Truy cập ngày 29 tháng 6 năm 2019.
- ^ Hoyme U, Baumueller A, Madsen PO (1978). “The influence of pH on antimicrobial substances in canine vaginal and urethral secretions”. Urol. Res. 6 (1): 35–42. PMID 25506.
- ^ Kopera, H.; Dhont, M.; Dienstl, F.; Gambrell, R. D.; Gordan, G. S.; Heidenreich, J.; Lachnit-Fixon, U.; Lauritzen, C.; Lebech, P. E. (1979). “Effects, side-effects, and dosage schemes of various sex hormones in the peri- and post-menopause”. Female and Male Climacteric. tr. 43–67. doi:10.1007/978-94-011-9720-5_6. ISBN 978-94-011-9722-9.
- ^ Mattson LA, Cullberg G, Tangkeo P, Zador G, Samsioe G (tháng 12 năm 1980). “Administration of dehydroepiandrosterone enanthate to oophorectomized women--effects on sex hormones and lipid metabolism”. Maturitas. 2 (4): 301–9. doi:10.1016/0378-5122(80)90032-8. PMID 6453267.
- ^ Muller (ngày 19 tháng 6 năm 1998). European Drug Index: European Drug Registrations, Fourth Edition. CRC Press. tr. 566–. ISBN 978-3-7692-2114-5.
- ^ a b C.W. Randolph, Jr., M.D.; Genie James (ngày 1 tháng 1 năm 2010). From Hormone Hell to Hormone Well: Straight Talk Women (and Men) Need to Know to Save Their Sanity, Health, and—Quite Possibly—Their Lives. Health Communications, Incorporated. tr. 72–. ISBN 978-0-7573-9759-2.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- ^ Marie Dunford; J. Andrew Doyle (ngày 7 tháng 2 năm 2014). Nutrition for Sport and Exercise. Cengage Learning. tr. 442–. ISBN 978-1-285-75249-5.
- ^ a b “Prasterone - Genelabs - AdisInsight”.
- ^ Sheldon Blau; Dodi Schultz (ngày 5 tháng 3 năm 2009). Living With Lupus: The Complete Guide, 2nd Edition. Da Capo Press. tr. 138–. ISBN 978-0-7867-2985-2.
- ^ a b Voelker, Rebecca (2017). “Relief for Painful Intercourse”. JAMA. 317 (1): 18. doi:10.1001/jama.2016.19077. ISSN 0098-7484. PMID 28030684.
- ^ “Prasterone (Intrarosa) for Dyspareunia”. JAMA. 318 (16): 1607. 2017. doi:10.1001/jama.2017.14981. ISSN 0098-7484.
- ^ I.K. Morton; Judith M. Hall (ngày 6 tháng 12 năm 2012). Concise Dictionary of Pharmacological Agents: Properties and Synonyms. Springer Science & Business Media. tr. 92, 96, 230. ISBN 978-94-011-4439-1.
- ^ a b “Prasterone”.
- ^ “Drug Information Portal - U.S. National Library of Medicine - Quick Access to Quality Drug Information”.
- ^ Calfee, R.; Fadale, P. (tháng 3 năm 2006). “Popular ergogenic drugs and supplements in young athletes”. Pediatrics. 117 (3): e577–89. doi:10.1542/peds.2005-1429. PMID 16510635.
In 2004, a new Steroid Control Act that placed androstenedione under Schedule III of controlled substances effective January 2005 was signed. DHEA was not included in this act and remains an over-the-counter nutritional supplement.
- ^ “Drug Scheduling Actions – 2005”. Drug Enforcement Administration. Bản gốc lưu trữ ngày 16 tháng 2 năm 2012. Truy cập ngày 29 tháng 6 năm 2019.
- ^ Corona, G; Rastrelli, G; Giagulli, VA; Sila, A; Sforza, A; Forti, G; Mannucci, E; Maggi, M (2013). “Dehydroepiandrosterone supplementation in elderly men: a meta-analysis study of placebo-controlled trials”. J. Clin. Endocrinol. Metab. 98 (9): 3615–26. doi:10.1210/jc.2013-1358. PMID 23824417.
- ^ Baker, WL; Karan, S; Kenny, AM (tháng 6 năm 2011). “Effect of dehydroepiandrosterone on muscle strength and physical function in older adults: a systematic review”. Journal of the American Geriatrics Society. 59 (6): 997–1002. doi:10.1111/j.1532-5415.2011.03410.x. PMID 21649617.
- ^ Wallace, M. B.; Lim, J.; Cutler, A.; Bucci, L. (1999). “Effects of dehydroepiandrosterone vs androstenedione supplementation in men”. Medicine and Science in Sports and Exercise. 31 (12): 1788–92. doi:10.1097/00005768-199912000-00014. PMID 10613429.
Đọc thêm
[sửa | sửa mã nguồn]- Keppel Hesselink JM (tháng 12 năm 1997). “[Prasterone (dihydroepiandrosterone): a modern source of eternal youth?]”. Ned Tijdschr Geneeskd (bằng tiếng Hà Lan và Flemish). 141 (51): 2484–7. PMID 9555138.Quản lý CS1: ngôn ngữ không rõ (liên kết)
- Zelissen PM, Thijssen JH (tháng 10 năm 2001). “[Role of prasterone (dehydroepiandrosterone) in substitution therapy for adrenocortical insufficiency]”. Ned Tijdschr Geneeskd (bằng tiếng Hà Lan và Flemish). 145 (42): 2018–22. PMID 11695098.Quản lý CS1: ngôn ngữ không rõ (liên kết)
- Pope, JE; Cupp, MJ; Tracy, TS (2003). Dehydroepiandrosterone (DHEA) (Prasterone). Dietary Supplements. Totowa, NJ: Humana Press. tr. 123–147. doi:10.1007/978-1-59259-303-3_8 (không hoạt động ngày 20 tháng 2 năm 2019). ISBN 9781592593033.Quản lý CS1: DOI không hoạt động tính đến 2019 (liên kết)
- Kocis P (tháng 11 năm 2006). “Prasterone”. Am J Health Syst Pharm. 63 (22): 2201–10. doi:10.2146/ajhp060100. PMID 17090740.
- Mendivil Dacal JM, Borges VM (tháng 4 năm 2009). “[Dehydroepiandrosterone (DHEA), review of its efficiency in the managing of the libido decrease and other symptoms of aging]”. Actas Urol Esp (bằng tiếng Tây Ban Nha). 33 (4): 390–401. doi:10.4321/s0210-48062009000400009. PMID 19579890.
- Alkatib AA, Cosma M, Elamin MB, Erickson D, Swiglo BA, Erwin PJ, Montori VM (tháng 10 năm 2009). “A systematic review and meta-analysis of randomized placebo-controlled trials of DHEA treatment effects on quality of life in women with adrenal insufficiency”. J. Clin. Endocrinol. Metab. 94 (10): 3676–81. doi:10.1210/jc.2009-0672. PMID 19773400.
- Panjari M, Davis SR (tháng 6 năm 2010). “DHEA for postmenopausal women: a review of the evidence”. Maturitas. 66 (2): 172–9. doi:10.1016/j.maturitas.2009.12.017. PMID 20089375.
- Oberbeck R, Kobbe P (2010). “Dehydroepiandrosterone (DHEA): a steroid with multiple effects. Is there any possible option in the treatment of critical illness?”. Curr. Med. Chem. 17 (11): 1039–47. doi:10.2174/092986710790820570. PMID 20156161.
- Prati A, Santagni S, Rattighieri E, Campedelli A, Ricchieri F, Chierchia E, Despini G, Genazzani AR, Genazzani AD (tháng 6 năm 2014). “[The putative role and use of DHEA and its association with the hormone replacement therapy]”. Minerva Ginecol (bằng tiếng Ý). 66 (3): 313–24. PMID 24971788.
- Genazzani AR, Pluchino N (tháng 8 năm 2010). “DHEA therapy in postmenopausal women: the need to move forward beyond the lack of evidence”. Climacteric. 13 (4): 314–6. doi:10.3109/13697137.2010.492496. PMID 20540592.
- Luci M, Valenti G, Maggio M (tháng 9 năm 2010). “[Dehydroepiandrosterone [DHEA(S)]: anabolic hormone?]”. Recenti Prog Med (bằng tiếng Ý). 101 (9): 333–44. PMID 21268370.
- Gleicher N, Barad DH (tháng 5 năm 2011). “Dehydroepiandrosterone (DHEA) supplementation in diminished ovarian reserve (DOR)”. Reprod. Biol. Endocrinol. 9: 67. doi:10.1186/1477-7827-9-67. PMC 3112409. PMID 21586137.
- Davis SR, Panjari M, Stanczyk FZ (tháng 6 năm 2011). “Clinical review: DHEA replacement for postmenopausal women”. J. Clin. Endocrinol. Metab. 96 (6): 1642–53. doi:10.1210/jc.2010-2888. PMID 21411558.
- Panjari M, Davis SR (tháng 9 năm 2011). “Vaginal DHEA to treat menopause related atrophy: a review of the evidence”. Maturitas. 70 (1): 22–5. doi:10.1016/j.maturitas.2011.06.005. PMID 21733647.
- Traish AM, Kang HP, Saad F, Guay AT (tháng 11 năm 2011). “Dehydroepiandrosterone (DHEA)--a precursor steroid or an active hormone in human physiology”. J Sex Med. 8 (11): 2960–82, quiz 2983. doi:10.1111/j.1743-6109.2011.02523.x. PMID 22032408.
- Savineau JP, Marthan R, Dumas de la Roque E (tháng 3 năm 2013). “Role of DHEA in cardiovascular diseases”. Biochem. Pharmacol. 85 (6): 718–26. doi:10.1016/j.bcp.2012.12.004. PMID 23270992.
- Labrie F, Labrie C (tháng 4 năm 2013). “DHEA and intracrinology at menopause, a positive choice for evolution of the human species”. Climacteric. 16 (2): 205–13. doi:10.3109/13697137.2012.733983. PMID 23126249.
- Rutkowski K, Sowa P, Rutkowska-Talipska J, Kuryliszyn-Moskal A, Rutkowski R (tháng 7 năm 2014). “Dehydroepiandrosterone (DHEA): hypes and hopes”. Drugs. 74 (11): 1195–207. doi:10.1007/s40265-014-0259-8. PMID 25022952.
- Peixoto C, Devicari Cheda JN, Nardi AE, Veras AB, Cardoso A (2014). “The effects of dehydroepiandrosterone (DHEA) in the treatment of depression and depressive symptoms in other psychiatric and medical illnesses: a systematic review”. Curr Drug Targets. 15 (9): 901–14. doi:10.2174/1389450115666140717111116. PMID 25039497.
- Elraiyah T, Sonbol MB, Wang Z, Khairalseed T, Asi N, Undavalli C, Nabhan M, Altayar O, Prokop L, Montori VM, Murad MH (tháng 10 năm 2014). “Clinical review: The benefits and harms of systemic dehydroepiandrosterone (DHEA) in postmenopausal women with normal adrenal function: a systematic review and meta-analysis”. J. Clin. Endocrinol. Metab. 99 (10): 3536–42. doi:10.1210/jc.2014-2261. PMC 5393492. PMID 25279571.
- Maggio M, De Vita F, Fisichella A, Colizzi E, Provenzano S, Lauretani F, Luci M, Ceresini G, Dall'Aglio E, Caffarra P, Valenti G, Ceda GP (tháng 1 năm 2015). “DHEA and cognitive function in the elderly”. J. Steroid Biochem. Mol. Biol. 145: 281–92. doi:10.1016/j.jsbmb.2014.03.014. PMID 24794824.
- Pluchino N, Drakopoulos P, Bianchi-Demicheli F, Wenger JM, Petignat P, Genazzani AR (tháng 1 năm 2015). “Neurobiology of DHEA and effects on sexuality, mood and cognition”. J. Steroid Biochem. Mol. Biol. 145: 273–80. doi:10.1016/j.jsbmb.2014.04.012. PMID 24892797.
- Warner M, Gustafsson JA (tháng 1 năm 2015). “DHEA - a precursor of ERβ ligands”. J. Steroid Biochem. Mol. Biol. 145: 245–7. doi:10.1016/j.jsbmb.2014.08.003. PMID 25125389.
- Lang K, Burger-Stritt S, Hahner S (tháng 1 năm 2015). “Is DHEA replacement beneficial in chronic adrenal failure?”. Best Pract. Res. Clin. Endocrinol. Metab. 29 (1): 25–32. doi:10.1016/j.beem.2014.09.007. PMID 25617170.
- Vuksan-Ćusa B, Šagud M, Radoš I (tháng 3 năm 2016). “The role of dehydroepiandrosterone (DHEA) in schizophrenia”. Psychiatr Danub. 28 (1): 30–3. PMID 26938818.
- Prough RA, Clark BJ, Klinge CM (tháng 4 năm 2016). “Novel mechanisms for DHEA action”. J. Mol. Endocrinol. 56 (3): R139–55. doi:10.1530/JME-16-0013. PMID 26908835.
- Qin JC, Fan L, Qin AP (tháng 5 năm 2016). “The effect of dehydroepiandrosterone (DHEA) supplementation on women with diminished ovarian reserve (DOR) in IVF cycle: Evidence from a meta-analysis”. J Gynecol Obstet Biol Reprod (Paris). 46: 1–7. doi:10.1016/j.jgyn.2016.01.002. PMID 27212610.
- Ohnaka K (tháng 7 năm 2016). “[Dehydroepiandrosterone (DHEA) and bone metabolism]”. Clin Calcium (bằng tiếng Nhật). 26 (7): 987–93. PMID 27346309.
- Handelsman DJ, Matsumoto AM, Gerrard DF (tháng 1 năm 2017). “Doping Status of DHEA Treatment for Female Athletes with Adrenal Insufficiency”. Clin J Sport Med. 27 (1): 78–85. doi:10.1097/JSM.0000000000000300. PMID 26844622.
- Qin JC, Fan L, Qin AP (tháng 1 năm 2017). “The effect of dehydroepiandrosterone (DHEA) supplementation on women with diminished ovarian reserve (DOR) in IVF cycle: Evidence from a meta-analysis”. J Gynecol Obstet Hum Reprod. 46 (1): 1–7. doi:10.1016/j.jgyn.2016.01.002. PMID 28403950.
- Labrie F, Martel C, Bélanger A, Pelletier G (tháng 4 năm 2017). “Androgens in women are essentially made from DHEA in each peripheral tissue according to intracrinology”. J. Steroid Biochem. Mol. Biol. 168: 9–18. doi:10.1016/j.jsbmb.2016.12.007. PMID 28153489.
- Triantafyllidou O, Sigalos G, Vlahos N (tháng 6 năm 2017). “Dehydroepiandrosterone (DHEA) supplementation and IVF outcome in poor responders”. Hum Fertil (Camb). 20 (2): 80–87. doi:10.1080/14647273.2016.1262065. PMID 27927044.
- Archer DF, Labrie F, Montesino M, Martel C (tháng 11 năm 2017). “Comparison of intravaginal 6.5mg (0.50%) prasterone, 0.3mg conjugated estrogens and 10μg estradiol on symptoms of vulvovaginal atrophy”. J. Steroid Biochem. Mol. Biol. 174: 1–8. doi:10.1016/j.jsbmb.2017.03.014. PMID 28323042.