Phân tử
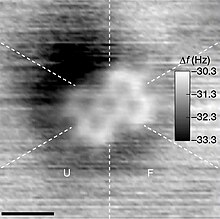


Phân tử là 1 nhóm trung hòa điện tích có nhiều hơn 2 nguyên tử liên kết với nhau bằng các liên kết hóa học.[4][5][6][7][8][9] Các phân tử được phân biệt với các ion do thiếu điện tích. Tuy nhiên, trong vật lý lượng tử, hóa học hữu cơ và hóa sinh, thuật ngữ phân tử thường được sử dụng ít nghiêm ngặt hơn, cũng được áp dụng cho các ion đa nguyên tử.
Trong lý thuyết động học của chất khí, thuật ngữ phân tử thường được sử dụng cho bất kỳ hạt khí nào bất kể thành phần của nó. Theo định nghĩa này, các nguyên tử khí trơ được coi là các phân tử vì chúng là các phân tử đơn phân tử.[10]
Một phân tử có thể là hạt nhân, nghĩa là, nó bao gồm các nguyên tử của một nguyên tố hóa học, như với oxy (O2); hoặc nó có thể là hạt nhân, một hợp chất hóa học bao gồm nhiều hơn một nguyên tố, như với nước (H2O). Các nguyên tử và phức chất được kết nối bởi các tương tác không cộng hóa trị, như liên kết hydro hoặc liên kết ion, thường không được coi là các phân tử đơn lẻ.[11]
Các phân tử như là thành phần của vật chất là phổ biến trong các chất hữu cơ (và do đó sinh hóa). Họ cũng chiếm hầu hết các đại dương và bầu khí quyển. Tuy nhiên, phần lớn các chất rắn quen thuộc trên Trái Đất, bao gồm hầu hết các khoáng chất tạo nên lớp vỏ, lớp phủ và lõi Trái Đất, chứa nhiều liên kết hóa học, nhưng không được tạo thành từ các phân tử có thể nhận dạng được. Ngoài ra, không có phân tử điển hình nào có thể được định nghĩa cho tinh thể ion (muối) và tinh thể cộng hóa trị (chất rắn mạng), mặc dù chúng thường bao gồm các tế bào đơn vị lặp lại kéo dài trong một mặt phẳng (như trong graphene) hoặc ba chiều (như trong kim cương, thạch anh, hoặc natri chloride). Chủ đề của cấu trúc đơn vị tế bào lặp đi lặp lại cũng giữ cho hầu hết các pha cô đặc có liên kết kim loại, có nghĩa là kim loại rắn cũng không được tạo ra từ các phân tử. Trong kính (chất rắn tồn tại ở trạng thái rối loạn thủy tinh thể), các nguyên tử cũng có thể được giữ với nhau bằng liên kết hóa học không có sự hiện diện của bất kỳ phân tử có thể xác định nào, cũng không có bất kỳ sự đều đặn nào của các đơn vị lặp lại đặc trưng cho tinh thể.
Khái niệm phân tử lần đầu được giới thiệu vào năm 1811 bởi Avogadro, sự tồn tại của các phân tử vẫn là một đề tài tranh cãi sôi nổi trong cộng đồng hoá học, cho tới khi năm 1911, khi Perrin công khai các kết quả nghiên cứu của mình. Thuyết phân tử hiện đại đã mang đến nhiều ứng dụng trong tính toán, là cơ sở để hình thành nên ngành hóa học tính toán đương thời.
Khoa học phân tử
[sửa | sửa mã nguồn]Khoa học về phân tử được gọi là hóa học phân tử hoặc vật lý phân tử, tùy thuộc vào việc tập trung vào hóa học hay vật lý. Hóa học phân tử liên quan đến các định luật chi phối sự tương tác giữa các phân tử dẫn đến sự hình thành và phá vỡ các liên kết hóa học, trong khi vật lý phân tử liên quan đến các định luật chi phối cấu trúc và tính chất của chúng. Trong thực tế, tuy nhiên, sự phân biệt này là mơ hồ. Trong khoa học phân tử, một phân tử bao gồm một hệ thống ổn định (trạng thái ràng buộc) gồm hai hoặc nhiều nguyên tử. Các ion polyatomic đôi khi có thể được coi là hữu ích như các phân tử tích điện. Thuật ngữ phân tử không ổn định được sử dụng cho các loài rất dễ phản ứng, tức là các tổ hợp tồn tại ngắn (cộng hưởng) của các electron và hạt nhân, chẳng hạn như các gốc, ion phân tử, phân tử Rydberg, trạng thái chuyển tiếp, phức hợp van der Waals hoặc hệ thống các nguyên tử va chạm như trong Bose mật Einstein ngưng tụ.
Liên kết
[sửa | sửa mã nguồn]Các phân tử được giữ với nhau bằng liên kết cộng hóa trị hoặc liên kết ion. Một số loại nguyên tố phi kim chỉ tồn tại dưới dạng phân tử trong môi trường. Ví dụ, hydro chỉ tồn tại dưới dạng phân tử hydro. Một phân tử của một hợp chất được tạo thành từ hai hoặc nhiều yếu tố.[12]
Hóa trị
[sửa | sửa mã nguồn]
Liên kết cộng hóa trị là liên kết hóa học liên quan đến việc chia sẻ các cặp electron giữa các nguyên tử. Các cặp electron này được gọi là cặp chia sẻ hoặc cặp liên kết và sự cân bằng ổn định của lực hấp dẫn và lực đẩy giữa các nguyên tử, khi chúng chia sẻ electron, được gọi là liên kết cộng hóa trị.[13]
Ion
[sửa | sửa mã nguồn]
Liên kết ion là một loại liên kết hóa học liên quan đến lực hút tĩnh điện giữa các ion tích điện trái dấu và là tương tác chính xảy ra trong các hợp chất ion. Các ion là các nguyên tử đã mất một hoặc nhiều electron (gọi là cation) và các nguyên tử đã thu được một hoặc nhiều electron (gọi là anion).[14] Sự chuyển điện tử này được gọi là điện hóa trái ngược với cộng hóa trị. Trong trường hợp đơn giản nhất, cation là nguyên tử kim loại và anion là nguyên tử phi kim, nhưng các ion này có thể có bản chất phức tạp hơn, ví dụ các ion phân tử như NH4+ hoặc SO42−.
Kích thước của phân tử
[sửa | sửa mã nguồn]Hầu hết các phân tử quá nhỏ để có thể nhìn thấy bằng mắt thường, mặc dù các phân tử của nhiều polyme có thể đạt kích thước vĩ mô, bao gồm cả các phân tử sinh học như DNA. Các phân tử thường được sử dụng làm các khối xây dựng để tổng hợp hữu cơ có kích thước từ một vài angstroms (Å) đến vài chục, hoặc khoảng một phần tỷ mét. Các phân tử đơn lẻ thường không thể được quan sát bằng ánh sáng (như đã lưu ý ở trên), nhưng các phân tử nhỏ và thậm chí các đường viền của các nguyên tử riêng lẻ có thể được truy tìm trong một số trường hợp bằng cách sử dụng kính hiển vi lực nguyên tử. Một số phân tử lớn nhất là đại phân tử hoặc siêu phân tử.
Phân tử nhỏ nhất là hydro (H2), với độ dài liên kết là 0,74.[15]
Bán kính phân tử hiệu quả là kích thước mà một phân tử hiển thị trong dung dịch.[16][17] Bảng tính thấm cho các chất khác nhau chứa các ví dụ.
Công thức phân tử
[sửa | sửa mã nguồn]Các loại công thức hóa học
[sửa | sửa mã nguồn]-Các công thức hóa học cho một phân tử sử dụng một dòng hóa yếu tố ký hiệu, số, và đôi khi cũng biểu tượng khác, chẳng hạn như dấu ngoặc đơn, dấu gạch ngang, dấu ngoặc, và cộng (+) và trừ (-) dấu hiệu. Chúng được giới hạn trong một dòng ký hiệu chính tả, có thể bao gồm các chỉ số và siêu ký tự.
Công thức thực nghiệm của một hợp chất là một loại công thức hóa học rất đơn giản.[18] Đây là tỷ lệ nguyên đơn giản nhất của các nguyên tố hóa học cấu thành nó.[19] Ví dụ, nước luôn bao gồm tỷ lệ 2: 1 của hydro với các nguyên tử oxy và ethanol (rượu ethyl) luôn bao gồm carbon, hydro và oxy theo tỷ lệ 2: 6: 1. Tuy nhiên, điều này không xác định loại phân tử duy nhất - ví dụ dimethyl ether có cùng tỷ lệ với ethanol. Các phân tử có cùng các nguyên tử trong các sắp xếp khác nhau được gọi là các đồng phân. Ngoài ra, carbohydrate, ví dụ, có cùng tỷ lệ (carbon: hydro: oxy = 1: 2: 1) (và do đó có cùng công thức thực nghiệm) nhưng tổng số nguyên tử khác nhau trong phân tử.
Công thức hóa học phản ánh số lượng chính xác các nguyên tử cấu thành phân tử và do đó đặc trưng cho các phân tử khác nhau. Tuy nhiên, các đồng phân khác nhau có thể có cùng thành phần nguyên tử trong khi là các phân tử khác nhau.
Công thức thực nghiệm thường giống như công thức phân tử nhưng không phải lúc nào cũng vậy. Ví dụ, acetylen phân tử có công thức phân tử C2H2, nhưng tỷ lệ nguyên đơn giản nhất của các nguyên tố là CH.
Các khối lượng phân tử có thể được tính từ công thức hóa học và được thể hiện trong truyền thống đơn vị khối lượng nguyên tử bằng 1/12 khối lượng của một không các-bon-12 (12C đồng vị) nguyên tử. Đối với chất rắn mạng, đơn vị công thức hạn được sử dụng trong tính toán cân bằng hóa học.
Công thức cấu trúc
[sửa | sửa mã nguồn]
Đối với các phân tử có cấu trúc 3 chiều phức tạp, đặc biệt là liên quan đến các nguyên tử liên kết với bốn nhóm thế khác nhau, một công thức phân tử đơn giản hoặc thậm chí công thức hóa học bán cấu trúc có thể không đủ để xác định hoàn toàn phân tử. Trong trường hợp này, một loại công thức đồ họa được gọi là công thức cấu trúc có thể cần thiết. Các công thức cấu trúc có thể lần lượt được biểu diễn bằng tên hóa học một chiều, nhưng danh pháp hóa học như vậy đòi hỏi nhiều từ và thuật ngữ không phải là một phần của công thức hóa học.
Hình học phân tử
[sửa | sửa mã nguồn]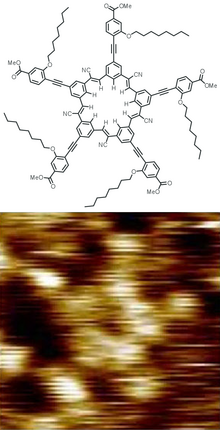
Các phân tử có hình học cân bằng cố định Độ dài liên kết và góc độ của mối quan hệ mà chúng liên tục dao động thông qua các chuyển động dao động và quay. Một chất tinh khiết bao gồm các phân tử có cùng cấu trúc hình học trung bình. Công thức hóa học và cấu trúc của một phân tử là hai yếu tố quan trọng quyết định tính chất của nó, đặc biệt là khả năng phản ứng của nó. Các chất đồng phân có chung một công thức hóa học nhưng thông thường có các tính chất rất khác nhau do cấu trúc khác nhau của chúng. Các đồng phân lập thể, một loại đồng phân đặc biệt, có thể có các tính chất hóa lý rất giống nhau và đồng thời các hoạt động sinh hóa khác nhau.
Quang phổ phân tử
[sửa | sửa mã nguồn]
Quang phổ phân tử liên quan đến phản ứng (phổ) của các phân tử tương tác với các tín hiệu thăm dò của năng lượng đã biết (hoặc tần số, theo công thức của Planck). Các phân tử có mức năng lượng được lượng tử hóa có thể được phân tích bằng cách phát hiện sự trao đổi năng lượng của phân tử thông qua sự hấp thụ hoặc phát xạ.[22] Quang phổ thường không đề cập đến các nghiên cứu nhiễu xạ trong đó các hạt như neutron, electron hoặc tia X năng lượng cao tương tác với sự sắp xếp thường xuyên của các phân tử (như trong tinh thể).
Quang phổ vi sóng thường đo các thay đổi trong quá trình quay của các phân tử và có thể được sử dụng để xác định các phân tử ngoài không gian. Quang phổ hồng ngoại đo sự rung động của các phân tử, bao gồm các chuyển động kéo dài, uốn cong hoặc xoắn. Nó thường được sử dụng để xác định các loại liên kết hoặc nhóm chức trong các phân tử. Những thay đổi trong cách sắp xếp các vạch hấp thụ hoặc phát xạ của electron trong tia cực tím, ánh sáng nhìn thấy hoặc gần tia hồng ngoại và dẫn đến màu sắc. Quang phổ cộng hưởng hạt nhân đo môi trường của các hạt nhân cụ thể trong phân tử và có thể được sử dụng để mô tả số lượng nguyên tử ở các vị trí khác nhau trong một phân tử.
Các khía cạnh lý thuyết
[sửa | sửa mã nguồn]Nghiên cứu về các phân tử bằng vật lý phân tử và hóa học lý thuyết phần lớn dựa trên cơ học lượng tử và rất cần thiết cho sự hiểu biết về liên kết hóa học. Đơn giản nhất trong số các phân tử là phân tử hydro-ion, H2+ và đơn giản nhất trong tất cả các liên kết hóa học là liên kết một electron. H2+ bao gồm hai proton tích điện dương và một electron tích điện âm, có nghĩa là phương trình Schrödinger cho hệ thống có thể được giải quyết dễ dàng hơn do thiếu lực đẩy electron electron. Với sự phát triển của máy tính kỹ thuật số nhanh, các giải pháp gần đúng cho các phân tử phức tạp hơn đã trở thành có thể và là một trong những khía cạnh chính của hóa học tính toán.
Khi cố gắng xác định chặt chẽ liệu một sự sắp xếp các nguyên tử có đủ ổn định để được coi là một phân tử hay không, IUPAC gợi ý rằng nó "phải tương ứng với một chỗ lõm trên bề mặt năng lượng đủ sâu để giam giữ ít nhất một trạng thái rung động".[22] Định nghĩa này không phụ thuộc vào bản chất của sự tương tác giữa các nguyên tử, mà chỉ phụ thuộc vào độ mạnh của sự tương tác. Trên thực tế, nó bao gồm các loài bị ràng buộc yếu mà theo truyền thống không được coi là các phân tử, chẳng hạn như helium dimer, He2, có một trạng thái ràng buộc rung động [23] và bị ràng buộc lỏng lẻo đến mức nó chỉ có thể được quan sát ở mức rất thấp nhiệt độ.
Việc sắp xếp các nguyên tử có đủ ổn định hay không để được coi là một phân tử vốn là một định nghĩa hoạt động. Về mặt triết học, do đó, một phân tử không phải là một thực thể cơ bản (ví dụ, ngược lại, với một hạt cơ bản); đúng hơn, khái niệm về một phân tử là cách nhà hóa học đưa ra tuyên bố hữu ích về sức mạnh của các tương tác quy mô nguyên tử trong thế giới mà chúng ta quan sát.
Xem thêm
[sửa | sửa mã nguồn]- Nguyên tử
- Đơn chất
- Hợp chất
- Nguyên tố hóa học
- Độ âm điện
- Dung dịch
- Công thức hóa học
- Đồng phân
- Số nguyên tử
Tham khảo
[sửa | sửa mã nguồn]- ^ Iwata, Kota; Yamazaki, Shiro; Mutombo, Pingo; Hapala, Prokop; Ondráček, Martin; Jelínek, Pavel; Sugimoto, Yoshiaki (2015). “Chemical structure imaging of a single molecule by atomic force microscopy at room temperature”. Nature Communications. 6: 7766. Bibcode:2015NatCo...6E7766I. doi:10.1038/ncomms8766. PMC 4518281. PMID 26178193.
- ^ Dinca, L.E.; De Marchi, F.; MacLeod, J.M.; Lipton-Duffin, J.; Gatti, R.; Ma, D.; Perepichka, D.F.; Rosei, F. (2015). “Pentacene on Ni(111): Room-temperature molecular packing and temperature-activated conversion to graphene”. Nanoscale. 7 (7): 3263–9. Bibcode:2015Nanos...7.3263D. doi:10.1039/C4NR07057G. PMID 25619890.
- ^ Hapala, Prokop; Švec, Martin; Stetsovych, Oleksandr; Van Der Heijden, Nadine J.; Ondráček, Martin; Van Der Lit, Joost; Mutombo, Pingo; Swart, Ingmar; Jelínek, Pavel (2016). “Mapping the electrostatic force field of single molecules from high-resolution scanning probe images”. Nature Communications. 7: 11560. Bibcode:2016NatCo...711560H. doi:10.1038/ncomms11560. PMC 4894979. PMID 27230940.
- ^ IUPAC, Compendium of Chemical Terminology (Giản lược thuật ngữ hoá học), bản thứ 2 ("Gold Book") (1997). Bản đã chỉnh sửa trực tuyến: (1994) "molecule". doi:10.1351/goldbook.M04002
- ^ Puling, Linus (1970). General Chemistry. New York: Dover Publications, Inc. ISBN 0-486-65622-5.
- ^ Ebbin, Darrell, D. (1990). General Chemistry, 3rd Ed. Boston: Houghton Mifflin Co. ISBN 0-395-43302-9.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- ^ Brown, T.L. (2003). Chemistry – the Central Science, 9th Ed. Kenneth C. Kemp, Theodore L. Brown, Harold Eugene LeMay, Bruce Edward Bursten. New Jersey: Prentice Hall. ISBN 0-13-066997-0.
- ^ Chang, Raymond (1998). Chemistry, 6th Ed. New York: McGraw Hill. ISBN 0-07-115221-0.
- ^ Zumdahl, Steven S. (1997). Chemistry, 4th ed. Boston: Houghton Mifflin. ISBN 0-669-41794-7.
- ^ Chandra, Sulekh (2005). Comprehensive Inorganic Chemistry. New Age Publishers. ISBN 978-81-224-1512-4.
- ^ “Molecule”. Encyclopædia Britannica. ngày 22 tháng 1 năm 2016. Truy cập ngày 23 tháng 2 năm 2016.
- ^ The Hutchinson unabridged encyclopedia with atlas and weather guide. Oxford, England. OCLC 696918830.
- ^ Campbell, Neil A.; Brad Williamson; Robin J. Heyden (2006). Biology: Exploring Life. Boston: Pearson Prentice Hall. ISBN 978-0-13-250882-7. Truy cập ngày 5 tháng 2 năm 2012.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- ^ Campbell, Flake C. (2008). Elements of Metallurgy and Engineering Alloys (bằng tiếng Anh). ASM International. ISBN 978-1-61503-058-3.
- ^ Roger L. DeKock; Harry B. Gray; Harry B. Gray (1989). Chemical structure and bonding. University Science Books. tr. 199. ISBN 978-0-935702-61-3.
- ^ Chang RL; Deen WM; Robertson CR; Brenner BM (1975). “Permselectivity of the glomerular capillary wall: III. Restricted transport of polyanions”. Kidney Int. 8 (4): 212–218. doi:10.1038/ki.1975.104. PMID 1202253.
- ^ Chang RL; Ueki IF; Troy JL; Deen WM; Robertson CR; Brenner BM (1975). “Permselectivity of the glomerular capillary wall to macromolecules. II. Experimental studies in rats using neutral dextran”. Biophys. J. 15 (9): 887–906. Bibcode:1975BpJ....15..887C. doi:10.1016/S0006-3495(75)85863-2. PMC 1334749. PMID 1182263.
- ^ Wink, Donald J.; Fetzer-Gislason, Sharon; McNicholas, Sheila (2003). The Practice of Chemistry (bằng tiếng Anh). Macmillan. ISBN 978-0-7167-4871-7.
- ^ “ChemTeam: Empirical Formula”. www.chemteam.info. Truy cập ngày 16 tháng 4 năm 2017.
- ^ Hirsch, Brandon E.; Lee, Semin; Qiao, Bo; Chen, Chun-Hsing; McDonald, Kevin P.; Tait, Steven L.; fluorod, Amar H. (2014). “Anion-induced dimerization of 5-fold symmetric cyanostars in 3D crystalline solids and 2D self-assembled crystals”. Chemical Communications. 50 (69): 9827–30. doi:10.1039/C4CC03725A. PMID 25080328.
- ^ Zoldan, V. C.; Faccio, R; Pasa, A.A. (2015). “N and p type character of single molecule diodes”. Scientific Reports. 5: 8350. Bibcode:2015NatSR...5E8350Z. doi:10.1038/srep08350. PMC 4322354. PMID 25666850.
- ^ a b IUPAC, Compendium of Chemical Terminology (Giản lược thuật ngữ hoá học), bản thứ 2 ("Gold Book") (1997). Bản đã chỉnh sửa trực tuyến: (2006–) "Phân tử". doi:10.1351/goldbook.M04002
- ^ Anderson JB (tháng 5 năm 2004). “Comment on "An exact quantum Monte Carlo calculation of the helium-helium intermolecular potential" [J. Chem. Phys. 115, 4546 (2001)]”. J Chem Phys. 120 (20): 9886–7. Bibcode:2004JChPh.120.9886A. doi:10.1063/1.1704638. PMID 15268005.
Liên kết ngoài
[sửa | sửa mã nguồn] GIẢM
41%
GIẢM
41%
 GIẢM
25%
GIẢM
25%
 GIẢM
5%
GIẢM
5%
 GIẢM
20%
GIẢM
20%
 GIẢM
32%
GIẢM
32%
 GIẢM
43%
GIẢM
43%