Nguyên tố hóa học
Bài viết này có một danh sách các nguồn tham khảo, nhưng vẫn chưa đáp ứng khả năng kiểm chứng được bởi thân bài vẫn còn thiếu các chú thích trong hàng. (tháng 9/2023) |

| Một phần của loạt bài về |
| Bảng tuần hoàn |
|---|
|
Các tập hợp nguyên tố |
Nguyên tố hóa học, thường được gọi đơn giản là nguyên tố, là một chất hóa học tinh khiết, bao gồm một kiểu nguyên tử, được phân biệt bởi số hiệu nguyên tử, là số lượng proton có trong mỗi hạt nhân[1]. Không giống như các hợp chất hóa học, các nguyên tố hóa học không thể bị phân hủy thành các chất đơn giản hơn bằng các phương pháp hóa học. Số proton trong hạt nhân là đặc tính xác định của một nguyên tố và được gọi là số nguyên tử của nó (được biểu thị bằng ký hiệu Z) – tất cả các nguyên tử có cùng số hiệu nguyên tử đều là nguyên tử của cùng một nguyên tố.[2] Tất cả các baryon vật chất của vũ trụ bao gồm các nguyên tố hóa học. Khi các nguyên tố khác nhau trải qua các phản ứng hóa học, các nguyên tử được sắp xếp lại thành các hợp chất mới được kết nối với nhau bằng các liên kết hóa học. Chỉ một số ít các nguyên tố, chẳng hạn như bạc và vàng, được tìm thấy dưới dạng chưa kết hợp với tư cách là các khoáng chất nguyên tố tự nhiên tương đối tinh khiết. Gần như tất cả các nguyên tố tự nhiên khác xuất hiện trong Trái đất dưới dạng hợp chất hoặc hỗn hợp. Không khí chủ yếu là hỗn hợp của các nguyên tố nitơ, oxy và argon, mặc dù nó có chứa các hợp chất bao gồm carbon dioxide và nước.
Lịch sử phát hiện và sử dụng các nguyên tố bắt đầu từ các xã hội loài người nguyên thủy phát hiện ra các khoáng chất bản địa như carbon, lưu huỳnh, đồng và vàng (mặc dù khái niệm về nguyên tố hóa học vẫn chưa được hiểu rõ). Nỗ lực phân loại các vật liệu như vậy đã dẫn đến các khái niệm về các nguyên tố cổ điển, thuật giả kim và nhiều lý thuyết tương tự khác nhau trong suốt lịch sử loài người. Phần lớn sự hiểu biết hiện đại về các nguyên tố được phát triển từ công trình của Dmitri Mendeleev, một nhà hóa học người Nga. Ông đã công bố bảng tuần hoàn dễ nhận biết đầu tiên vào năm 1869. Bảng này sắp xếp các nguyên tố theo số nguyên tử tăng dần thành các hàng ("chu kỳ") trong đó các nguyên tố cùng cột ("nhóm") có chung các tính chất vật lý và hóa học một cách tuần hoàn. Bảng tuần hoàn tóm tắt các tính chất khác nhau của các nguyên tố, cho phép các nhà hóa học suy ra mối quan hệ giữa chúng và đưa ra dự đoán về các hợp chất và các nguyên tố mới tiềm năng.
Đến tháng 11 năm 2016, Liên minh Quốc tế về Hóa học thuần túy và ứng dụng đã công nhận tổng số 118 nguyên tố. 94 nguyên tố đầu tiên xuất hiện tự nhiên trên Trái Đất, và 24 nguyên tố còn lại là các nguyên tố tổng hợp được tạo ra trong các phản ứng hạt nhân. Trừ ra các nguyên tố phóng xạ không ổn định (hạt nhân phóng xạ) phân hủy nhanh chóng, gần như tất cả các nguyên tố đều có sẵn trong công nghiệp với số lượng khác nhau. Việc khám phá và tổng hợp các nguyên tố mới hơn nữa là một lĩnh vực nghiên cứu khoa học đang diễn ra.
Mô tả
[sửa | sửa mã nguồn]Các nguyên tố hóa học nhẹ nhất là hydro và heli, cả hai đều được tạo ra bởi quá trình tổng hợp hạt nhân Big Bang trong 20 phút đầu tiên của vũ trụ[3] theo tỷ lệ khoảng 3: 1 theo khối lượng (hoặc 12: 1 theo số nguyên tử),[4][5] cùng với những lượng rất nhỏ của hai nguyên tố tiếp theo, lithi và beryli. Hầu hết tất cả các nguyên tố khác được tìm thấy trong tự nhiên đều được tạo ra bằng các phương pháp tổng hợp hạt nhân tự nhiên khác nhau.[6] Trên Trái đất, một lượng nhỏ các nguyên tử mới được tạo ra một cách tự nhiên trong các phản ứng nucleogenic, hoặc trong các quá trình vũ trụ, chẳng hạn như sự phóng xạ tia vũ trụ. Nguyên tử mới cũng được tự nhiên được sản xuất trên Trái Đất như phóng xạ đồng vị phân rã của các quá trình phân rã phóng xạ diễn ra như phân rã alpha, phân rã beta, phân hạch tự phát, phân rã cụm, và các chế độ phân rã hiếm khác.
Trong số 94 nguyên tố có trong tự nhiên, những nguyên tố có số nguyên tử từ 1 đến 82 đều có ít nhất một đồng vị bền (ngoại trừ techneti, nguyên tố 43 và promethi, nguyên tố 61, không có đồng vị bền). Các chất đồng vị được coi là ổn định là những chất chưa quan sát thấy sự phân rã phóng xạ. Các nguyên tố có số hiệu nguyên tử từ 83 đến 94 không ổn định đến mức có thể phát hiện được sự phân rã phóng xạ của tất cả các đồng vị. Một số nguyên tố này, đặc biệt là bismuth (số nguyên tử 83), thori (số nguyên tử 90) và urani (số nguyên tử 92), có một hoặc nhiều đồng vị có chu kỳ bán rã đủ dài để tồn tại dưới dạng tàn dư của quá trình tổng hợp hạt nhân sao nổ tạo ra các kim loại nặng trước khi hình thành Hệ Mặt trời của chúng ta. Với thời gian phân rã hơn 1,9 ×1019 năm, dài hơn một tỷ lần so với tuổi ước tính hiện tại của vũ trụ, bismuth-209 (số nguyên tử 83) có chu kỳ bán rã alpha lâu nhất được biết đến trong số các nguyên tố tự nhiên và hầu như luôn được coi là ngang bằng với 80 nguyên tố ổn định.[7][8] Các nguyên tố rất nặng nhất (những nguyên tố ngoài plutoni, nguyên tố 94) trải qua quá trình phân rã phóng xạ với chu kỳ bán rã ngắn đến mức chúng không được tìm thấy trong tự nhiên và phải được tổng hợp.
Hiện đã có 118 nguyên tố được biết đến. Trong bối cảnh này, "đã biết" có nghĩa là được quan sát đủ rõ, thậm chí chỉ từ một vài sản phẩm phân rã, để được phân biệt với các nguyên tố khác.[9][10] Gần đây nhất, sự tổng hợp của nguyên tố 118 (vì được đặt tên là oganesson) đã được báo cáo vào tháng 10 năm 2006, và sự tổng hợp của nguyên tố 117 (tennessine) được báo cáo vào tháng 4 năm 2010.[11][12] Trong số 118 nguyên tố này, 94 nguyên tố xuất hiện tự nhiên trên Trái đất. Sáu trong số này xảy ra với số lượng vết cực nhỏ: techneti, số nguyên tử 43; promethi, số 61; astatin, số 85; franci, số 87; neptuni, số 93; và plutoni, số 94. 94 nguyên tố này đã được phát hiện trong vũ trụ nói chung, trong quang phổ của các ngôi sao và cả siêu tân tinh, nơi các nguyên tố phóng xạ tồn tại trong thời gian ngắn mới được tạo ra. 94 nguyên tố đầu tiên đã được phát hiện trực tiếp trên Trái đất dưới dạng các nuclide nguyên thủy có từ khi hình thành hệ Mặt trời, hoặc dưới dạng các sản phẩm chuyển hóa hoặc phân hạch xảy ra tự nhiên của urani và thori.
24 nguyên tố nặng hơn còn lại, ngày nay không được tìm thấy trên Trái đất hay trong quang phổ thiên văn, chúng đã được sản xuất nhân tạo: tất cả đều là chất phóng xạ, với chu kỳ bán rã rất ngắn; nếu có bất kỳ nguyên tử nào của các nguyên tố này khi hình thành Trái đất, thì chúng rất có thể, đến mức chắc chắn, đã bị phân rã, và nếu có trong các tân tinh thì chúng có số lượng quá nhỏ để có thể được ghi nhận. Techneti là nguyên tố có chủ đích không phải tự nhiên đầu tiên được tổng hợp vào năm 1937, mặc dù một lượng nhỏ của techneti đã được tìm thấy trong tự nhiên (và nguyên tố này cũng có thể được phát hiện trong tự nhiên vào năm 1925).[13] Mô hình sản xuất nhân tạo và khám phá tự nhiên sau này đã được lặp lại với một số nguyên tố hiếm có nguồn gốc tự nhiên phóng xạ khác.[14]
Danh sách các nguyên tố có sẵn theo tên, số nguyên tử, mật độ, điểm nóng chảy, điểm sôi và theo ký hiệu, cũng như năng lượng ion hóa của các nguyên tố. Các nucleotit của các nguyên tố phóng xạ và ổn định cũng có sẵn dưới dạng danh sách các nuclide, được sắp xếp theo độ dài chu kỳ bán rã của các nguyên tố không ổn định. Một trong những cách trình bày thuận tiện nhất, và chắc chắn là truyền thống nhất về các nguyên tố, là ở dạng bảng tuần hoàn, nhóm các nguyên tố có tính chất hóa học tương tự lại với nhau (và thường là các cấu trúc điện tử tương tự).
Mỗi nguyên tố hóa học đều có một tên và ký hiệu riêng để dễ nhận biết. Tên gọi chính thức của các nguyên tố hóa học được quy định bởi Liên đoàn Quốc tế về Hoá học Thuần túy và Ứng dụng (tiếng Anh: International Union of Pure and Applied Chemistry) (viết tắt: IUPAC). Tổ chức này nói chung chấp nhận tên gọi mà người (hay tổ chức) phát hiện ra nguyên tố đã lựa chọn. Điều này có thể dẫn đến tranh luận là nhóm nghiên cứu nào thực sự tìm ra nguyên tố, là câu hỏi từng làm chậm trễ việc đặt tên cho các nguyên tố với số nguyên tử từ 104 trở lên trong một thời gian dài (Xem thêm Tranh luận về đặt tên nguyên tố). Các nguyên tố hóa học cũng được cấp cho một ký hiệu hóa học thống nhất, dựa trên cơ sở tên gọi của nguyên tố, phần lớn là viết tắt theo tên gọi Latinh. (Ví dụ, carbon có ký hiệu hóa học 'C', natri có ký hiệu hóa học 'Na' từ tên gọi Latinh natrium). Ký hiệu hóa học của nguyên tố được thống nhất và hiểu trên toàn thế giới trong khi tên gọi thông thường của nó khi chuyển sang một ngôn ngữ khác thì phần lớn không giống nhau.
Số nguyên tử
[sửa | sửa mã nguồn]Số nguyên tử của một nguyên tố (ký hiệu Z) bằng số proton trong mỗi nguyên tử và xác định nguyên tố này.[15] Ví dụ, tất cả các nguyên tử carbon đều chứa 6 proton trong hạt nhân nguyên tử của chúng; vậy số nguyên tử của carbon là 6.[16] Nguyên tử carbon có thể có số neutron khác nhau; các nguyên tử của cùng một nguyên tố có số neutron khác nhau được gọi là các đồng vị của nguyên tố đó.[17]
Số proton trong hạt nhân nguyên tử cũng quyết định điện tích của nó, do đó nó quyết định số electron của nguyên tử ở trạng thái không bị ion hóa. Các electron được đặt vào các obitan nguyên tử quyết định các tính chất hóa học khác nhau của nguyên tử. Số lượng neutron trong hạt nhân thường ảnh hưởng rất ít đến tính chất hóa học của nguyên tố (ngoại trừ trường hợp của hydro và đơteri). Do đó, tất cả các đồng vị carbon đều có các tính chất hóa học gần giống nhau vì chúng đều có 6 proton và 6 electron, mặc dù các nguyên tử carbon chẳng hạn có thể có 6 hoặc 8 neutron. Đó là lý do tại sao số nguyên tử, chứ không phải số khối hay trọng lượng nguyên tử, được coi là đặc điểm nhận dạng của một nguyên tố hóa học.
Đồng vị
[sửa | sửa mã nguồn]Đồng vị là những nguyên tử của cùng một nguyên tố (nghĩa là có cùng số proton trong hạt nhân nguyên tử của chúng), nhưng có số neutron khác nhau. Vì vậy, chẳng hạn, có ba đồng vị chính của carbon. Tất cả các nguyên tử carbon đều có 6 proton trong hạt nhân, nhưng chúng có thể có 6, 7 hoặc 8 neutron. Vì số khối của chúng lần lượt là 12, 13 và 14, nên ba đồng vị của carbon được gọi là carbon-12, carbon-13 và carbon-14, thường được viết tắt là 12C, 13C và 14C. Carbon trong cuộc sống hàng ngày và trong hóa học là hỗn hợp của 12C (khoảng 98,9%), 13C (khoảng 1,1%) và khoảng 1 nguyên tử 14C trên một nghìn tỷ nguyên tử tổng cộng.
Hầu hết (66 trong số 94) nguyên tố xuất hiện tự nhiên có nhiều hơn một đồng vị ổn định. Ngoại trừ các đồng vị của hydro (khác nhau rất nhiều về khối lượng tương đối - đủ để gây ra các hiệu ứng hóa học), các đồng vị của một nguyên tố nhất định gần như không thể phân biệt được về mặt hóa học.
Tất cả các nguyên tố đều có một số đồng vị là chất phóng xạ (đồng vị phóng xạ), mặc dù không phải tất cả các đồng vị phóng xạ này đều tồn tại ngoài tự nhiên. Các đồng vị phóng xạ thường phân rã thành các nguyên tố khác khi phóng ra một hạt alpha hoặc beta. Nếu một nguyên tố có các đồng vị không phóng xạ, chúng được gọi là cá đồng vị "ổn định". Tất cả các đồng vị ổn định đã biết đều tồn tại ngoài tự nhiên (xem đồng vị nguyên thủy). Nhiều đồng vị phóng xạ không có trong tự nhiên đã được nghiên cứu sau khi được tạo ra một cách nhân tạo. Một số nguyên tố không có đồng vị bền và chỉ bao gồm các đồng vị phóng xạ: cụ thể là các nguyên tố không có đồng vị bền nào là techneti (số nguyên tử 43), promethi (số nguyên tử 61) và tất cả các nguyên tố quan sát được có số nguyên tử lớn hơn 82.
Trong số 80 nguyên tố có ít nhất một đồng vị bền, 26 nguyên tố chỉ có một đồng vị bền duy nhất. Số đồng vị ổn định trung bình của 80 nguyên tố ổn định là 3,1 đồng vị ổn định trên mỗi nguyên tố. Số lượng đồng vị bền lớn nhất xảy ra đối với một nguyên tố là 10 (thiếc, nguyên tố 50).
Khối lượng đồng vị và khối lượng nguyên tử
[sửa | sửa mã nguồn]Số khối của một nguyên tố A, là số nucleon (proton và neutron) trong hạt nhân nguyên tử. Các đồng vị khác nhau của một nguyên tố nhất định được phân biệt bằng số khối của chúng, được viết theo quy ước dưới dạng ký tự trên bên trái của ký hiệu nguyên tử (ví dụ: 238U). Số khối luôn là một số nguyên và có đơn vị là "nucleon". Ví dụ, magnesi-24 (24 là số khối) là một nguyên tử có 24 nucleon (12 proton và 12 neutron).
Trong khi số khối chỉ đơn giản đếm tổng số neutron và proton và do đó là một số tự nhiên, khối lượng nguyên tử của một nguyên tử là một số thực cho khối lượng của một đồng vị cụ thể (hoặc "nuclide") của nguyên tố, tính bằng đơn vị khối lượng nguyên tử (kí hiệu: u). Nói chung, số khối của một nuclide nhất định khác một chút về giá trị so với khối lượng nguyên tử của nó, vì khối lượng của mỗi proton và neutron không chính xác đúng 1 u; vì các điện tử đóng góp một phần nhỏ hơn vào khối lượng nguyên tử vì số neutron vượt quá số proton; và (cuối cùng) vì năng lượng liên kết hạt nhân. Ví dụ, khối lượng nguyên tử của chlor-35 có năm chữ số có nghĩa là 34,969 u và của chlor-37 là 36,966 u. Tuy nhiên, khối lượng nguyên tử tính bằng u của mỗi đồng vị khá gần với số khối lượng đơn giản của nó (luôn nằm trong khoảng 1%). Đồng vị duy nhất có khối lượng nguyên tử chính xác là một số tự nhiên là 12C, theo định nghĩa có khối lượng chính xác bằng 12 vì u được định nghĩa là 1/12 khối lượng của nguyên tử carbon-12 trung hòa tự do ở trạng thái cơ bản.
Trọng lượng nguyên tử tiêu chuẩn (thường được gọi là "trọng lượng nguyên tử") của một nguyên tố là trung bình cộng của các khối lượng nguyên tử của tất cả các đồng vị của nguyên tố hóa học được tìm thấy trong một môi trường cụ thể, có trọng lượng bằng lượng đồng vị, so với đơn vị khối lượng nguyên tử. Số này có thể là một phân số không gần với một số nguyên. Ví dụ, khối lượng nguyên tử tương đối của chlor là 35,453 u, khác rất nhiều so với một số nguyên vì nó là trung bình của khoảng 76% chlor-35 và 24% chlor-37. Bất cứ khi nào giá trị khối lượng nguyên tử tương đối khác hơn 1% so với một số nguyên, đó là do hiệu ứng trung bình này, vì một lượng đáng kể của nhiều hơn một đồng vị có trong một mẫu nguyên tố đó một cách tự nhiên.
Tinh khiết về mặt hóa học và tinh khiết về mặt đồng vị
[sửa | sửa mã nguồn]Các nhà hóa học và các nhà khoa học hạt nhân có các định nghĩa khác nhau về một nguyên tố tinh khiết. Trong hóa học, nguyên tố nguyên chất có nghĩa là chất mà tất cả các nguyên tử (hoặc trong thực tế là hầu hết) đều có cùng số nguyên tử hoặc số proton. Tuy nhiên, các nhà khoa học hạt nhân định nghĩa một nguyên tố tinh khiết là một nguyên tố chỉ bao gồm một đồng vị ổn định.[18]
Ví dụ, một sợi dây đồng là 99,99% tinh khiết về mặt hóa học nếu 99,99% nguyên tử của nó là đồng, với 29 proton mỗi nguyên tử. Tuy nhiên, nó không phải là đồng vị tinh khiết vì đồng thông thường bao gồm hai đồng vị bền, 69% 63Cu và 31% 65Cu, với số neutron khác nhau. Tuy nhiên, một thỏi vàng nguyên chất sẽ tinh khiết cả về mặt hóa học và đồng vị, vì vàng thông thường chỉ bao gồm một đồng vị, 197Au.
Thù hình
[sửa | sửa mã nguồn]Nguyên tử của các nguyên tố tinh khiết về mặt hóa học có thể liên kết với nhau về mặt hóa học theo nhiều cách, cho phép nguyên tố tinh khiết tồn tại trong nhiều cấu trúc hóa học (cách sắp xếp không gian của các nguyên tử), được gọi là các dạng thù hình, khác nhau về tính chất của chúng. Ví dụ, carbon có thể được tìm thấy dưới các dạng: kim cương, có cấu trúc tứ diện xung quanh mỗi nguyên tử carbon; than chì, có các lớp nguyên tử carbon có cấu trúc lục giác xếp chồng lên nhau; graphene, là một lớp graphit đơn lẻ rất bền; fullerene, có hình dạng gần như hình cầu; và ống nano carbon, là những ống có cấu trúc hình lục giác (thậm chí chúng có thể khác nhau về tính chất điện). Khả năng tồn tại của một nguyên tố ở một trong nhiều dạng cấu trúc được gọi là 'khả năng thù hình'.
Trạng thái chuẩn của một nguyên tố được định nghĩa là trạng thái ổn định nhất về mặt nhiệt động lực học của nó ở áp suất 1 bar và nhiệt độ nhất định (thường ở 298,15 K). Trong nhiệt hóa học, một nguyên tố được định nghĩa là có entanpi tạo thành bằng 0 ở trạng thái chuẩn của nó. Ví dụ, trạng thái tham chiếu của carbon là graphit, vì cấu trúc của graphit ổn định hơn so với các dạng thù hình khác.
Thuộc tính
[sửa | sửa mã nguồn]Một số loại phân loại mô tả có thể được áp dụng rộng rãi cho các nguyên tố, bao gồm việc xem xét các đặc tính vật lý và hóa học chung của chúng, trạng thái vật chất của chúng trong các điều kiện quen thuộc, điểm nóng chảy và sôi của chúng, mật độ của chúng, cấu trúc tinh thể của chúng khi là chất rắn và nguồn gốc của chúng.
Các thuộc tính chung
[sửa | sửa mã nguồn]Một số thuật ngữ thường được sử dụng để mô tả các tính chất vật lý và hóa học chung của các nguyên tố hóa học. Điểm phân biệt đầu tiên là kim loại dễ dẫn điện, phi kim không dẫn điện và một nhóm nhỏ (các á kim), có các đặc tính trung gian và thường hoạt động như chất bán dẫn.
Sự phân loại tinh tế hơn thường được thể hiện trong các bản trình bày màu của bảng tuần hoàn. Hệ thống này hạn chế các thuật ngữ "kim loại" và "phi kim" chỉ đối với một số kim loại và phi kim được xác định rộng hơn, bổ sung các thuật ngữ bổ sung cho một số nhóm kim loại và phi kim được xem rộng rãi hơn. Phiên bản của phân loại này được sử dụng trong bảng tuần hoàn được trình bày ở đây bao gồm: họ actini, kim loại kiềm , kim loại kiềm thổ, halogen, họ lanthan, kim loại chuyển tiếp, kim loại sau chuyển tiếp, á kim, phi kim phản ứng và khí trơ. Trong hệ thống này, các kim loại kiềm, kim loại kiềm thổ và kim loại chuyển tiếp, cũng như các lantan và actini, là các nhóm kim loại đặc biệt được nhìn nhận theo nghĩa rộng hơn. Tương tự, các phi kim phản ứng và các khí quý là các phi kim được nhìn theo nghĩa rộng hơn. Trong một số bài thuyết trình, các halogen không được phân biệt, với astatin được xác định là một kim loại và các chất khác được xác định là phi kim.
Trạng thái vật chất
[sửa | sửa mã nguồn]Một sự phân biệt cơ bản khác thường được sử dụng giữa các nguyên tố là trạng thái vật chất (pha) của chúng, cho dù là rắn, lỏng hay khí, ở nhiệt độ và áp suất tiêu chuẩn đã chọn (STP). Hầu hết các nguyên tố là chất rắn ở nhiệt độ thông thường và áp suất khí quyển, trong khi một số nguyên tố là chất khí. Chỉ có brom và thủy ngân là chất lỏng ở 0 độ C (32 độ F) và áp suất khí quyển bình thường; caesi và gali là chất rắn ở nhiệt độ đó, nhưng nóng chảy ở 28,4 °C (83,2 °F) và 29,8 °C (85,6 °F), tương ứng.
Điểm nóng chảy và điểm sôi
[sửa | sửa mã nguồn]Điểm chảy và điểm sôi, thường được biểu thị bằng độ C ở áp suất của một bầu khí quyển, thường được sử dụng để mô tả đặc tính của các nguyên tố khác nhau. Mặc dù được biết đến với hầu hết các nguyên tố, nhưng một trong hai hoặc cả hai phép đo này vẫn chưa được xác định đối với một số nguyên tố phóng xạ chỉ có sẵn với số lượng rất nhỏ. Vì heli vẫn là chất lỏng ngay cả ở độ không tuyệt đối ở áp suất khí quyển, nên nó chỉ có nhiệt độ sôi chứ không phải nhiệt độ nóng chảy, trong các bài thuyết trình thông thường.
Khối lượng riêng
[sửa | sửa mã nguồn]Khối riêng hay mật độ của ở nhiệt độ và áp suất tiêu chuẩn đã chọn (STP) thường được sử dụng để xác định đặc tính của các phần tử. Mật độ thường được biểu thị bằng gam trên centimet khối (g / cm³). Vì một số nguyên tố là chất khí ở nhiệt độ thường gặp, khối lượng riêng của chúng thường được nêu ở dạng khí; khi hóa lỏng hoặc đông đặc, các nguyên tố khí cũng có khối lượng riêng tương tự như khối lượng riêng của các nguyên tố khác.
Khi một phần tử có các dạng thù hình với các mật độ khác nhau, một dạng thù hình đại diện thường được chọn trong các bản trình bày tóm tắt, trong khi mật độ cho mỗi dạng allotro có thể được nêu khi cung cấp thêm thông tin chi tiết. Ví dụ, ba dạng thù hình quen thuộc của carbon (carbon vô định hình, than chì và kim cương) có khối lượng riêng tương ứng là 1,8–2,1, 2,267 và 3,515 g / cm 3.
Cấu trúc tinh thể
[sửa | sửa mã nguồn]Các nguyên tố được nghiên cứu cho đến nay làm mẫu rắn có tám loại cấu trúc tinh thể : lập phương hình thân, lập phương diện tâm, lục giác, đơn nghiêng, trực thoi, lục phương và bốn phương. Đối với một số nguyên tố sau urani được sản xuất tổng hợp, các mẫu sẵn có quá nhỏ để xác định cấu trúc tinh thể.
Sự xuất hiện và nguồn gốc trên Trái Đất
[sửa | sửa mã nguồn]Các nguyên tố hóa học cũng có thể được phân loại theo nguồn gốc của chúng trên Trái đất, với 94 nguyên tố đầu tiên được coi là xuất hiện ngoài tự nhiên, trong khi những nguyên tố có số nguyên tử ngoài 94 chỉ được sản xuất nhân tạo như là sản phẩm tổng hợp của các phản ứng hạt nhân nhân tạo.
Trong số 94 nguyên tố xuất hiện tự nhiên, 83 nguyên tố được coi là nguyên sinh và có tính phóng xạ yếu hoặc ổn định. 11 nguyên tố tự nhiên còn lại có chu kỳ bán rã quá ngắn để chúng có mặt ở thời kỳ đầu của Hệ Mặt trời, và do đó được coi là các nguyên tố nhất thời. Trong số 11 nguyên tố thoáng qua này, 5 nguyên tố (poloni, radon, radi, actini và protactini) là các sản phẩm phân rã tương đối phổ biến của thori và urani. 6 nguyên tố thoáng qua còn lại (techneti, promethi, astatin, franci, neptuni và plutoni) hiếm khi xảy ra, vì là sản phẩm của các chế độ phân rã hiếm hoặc quá trình phản ứng hạt nhân liên quan đến urani hoặc các nguyên tố nặng khác.
Không có sự phân rã phóng xạ nào được quan sát thấy đối với các nguyên tố có số nguyên tử từ 1 đến 82, ngoại trừ 43 (techneti) và 61 (promethi). Tuy nhiên, đồng vị bền quan sát của một số nguyên tố (như wolfram và chì) được dự đoán là hơi phóng xạ với chu kỳ bán rã rất dài: [18] ví dụ, chu kỳ bán rã được dự đoán cho đồng vị chì ổn định quan sát nằm trong khoảng từ 1035 đến 10189 năm. Các nguyên tố có số nguyên tử 43, 61 và 83 đến 94 không ổn định đủ để có thể dễ dàng phát hiện ra sự phân rã phóng xạ của chúng. Ba trong số các nguyên tố này, bitmut (nguyên tố 83), thori (nguyên tố 90) và urani (nguyên tố 92) có một hoặc nhiều đồng vị có chu kỳ bán rã đủ dài để tồn tại như tàn tích của quá trình tổng hợp hạt nhân sao nổ tạo ra các nguyên tố nặng trước sự hình thành của Hệ Mặt Trời. Ví dụ, với chu kỳ bán rã hơn 1,9×1019 năm, dài hơn một tỷ lần so với tuổi ước tính hiện tại của vũ trụ, bismuth-209 có chu kỳ bán rã alpha lâu nhất được biết đến trong số các nguyên tố tự nhiên. [7] [8] 24 nguyên tố nặng nhất (những nguyên tố ngoài plutoni, nguyên tố 94) trải qua quá trình phân rã phóng xạ với chu kỳ bán rã quá ngắn và không thể được tạo ra như sản phẩm phụ của các nguyên tố có tuổi thọ cao hơn, và do đó hoàn toàn không được biết là có tồn tại ngoài tự nhiên.
Bảng tuần hoàn
[sửa | sửa mã nguồn]| Nhóm → | 1A | 2A | 3B | 4B | 5B | 6B | 7B | 8B | 8B | 8B | 1B | 2B | 3A | 4A | 5A | 6A | 7A | 8A | |
| ↓ Chu kỳ | |||||||||||||||||||
| 1 | 1 H |
2 He | |||||||||||||||||
| 2 | 3 Li |
4 Be |
5 B |
6 C |
7 N |
8 O |
9 F |
10 Ne | |||||||||||
| 3 | 11 Na |
12 Mg |
13 Al |
14 Si |
15 P |
16 S |
17 Cl |
18 Ar | |||||||||||
| 4 | 19 K |
20 Ca |
21 Sc |
22 Ti |
23 V |
24 Cr |
25 Mn |
26 Fe |
27 Co |
28 Ni |
29 Cu |
30 Zn |
31 Ga |
32 Ge |
33 As |
34 Se |
35 Br |
36 Kr | |
| 5 | 37 Rb |
38 Sr |
39 Y |
40 Zr |
41 Nb |
42 Mo |
43 Tc |
44 Ru |
45 Rh |
46 Pd |
47 Ag |
48 Cd |
49 In |
50 Sn |
51 Sb |
52 Te |
53 I |
54 Xe | |
| 6 | 55 Cs |
56 Ba |
* |
72 Hf |
73 Ta |
74 W |
75 Re |
76 Os |
77 Ir |
78 Pt |
79 Au |
80 Hg |
81 Tl |
82 Pb |
83 Bi |
84 Po |
85 At |
86 Rn | |
| 7 | 87 Fr |
88 Ra |
** |
104 Rf |
105 Db |
106 Sg |
107 Bh |
108 Hs |
109 Mt |
110 Ds |
111 Rg |
112 Cn |
113 Nh |
114 Fl |
115 Mc |
116 Lv |
117 Ts |
118 Og | |
| * Họ Lanthan | 57 La |
58 Ce |
59 Pr |
60 Nd |
61 Pm |
62 Sm |
63 Eu |
64 Gd |
65 Tb |
66 Dy |
67 Ho |
68 Er |
69 Tm |
70 Yb |
71 Lu | ||||
| ** Họ Actini | 89 Ac |
90 Th |
91 Pa |
92 U |
93 Np |
94 Pu |
95 Am |
96 Cm |
97 Bk |
98 Cf |
99 Es |
100 Fm |
101 Md |
102 No |
103 Lr | ||||
| |||||
|
| Kim loại kiềm | Kim loại kiềm thổ | Họ Lanthan | Họ Actini | Kim loại chuyển tiếp |
| Kim loại yếu | Á kim | Phi kim | Halogen | Khí hiếm |
Tính chất của các nguyên tố hóa học thường được tóm tắt bằng cách sử dụng bảng tuần hoàn, bảng tuần hoàn sắp xếp các nguyên tố một cách mạnh mẽ và trang nhã bằng cách tăng số nguyên tử thành các hàng ( "chu kỳ" ) trong đó các cột ( "nhóm" ) chia sẻ sự lặp lại ("tuần hoàn") của các tính chất vật lý và tính chất hóa học. Bảng tuần hoàn tiêu chuẩn hiện tại chứa 118 nguyên tố đã được xác nhận tính đến năm 2019.
Mặc dù những tiền thân trước đó của bảng này đã tồn tại, nhưng việc phát minh ra nó thường được ghi công cho nhà hóa học người Nga Dmitri Mendeleev vào năm 1869, người đã dự định dùng bảng để minh họa các xu hướng lặp lại trong các tính chất của các nguyên tố. Bố cục của bảng đã được tinh chỉnh và mở rộng theo thời gian khi các nguyên tố mới được phát hiện và các mô hình lý thuyết mới đã được phát triển để giải thích hành vi hóa học của chúng.
Việc sử dụng bảng tuần hoàn hiện nay đã phổ biến trong ngành học hóa học, cung cấp một khung cực kỳ hữu ích để phân loại, hệ thống hóa và so sánh tất cả các dạng hành vi hóa học khác nhau. Bảng cũng được ứng dụng rộng rãi trong vật lý, địa chất, sinh học, khoa học vật liệu, kỹ thuật, nông nghiệp, y học, dinh dưỡng, sức khỏe môi trường và thiên văn học. Các nguyên tắc của nó đặc biệt quan trọng trong kỹ thuật hóa học.
Nguồn gốc
[sửa | sửa mã nguồn]
Chỉ khoảng 4% tổng khối lượng của vũ trụ được tạo ra từ các nguyên tử hoặc ion, và do đó được biểu thị bằng các nguyên tố hóa học. Phần này chiếm khoảng 15% tổng số vật chất, với phần còn lại của vật chất (85%) là vật chất tối. Bản chất của vật chất tối vẫn chưa được biết, nhưng nó không được cấu tạo bởi các nguyên tử của các nguyên tố hóa học vì nó không chứa proton, neutron hoặc electron. (Phần phi vật chất còn lại của khối lượng vũ trụ được cấu tạo từ năng lượng tối thậm chí còn ít được hiểu rõ hơn).
94 nguyên tố hóa học có trong tự nhiên được tạo ra bởi ít nhất bốn lớp của quá trình vật lý thiên văn. Hầu hết hydro, heli và một lượng rất nhỏ lithi được tạo ra trong vài phút đầu tiên của Vụ Nổ Lớn. Quá trình tổng hợp hạt nhân Big Bang này chỉ xảy ra một lần; các quá trình khác đang diễn ra. Phản ứng tổng hợp hạt nhân bên trong các ngôi sao tạo ra các nguyên tố thông qua quá trình tổng hợp hạt nhân của các ngôi sao, bao gồm tất cả các nguyên tố từ carbon đến sắt về số lượng nguyên tử. Các nguyên tố có số nguyên tử cao hơn sắt, bao gồm các nguyên tố nặng như urani và plutoni, được tạo ra bởi nhiều dạng tổng hợp hạt nhân bùng nổ khác nhau trong quá trình sáp nhập sao siêu mới và neutron. Các nguyên tố nhẹ lithi, beryli và bor được tạo ra hầu hết thông qua sự phân tán tia vũ trụ (sự phân mảnh do tia vũ trụ gây ra) của carbon, nitơ và oxy.
Trong giai đoạn đầu của Vụ Nổ Lớn, sự tổng hợp hạt nhân của hạt nhân hydro dẫn đến việc sản xuất ra hydro-1 (proti, 1H) và heli-4 (4He), cũng như một lượng nhỏ hơn deuteri (2H) và lượng rất nhỏ (theo lũy thừa 10−10) của lithi và beryli. Thậm chí một lượng nguyên tố bor nhỏ hơn có thể đã được tạo ra trong Vụ Nổ Lớn, vì nó đã được quan sát thấy ở một số ngôi sao rất cũ, trong khi carbon thì không.[19] Không có nguyên tố nào nặng hơn bor được tạo ra trong Vụ Nổ Lớn. Kết quả là, sự phong phú ban đầu của các nguyên tử (hoặc ion) bao gồm khoảng 75% 1H, 25% 4He, và 0,01% đơteri, chỉ với những lượng rất nhỏ lithi, beryli và có lẽ là bo.[20] Sự làm giàu sau đó của các quầng thiên hà xảy ra do quá trình tổng hợp hạt nhân sao và quá trình tổng hợp hạt nhân siêu tân tinh.[21] Tuy nhiên, sự phong phú của nguyên tố trong không gian giữa các thiên hà vẫn có thể gần giống với các điều kiện nguyên thủy, trừ khi nó đã được làm giàu bằng một số phương pháp.
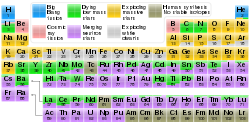
Trên Trái đất (và các nơi khác), lượng nhỏ của các nguyên tố khác nhau tiếp tục được tạo ra từ các nguyên tố khác như là sản phẩm của quá trình biến đổi hạt nhân. Chúng bao gồm một số được tạo ra bởi các tia vũ trụ hoặc các phản ứng hạt nhân khác (xem các nuclid vũ trụ và nucleogenic ), và một số khác được tạo ra dưới dạng sản phẩm phân rã của các nuclide nguyên thủy tồn tại lâu dài.[22] Ví dụ, một lượng vết (nhưng có thể phát hiện được) của carbon-14 (14C) liên tục được tạo ra trong khí quyển do các tia vũ trụ tác động vào các nguyên tử nitơ và argon-40 ( 40Ar) liên tục được tạo ra do sự phân hủy của kali-40 (40K) nguyên thủy nhưng không ổn định. Ngoài ra, ba nguyên tố nguyên thủy xuất hiện trừ các nguyên tố có tính phóng xạ thuộc họ actini, đó là thori, urani và plutoni, phân rã qua một loạt các định kỳ sản xuất nhưng không ổn định các yếu tố phóng xạ như radi và radon, vốn chỉ xuất hiện thoáng qua trong bất kỳ mẫu của các kim loại này hoặc quặng hoặc các hợp chất của chúng. Ba nguyên tố phóng xạ khác, techneti, promethi và neptuni, chỉ xuất hiện ngẫu nhiên trong các vật liệu tự nhiên, được tạo ra dưới dạng các nguyên tử riêng lẻ bằng cách phân hạch hạt nhân của các hạt nhân của các nguyên tố nặng khác nhau hoặc trong các quá trình hạt nhân hiếm gặp khác.
Ngoài 94 nguyên tố tự nhiên, một số nguyên tố nhân tạo đã được sản xuất bằng công nghệ vật lý hạt nhân của con người. Tính đến năm 2021[cập nhật], những thí nghiệm này đã tạo ra tất cả các nguyên tố lên đến số nguyên tử 118.
Lượng nguyên tố trong tự nhiên
[sửa | sửa mã nguồn]Biểu đồ sau (thang log) cho thấy sự phong phú của các nguyên tố trong Hệ Mặt Trời của chúng ta. Bảng cho thấy mười hai nguyên tố phổ biến nhất trong thiên hà của chúng ta (ước tính theo phương pháp quang phổ), được đo bằng phần triệu, khối lượng.[23] Các thiên hà gần đó đã phát triển dọc theo các đường tương tự có sự làm giàu tương ứng của các nguyên tố nặng hơn hydro và heli. Các thiên hà xa hơn đang được xem như chúng đã xuất hiện trong quá khứ, vì vậy lượng nguyên tố dồi dào của chúng dường như gần với hỗn hợp nguyên thủy hơn. Tuy nhiên, khi các quy luật và quy trình vật lý xuất hiện phổ biến trong vũ trụ hữu hình, các nhà khoa học kỳ vọng rằng các thiên hà này đã tiến hóa các nguyên tố với mức độ phong phú tương tự.

Sự phong phú của các nguyên tố trong Hệ Mặt trời phù hợp với nguồn gốc của chúng từ quá trình tổng hợp hạt nhân trong Vụ Nổ Lớn và một số sao siêu tân tinh tiền thân. Hydro và heli rất dồi dào là sản phẩm của Vụ nổ lớn, nhưng ba nguyên tố tiếp theo rất hiếm vì chúng có rất ít thời gian hình thành trong Vụ nổ lớn và không được tạo ra trong các ngôi sao (tuy nhiên, chúng được tạo ra với số lượng nhỏ do sự tan rã của các nguyên tố nặng hơn trong bụi giữa các vì sao, do tác động của tia vũ trụ ). Bắt đầu với carbon, các nguyên tố được tạo ra trong các ngôi sao bằng cách tích tụ từ các hạt alpha (hạt nhân heli), dẫn đến sự phong phú xen kẽ của các nguyên tố có số nguyên tử chẵn (những nguyên tố này cũng ổn định hơn). Nói chung, các nguyên tố như sắt được tạo ra trong các ngôi sao lớn trong quá trình trở thành siêu tân tinh. Sắt-56 đặc biệt phổ biến, vì nó là nguyên tố ổn định nhất có thể dễ dàng được tạo ra từ các hạt alpha (là sản phẩm của sự phân rã phóng xạ nickel-56, cuối cùng được tạo ra từ 14 hạt nhân heli). Các nguyên tố nặng hơn sắt được tạo ra trong quá trình hấp thụ năng lượng ở các ngôi sao lớn, và sự phong phú của chúng trong vũ trụ (và trên Trái đất) thường giảm theo số nguyên tử của chúng.
Sự phong phú của các nguyên tố hóa học trên Trái Đất thay đổi từ không khí đến lớp vỏ đến đại dương, và trong các dạng sống khác nhau. Sự phong phú của các nguyên tố trong lớp vỏ Trái đất khác với sự phong phú của các nguyên tố trong Hệ Mặt trời (như được thấy ở Mặt trời và các hành tinh nặng như Sao Mộc) chủ yếu ở việc mất đi có chọn lọc các nguyên tố rất nhẹ nhất (hydro và heli) và cả neon, carbon dễ bay hơi (như hydrocarbon), nitơ và lưu huỳnh, là kết quả của quá trình sưởi ấm bằng năng lượng mặt trời trong giai đoạn đầu hình thành hệ mặt trời. Oxy, nguyên tố Trái đất dồi dào nhất tính theo khối lượng, được giữ lại trên Trái đất bằng cách kết hợp với silic. Nhôm có 8% khối lượng phổ biến hơn trong vỏ Trái đất so với vũ trụ và Hệ Mặt trời, nhưng thành phần của lớp phủ cồng kềnh hơn nhiều, có magnesi và sắt thay cho nhôm (chỉ xuất hiện ở 2% khối lượng) phản ánh chặt chẽ hơn thành phần nguyên tố của Hệ Mặt Trời, chưa kể sự mất mát được ghi nhận của các nguyên tố dễ bay hơi vào không gian và mất lượng nguyên tố sắt đã di chuyển đến lõi của Trái Đất.
Ngược lại, thành phần của cơ thể con người theo sát thành phần của nước biển - giúp cơ thể con người có thêm lượng dự trữ carbon và nitơ cần thiết để tạo thành protein và acidnucleic, cùng với phosphor trong acidnucleic và phân tử truyền năng lượng. Adenosine triphosphate (ATP) xuất hiện trong tế bào của tất cả các sinh vật sống. Một số loại sinh vật đòi hỏi các nguyên tố đặc biệt bổ sung, ví dụ như magnesi trong chất diệp lục trong cây xanh, các calci trong vỏ động vật thân mềm, hoặc sắt trong hemoglobin trong hồng cầu của động vật có xương sống.
Lịch sử
[sửa | sửa mã nguồn]
Phát triển các định nghĩa
[sửa | sửa mã nguồn]Khái niệm "nguyên tố" như một chất không thể phân chia đã phát triển qua ba giai đoạn lịch sử chính: Định nghĩa cổ điển (chẳng hạn như định nghĩa của người Hy Lạp cổ đại), định nghĩa hóa học và định nghĩa hạt nhân.
Định nghĩa cổ điển
[sửa | sửa mã nguồn]Triết học cổ đại đặt ra một tập hợp các nguyên tố cổ điển để giải thích các mô hình quan sát được trong tự nhiên. Những nguyên tố này ban đầu được gọi là đất, nước, khí và lửa thay vì các nguyên tố hóa học của khoa học hiện đại.
Thuật ngữ 'nguyên tố' (stoicheia) lần đầu tiên được nhà triết học Hy Lạp Plato sử dụng vào khoảng năm 360 TCN trong cuộc đối thoại của ông với Timaeus, trong đó bao gồm một cuộc thảo luận của các thành phần của các cơ quan vô cơ và hữu cơ và là một chuyên luận phỏng đoán về hóa học. Plato tin rằng các nguyên tố được Empedocles đưa vào một thế kỷ trước đó bao gồm các dạng đa diện nhỏ: tứ diện (lửa), bát diện (khí), nhị thập diện (nước) và khối lập phương (đất).[24][25]
Aristotle, khoảng năm 350 TCN, cũng sử dụng từ stoicheia và bổ sung thêm một nguyên tố thứ năm gọi là aether, mà hình thành các tầng trời. Aristotle đã định nghĩa một nguyên tố là:
Element – one of those bodies into which other bodies can decompose, and that itself is not capable of being divided into other.[26]
Định nghĩa hóa học
[sửa | sửa mã nguồn]
Năm 1661, Robert Boyle đề xuất lý thuyết về vật thể của mình, trong đó ủng hộ việc phân tích vật chất được cấu thành bởi các đơn vị vật chất không thể thu nhỏ hơn được (nguyên tử) và, không chọn quan điểm của Aristotle về bốn nguyên tố cũng như quan điểm của Paracelsus về ba nguyên tố cơ bản, và còn bỏ ngỏ. câu hỏi về số lượng nguyên tố. [27] Danh sách các nguyên tố hóa học hiện đại đầu tiên được đưa ra trong Các nguyên tố hóa học năm 1789 của Antoine Lavoisier, chứa ba mươi ba nguyên tố, bao gồm cả ánh sáng và nhiệt lượng.[28] Đến năm 1818, Jöns Jakob Berzelius đã xác định được trọng lượng nguyên tử cho 45 trong số 49nguyên tố được chấp nhận sau đó. Dmitri Mendeleev đưa ra 66 nguyên tố trong bảng tuần hoàn của ông vào năm 1869.
Từ thời Boyle cho đến đầu thế kỷ 20, một nguyên tố được định nghĩa là một chất tinh khiết không thể bị phân hủy thành bất kỳ chất nào đơn giản hơn.[27] Nói cách khác, một nguyên tố hóa học không thể chuyển hóa thành các nguyên tố hóa học khác bằng các quá trình hóa học. Các nguyên tố trong thời gian này thường được phân biệt bằng khối lượng nguyên tử của chúng, một đặc tính có thể đo được với độ chính xác khá cao bằng các kỹ thuật phân tích có sẵn.
Định nghĩa hạt nhân
[sửa | sửa mã nguồn]Phát hiện năm 1913 của nhà vật lý người Anh Henry Moseley rằng điện tích hạt nhân là cơ sở vật lý cho số nguyên tử của một nguyên tử, được hoàn thiện thêm khi bản chất của proton và neutron được nhìn nhận, cuối cùng dẫn đến định nghĩa hiện tại về một nguyên tố dựa trên số nguyên tử (số proton trên mỗi hạt nhân nguyên tử). Việc sử dụng các số nguyên tử, chứ không phải là khối lượng nguyên tử, để phân biệt các nguyên tố có giá trị tiên đoán lớn hơn (do những con số là các số nguyên), và cũng có thể giải quyết một số những mập mờ trong giao diện hóa học dựa trên do tính chất của biến đổi đồng vị và thù hình trong cùng một nguyên tố. Hiện tại, IUPAC xác định một nguyên tố tồn tại nếu nó có các đồng vị có thời gian sống lâu hơn 10−14 giây, thời gian mà hạt nhân cần đến để tạo thành một đám mây điện tử.[29]
Đến năm 1914, 72 nguyên tố đã được biết đến, tất cả đều xuất hiện trong tự nhiên.[30] Các nguyên tố trong tự nhiên còn lại đã được phát hiện hoặc chiết tách trong những thập kỷ tiếp theo, và nhiều nguyên tố bổ sung khác cũng đã được sản xuất tổng hợp, với phần lớn công trình đó do Glenn T. Seaborg đi tiên phong. Năm 1955, nguyên tố 101 được phát hiện và đặt tên là mendelevi để vinh danh D. I. Mendeleev, người đầu tiên sắp xếp các nguyên tố theo cách tuần hoàn.
Khám phá và công nhận các nguyên tố khác nhau
[sửa | sửa mã nguồn]Mười chất liệu quen thuộc với các nền văn hóa tiền sử khác nhau hiện được biết đến là các nguyên tố hóa học: carbon, đồng, vàng, sắt, chì, thủy ngân, bạc, lưu huỳnh, thiếc và kẽm. Ba vật liệu bổ sung hiện được chấp nhận là nguyên tố, arsenic, antimon và bismuth, đã được công nhận là các chất riêng biệt trước năm 1500. Phosphor, cobalt và platin đã được phân lập trước năm 1750.
Hầu hết các nguyên tố hóa học trong tự nhiên còn lại đã được xác định và ghi nhận tính chất vào năm 1900, bao gồm:
- Các vật liệu công nghiệp quen thuộc hiện nay như nhôm, silicon, nickel, chromi, magnesi và wolfram
- Các kim loại phản ứng như lithi, natri, kali và calci
- Các halogen fluor, chlor, brom và iod
- Các khí như hydro, oxy, nitơ, heli, argon và neon
- Hầu hết các nguyên tố đất hiếm, bao gồm ceri, lantan, gadolini và neodymi.
- Các nguyên tố phóng xạ phổ biến hơn, bao gồm urani, thori, radi và radon
Các nguyên tố được phân lập hoặc sản xuất kể từ năm 1900 bao gồm:
- Ba nguyên tố tự nhiên ổn định thường xuyên chưa được phát hiện còn lại: hafni, luteti, và rheni
- Plutoni, được Glenn T. Seaborg sản xuất tổng hợp lần đầu tiên vào năm 1940, nhưng bây giờ cũng được biết đến từ một vài sự kiện xảy ra trong tự nhiên với thời gian dài
- Ba nguyên tố tự nhiên xuất hiện ngẫu nhiên ( neptuni, promethi và techneti), lần đầu tiên được sản xuất tổng hợp nhưng sau đó được phát hiện với lượng nhỏ trong một số mẫu địa chất nhất định
- Bốn sản phẩm phân rã hiếm của urani hoặc thori (astatine, franci, actini và protactini), và
- Các nguyên tố siêu urani tổng hợp khác nhau, bắt đầu bằng americi và curi.
Các nguyên tố được phát hiện gần đây
[sửa | sửa mã nguồn]Nguyên tố siêu urani đầu tiên (nguyên tố có số nguyên tử lớn hơn 92) được phát hiện là neptuni vào năm 1940. Kể từ năm 1999, các tuyên bố về việc phát hiện ra các nguyên tố mới đã được Ban công tác chung IUPAC/IUPAP xem xét. Tính đến tháng 1 năm 2016, tất cả 118 nguyên tố đã được IUPAC xác nhận là đã phát hiện ra. Việc phát hiện ra nguyên tố 112 đã được công nhận vào năm 2009, và cái tên copernici và ký hiệu nguyên tử Cn đã được gợi ý cho nguyên tố này.[31] Tên và biểu tượng của nguyên tố này đã được IUPAC chính thức xác nhận vào ngày 19 tháng 2 năm 2010.[32] Nguyên tố nặng nhất được cho là đã được tổng hợp cho đến nay là nguyên tố 118, oganesson, vào ngày 9 tháng 10 năm 2006, do Phòng thí nghiệm phản ứng hạt nhân Flerov ở Dubna, Nga tìm ra. [10][33] Tennessine, nguyên tố 117 là nguyên tố mới nhất được tuyên bố là đã được phát hiện, vào năm 2009.[34] Vào ngày 28 tháng 11 năm 2016, các nhà khoa học tại IUPAC đã chính thức công nhận tên của bốn nguyên tố hóa học mới nhất, với các số hiệu nguyên tử 113, 115, 117 và 118.[35][36]
Danh sách nguyên tố hóa học
[sửa | sửa mã nguồn]| Tên tiếng Việt | Tên tiếng Latinh | Ký hiệu nguyên tố hóa học |
Số nguyên tử | Nguyên tử lượng Ar |
Năm phát hiện |
|---|---|---|---|---|---|
| actini | actini | Ac | 89 | 227,0277)* | 1899 |
| americi | americi | Am | 95 | 243,0614)* | 1944 |
| antimon
(Stibi) |
stibi
(antimoni) |
Sb | 51 | 121,75 | thời thượng cổ |
| argon | argon | Ar | 18 | 39,948 | 1894 |
| arsenic | arsenicum | As | 33 | 74,922 | thời trung cổ |
| astatin | astati | At | 85 | 209,9871)* | 1940 |
| bari | bari | Ba | 56 | 137,34 | 1774 |
| berkeli | berkeli | Bk | 97 | 247,0703)* | 1950 |
| beryli | berylli | Be | 4 | 9,0122 | 1797 |
| bismuth | bismutum | Bi | 83 | 208,980 | thời thượng cổ |
| bohri | bohri | Bh | 107 | 264,12)* | 1981 |
| bor | boroni | B | 5 | 10,811 | 1808 |
| brom | bromum | Br | 35 | 79,909 | 1826 |
| carbon | carboneum | C | 6 | 12,01115 | thời thượng cổ |
| ceri | ceri | Ce | 58 | 140,12 | 1803 |
| caesi | caesi | Cs | 55 | 132,905 | 1860 |
| thiếc | stannum | Sn | 50 | 118,69 | thời thượng cổ |
| curi | curi | Cm | 96 | 247,0704)* | 1944 |
| darmstadti | darmstadti | Ds | 110 | 271)* | 1994 |
| kali | kali | K | 19 | 39,102 | 1807 |
| dubni | dubni | Db | 105 | 262,1144)* | 1970 |
| nitơ | nitrogen | N | 7 | 14,0067 | 1772 |
| dysprosi | dysprosi | Dy | 66 | 162,50 | 1886 |
| einsteini | einsteini | Es | 99 | 252,0830)* | 1952 |
| erbi | erbi | Er | 68 | 167,26 | 1843 |
| europi | europi | Eu | 63 | 151,964 | 1901 |
| fermi | fermi | Fm | 100 | 257,0951)* | 1952 |
| fluor | fluorum | F | 9 | 18,9984 | 1886 |
| phosphor | phosphorus | P | 15 | 30,973 8 | 1669 |
| franci | franci | Fr | 87 | 223,0197)* | 1939 |
| gadolini | gadolini | Gd | 64 | 157,25 | 1880 |
| gali | galli | Ga | 31 | 69,72 | 1875 |
| germani | germani | Ge | 32 | 72,59 | 1886 |
| hafni | hafni | Hf | 72 | 178,49 | 1923 |
| hassi | hassi | Hs | 108 | 265,1306)* | 1984 |
| heli | heli | He | 2 | 4,0026 | 1868 |
| nhôm | aluminum | Al | 13 | 26,9815 | 1825 |
| holmi | holmi | Ho | 67 | 164,930 | 1879 |
| magnesi | magnesi | Mg | 12 | 24,312 | 1775 |
| chlor | chlorum | Cl | 17 | 35,453 | 1774 |
| chromi | chromi | Cr | 24 | 51,996 | 1797 |
| indi | indi | In | 49 | 114,82 | 1863 |
| iridi | iridi | Ir | 77 | 192,2 | 1802 |
| iod | iodum | I | 53 | 126,904 | 1811 |
| cadmi | cadmi | Cd | 48 | 112,40 | 1817 |
| californi | californi | Cf | 98 | 251,0796)* | 1950 |
| cobalt | cobaltum | Co | 27 | 58,933 | 1735 |
| krypton | krypton | Kr | 36 | 83,80 | 1898 |
| silic | siliconi | Si | 14 | 28,086 | 1823 |
| oxy | oxygen | O | 8 | 15,9994 | 1774 |
| lanthan | lanthanum | La | 57 | 138,91 | 1839 |
| lawrenci | laurenti | Lr | 103 | 262,1097)* | 1961 |
| lithi | lithi | Li | 3 | 6,939 | 1817 |
| luteti | luteti | Lu | 71 | 174,97 | 1907 |
| mangan | manganum | Mn | 25 | 54,938 | 1774 |
| đồng | cuprum | Cu | 29 | 63,54 | thời thượng cổ |
| meitneri | meitneri | Mt | 109 | 268,1388)* | 1982 |
| mendelevi | mendelevi | Md | 101 | 258,0984)* | 1955 |
| molypden | molybdenum | Mo | 42 | 95,94 | 1778 |
| neodymi | neodymi | Nd | 60 | 144,24 | 1885 |
| neon | neon | Ne | 10 | 20,183 | 1898 |
| neptuni | neptuni | Np | 93 | 237,0482)* | 1940 |
| nickel | nickelum | Ni | 28 | 58,71 | 1751 |
| niobi | niobi | Nb | 41 | 92,906 | 1801 |
| nobeli | nobeli | No | 102 | 259,1010)* | 1958 |
| chì | plumbum | Pb | 82 | 207,19 | thời thượng cổ |
| osmi | osmi | Os | 76 | 190,2 | 1803 |
| paladi | palladi | Pd | 46 | 106,4 | 1803 |
| platin | platinum | Pt | 78 | 195,09 | 1738 |
| plutoni | plutoni | Pu | 94 | 244,0642)* | 1940 |
| poloni | poloni | Po | 84 | 208,9824)* | 1898 |
| praseodymi | praseodymi | Pr | 59 | 140,907 | 1885 |
| promethi | promethi | Pm | 61 | 145 | 1938 |
| protactini | protactini | Pa | 91 | 231,0359)* | 1917 |
| radi | radi | Ra | 88 | 226,0254)* | 1898 |
| radon | radon | Rn | 86 | 222,0176)* | 1900 |
| rheni | rheni | Re | 75 | 186,2 | 1924 |
| rhodi | rhodi | Rh | 45 | 102,905 | 1803 |
| roentgeni | roentgeni | Rg | 111 | 272)* | 1994 |
| thủy ngân | hydrargyrum | Hg | 80 | 200,59 | thời thượng cổ |
| rubidi | rubidi | Rb | 37 | 85,47 | 1861 |
| rutheni | rutheni | Ru | 44 | 101,107 | 1844 |
| rutherfordi | rutherfordi | Rf | 104 | 261,1088)* | 1964 |
| samari | samari | Sm | 62 | 150,35 | 1879 |
| seaborgi | seaborgi | Sg | 106 | 263,1186)* | 1974 |
| seleni | seleni | Se | 34 | 78,96 | 1817 |
| lưu huỳnh | sulfur | S | 16 | 32,064 | thời thượng cổ |
| scandi | scandi | Sc | 21 | 44,956 | 1879 |
| natri | natri | Na | 11 | 22,9898 | 1807 |
| stronti | stronti | Sr | 38 | 87,62 | 1790 |
| bạc | argentum | Ag | 47 | 107,870 | thời thượng cổ |
| tantal | tantalum | Ta | 73 | 180,948 | 1802 |
| techneti | techneti | Tc | 43 | 97,9072 | 1937 |
| teluri | telluri | Te | 52 | 127,60 | 1782 |
| terbi | terbi | Tb | 65 | 158,924 | 1843 |
| thali | thalli | Tl | 81 | 204,37 | 1861 |
| thori | thori | Th | 90 | 232,0381* | 1828 |
| thuli | thuli | Tm | 69 | 168,934 | 1879 |
| titan | titani | Ti | 22 | 47,90 | 1791 |
| urani | urani | U | 92 | (238) | 1789 |
| vanadi | vanadi | V | 23 | 50,942 | 1830 |
| calci | calci | Ca | 20 | 40,08 | 1808 |
| hydro | hydrogen | H | 1 | 1,00797 | 1766 |
| wolfram | wolframi
(tungsteni) |
W | 74 | 183,85 | 1781 |
| xenon | xenon | Xe | 54 | 131,30 | 1898 |
| ytterbi | ytterbi | Yb | 70 | 173,04 | 1878 |
| ytri | ytri | Y | 39 | 88,905 | 1794 |
| kẽm | zincum | Zn | 30 | 65,37 | thời thượng cổ |
| zirconi | zirconi | Zr | 40 | 91,22 | 1789 |
| vàng | aurum | Au | 79 | 196,967 | thời thượng cổ |
| sắt | ferrum | Fe | 26 | 55,847 | thời thượng cổ |
Xem thêm
[sửa | sửa mã nguồn]- Tên các nguyên tố
- Hóa học
- Sự phổ biến của các nguyên tố hóa học
- Tên gọi hệ thống của các nguyên tố
- Các nguyên tố hư cấu
- Các nguyên tố đặt tên theo danh nhân
- Các nguyên tố đặt tên theo địa danh
- Hợp chất
chú thích
[sửa | sửa mã nguồn]- ^ IUPAC, Compendium of Chemical Terminology (Giản lược thuật ngữ hoá học), bản thứ 2 ("Gold Book") (1997). Bản đã chỉnh sửa trực tuyến: (2006–) "[1]". doi:10.1351/goldbook.C01022
- ^ IUPAC, Compendium of Chemical Terminology (Giản lược thuật ngữ hoá học), bản thứ 2 ("Gold Book") (1997). Bản đã chỉnh sửa trực tuyến: (2006–) "chemical element". doi:10.1351/goldbook.C01022
- ^ See the timeline on p.10 in Oganessian, Yu. Ts.; Utyonkov, V.; Lobanov, Yu.; và đồng nghiệp (2006). "Evidence for Dark Matter" (PDF). Physical Review C. Quyển 74 số 4. tr. 044602. Bibcode:2006PhRvC..74d4602O. doi:10.1103/PhysRevC.74.044602. ISSN 0556-2813. Bản gốc (PDF) lưu trữ ngày 13 tháng 2 năm 2021. Truy cập ngày 9 tháng 9 năm 2021.
- ^ lbl.gov (2005). "The Universe Adventure Hydrogen and Helium". Lawrence Berkeley National Laboratory U.S. Department of Energy. Bản gốc lưu trữ ngày 21 tháng 9 năm 2013.
- ^ astro.soton.ac.uk (ngày 3 tháng 1 năm 2001). "Formation of the light elements". University of Southampton. Bản gốc lưu trữ ngày 21 tháng 9 năm 2013.
- ^ foothill.edu (ngày 18 tháng 10 năm 2006). "How Stars Make Energy and New Elements" (PDF). Foothill College.
- ^ a b Dumé, B. (ngày 23 tháng 4 năm 2003). "Bismuth breaks half-life record for alpha decay". Physicsworld.com. Bristol, England: Institute of Physics. Truy cập ngày 14 tháng 7 năm 2015.
- ^ a b de Marcillac, P.; Coron, N.; Dambier, G.; Leblanc, J.; Moalic, J-P (2003). "Experimental detection of alpha-particles from the radioactive decay of natural bismuth". Nature. Quyển 422 số 6934. tr. 876–8. Bibcode:2003Natur.422..876D. doi:10.1038/nature01541. PMID 12712201.
- ^ Sanderson, K. (ngày 17 tháng 10 năm 2006). "Heaviest element made – again". News@nature. doi:10.1038/news061016-4.
- ^ a b Schewe, P.; Stein, B. (ngày 17 tháng 10 năm 2000). "Elements 116 and 118 Are Discovered". Physics News Update. American Institute of Physics. Bản gốc lưu trữ ngày 1 tháng 1 năm 2012. Truy cập ngày 19 tháng 10 năm 2006.
- ^ Glanz, J. (ngày 6 tháng 4 năm 2010). "Scientists Discover Heavy New Element". The New York Times.
- ^ Oganessian, Yu. Ts.; Abdullin, F. Sh.; Bailey, P. D.; và đồng nghiệp (tháng 4 năm 2010). "Synthesis of a New Element with Atomic Number Z=117". Physical Review Letters. Quyển 104 số 14. tr. 142502. Bibcode:2010PhRvL.104n2502O. doi:10.1103/PhysRevLett.104.142502. PMID 20481935.
- ^ United States Environmental Protection Agency. "Technetium-99". epa.gov. Truy cập ngày 26 tháng 2 năm 2013.
- ^ Harvard–Smithsonian Center for Astrophysics. "Origins of Heavy Elements". cfa.harvard.edu. Truy cập ngày 26 tháng 2 năm 2013.
- ^ "Atomic Number and Mass Numbers". ndt-ed.org. Bản gốc lưu trữ ngày 12 tháng 2 năm 2014. Truy cập ngày 17 tháng 2 năm 2013.
- ^ periodic.lanl.gov. "Periodic Table of Elements: LANL Carbon". Los Alamos National Laboratory.
- ^ Katsuya Yamada. "Atomic mass, isotopes, and mass number" (PDF). Los Angeles Pierce College. Bản gốc (PDF) lưu trữ ngày 11 tháng 1 năm 2014.
- ^ "Pure element". European Nuclear Society. Bản gốc lưu trữ ngày 13 tháng 6 năm 2017. Truy cập ngày 13 tháng 8 năm 2013.
- ^ Wilford, J.N. (ngày 14 tháng 1 năm 1992). "Hubble Observations Bring Some Surprises". The New York Times.
- ^ Wright, E. L. (ngày 12 tháng 9 năm 2004). "Big Bang Nucleosynthesis". UCLA, Division of Astronomy. Truy cập ngày 22 tháng 2 năm 2007.
- ^ Wallerstein, George; Iben, Icko; Parker, Peter; và đồng nghiệp (1999). "Synthesis of the elements in stars: forty years of progress" (PDF). Reviews of Modern Physics. Quyển 69 số 4. tr. 995–1084. Bibcode:1997RvMP...69..995W. doi:10.1103/RevModPhys.69.995. Bản gốc (PDF) lưu trữ ngày 28 tháng 9 năm 2006.
- ^ Earnshaw, A.; Greenwood, N. (1997). Chemistry of the Elements (ấn bản thứ 2). Butterworth-Heinemann.
- ^ Croswell, Ken (1996). Alchemy of the Heavens. Anchor. ISBN 978-0-385-47214-2.
- ^ Plato (2008) [c. 360 BC]. Timaeus. Forgotten Books. tr. 45. ISBN 978-1-60620-018-6.
- ^ Hillar, M. (2004). "The Problem of the Soul in Aristotle's De anima". NASA/WMAP. Bản gốc lưu trữ ngày 9 tháng 9 năm 2006. Truy cập ngày 10 tháng 8 năm 2006.
- ^ Partington, J. R. (1937). A Short History of Chemistry. New York: Dover Publications. ISBN 978-0-486-65977-0.
- ^ a b Boyle, R. (1661). The Sceptical Chymist. London. ISBN 978-0-922802-90-6.
- ^ Lavoisier, A. L. (1790). Elements of chemistry translated by Robert Kerr. Edinburgh. tr. 175–6. ISBN 978-0-415-17914-0.
- ^ Transactinide-2. www.kernchemie.de
- ^ Carey, G.W. (1914). The Chemistry of Human Life. Los Angeles. ISBN 978-0-7661-2840-8.
{{Chú thích sách}}: Quản lý CS1: địa điểm thiếu nhà xuất bản (liên kết) - ^ "IUPAC Announces Start of the Name Approval Process for the Element of Atomic Number 112" (PDF). IUPAC. ngày 20 tháng 7 năm 2009. Truy cập ngày 27 tháng 8 năm 2009.
- ^ "IUPAC (International Union of Pure and Applied Chemistry): Element 112 is Named Copernicium". IUPAC. ngày 20 tháng 2 năm 2010. Bản gốc lưu trữ ngày 24 tháng 2 năm 2010.
- ^ Oganessian, Yu. Ts.; Utyonkov, V.; Lobanov, Yu.; và đồng nghiệp (2006). "Evidence for Dark Matter" (PDF). Physical Review C. Quyển 74 số 4. tr. 044602. Bibcode:2006PhRvC..74d4602O. doi:10.1103/PhysRevC.74.044602. ISSN 0556-2813. Bản gốc (PDF) lưu trữ ngày 13 tháng 2 năm 2021. Truy cập ngày 9 tháng 9 năm 2021.
- ^ Greiner, W. "Recommendations" (PDF). 31st meeting, PAC for Nuclear Physics. Joint Institute for Nuclear Research. Bản gốc (PDF) lưu trữ ngày 14 tháng 4 năm 2010.
- ^ Staff (ngày 30 tháng 11 năm 2016). "IUPAC Announces the Names of the Elements 113, 115, 117, and 118". IUPAC. Truy cập ngày 1 tháng 12 năm 2016.
- ^ St. Fleur, Nicholas (ngày 1 tháng 12 năm 2016). "Four New Names Officially Added to the Periodic Table of Elements". The New York Times. Truy cập ngày 1 tháng 12 năm 2016.
Liên kết ngoài
[sửa | sửa mã nguồn]- Elementymology & Elements Multidict word history and language dictionary
Thông tin về hóa học
[sửa | sửa mã nguồn]- ChemGlobe Lưu trữ ngày 6 tháng 2 năm 2005 tại Wayback Machine
- Phòng thí nghiệm quốc gia LosAlamos Lưu trữ ngày 19 tháng 1 năm 2005 tại Wayback Machine
- Nguyên tố hóa học
 GIẢM
48%
GIẢM
48%
 GIẢM
47%
GIẢM
47%
 GIẢM
-50%
GIẢM
-50%
 GIẢM
40%
GIẢM
40%
![[Tập hiểu sâu]: Vì sao Bạn luôn KHÔNG ỔN?](https://images.spiderum.com/sp-images/f5ab2630336211eea9e7ef608f381f46.png) GIẢM
12%
GIẢM
12%






![[Xiao] Tứ Kiếp - Genshin Impact](https://i.ytimg.com/vi/lNCvBV9HplM/maxresdefault.jpg)


![[Review] Socrates thân yêu – Cửu Nguyệt Hy](https://tugovo.files.wordpress.com/2017/11/15110914_1366937743319473_6853806389128835474_o.jpg)