Acetylen
| Acetylen | |
|---|---|
 Acetylen | |
Acetylen | |
 Mô hình lấp đầy của phân tử acetylen | |
| Tên hệ thống | Ethyne[1] |
| Nhận dạng | |
| Số CAS | |
| PubChem | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| Số RTECS | AO9600000 |
| Ảnh Jmol-3D | ảnh |
| SMILES | đầy đủ
|
| InChI | đầy đủ
|
| Tham chiếu Beilstein | 906677 |
| Tham chiếu Gmelin | 210 |
| UNII | |
| Thuộc tính | |
| Bề ngoài | Khí không màu |
| Mùi | Không mùi |
| Khối lượng riêng | 1,1772 g/L = 1,1772 kg/m3 (0 °C, 101.3 kPa)[2] |
| Điểm nóng chảy | Lỗi Lua trong Mô_đun:Convert tại dòng 328: attempt to compare number with nil. Điểm ba tại 1.27 atm |
| Điểm sôi | |
| Điều kiện thăng hoa | −84 °C; −119 °F; 189 K (1 atm) |
| Độ hòa tan trong nước | tan khá tốt |
| Độ hòa tan | tan khá tốt trong alcohol tan tốt trong acetone, benzen |
| Áp suất hơi | 44.2 atm (20 °C)[3] |
| Độ axit (pKa) | 25[4] |
| MagSus | −20.8×10−6 cm3/mol [5] |
| Độ dẫn nhiệt | 21.4 mW·m−1·K−1 (300 K) [5] |
| Acid liên hợp | Ethynium |
| Cấu trúc | |
| Hình dạng phân tử | Tuyến tính |
| Nhiệt hóa học | |
| Entropy mol tiêu chuẩn S | 200.927 J·mol−1·K−1 |
| Nhiệt dung | 44.036 J·mol−1·K−1 |
| Các nguy hiểm | |
| NFPA 704 |
|
| Giới hạn nổ | 2.5–100% |
| PEL | none[3] |
| REL | C 2500 ppm (2662 mg/m3)[3] |
| IDLH | N.D.[3] |
| Ký hiệu GHS |   |
| Báo hiệu GHS | Danger |
| Chỉ dẫn nguy hiểm GHS | H220, H336 |
| Chỉ dẫn phòng ngừa GHS | P202, P210, P233, P261, P271, P304, P312, P340, P377, P381, P403, P405, P501 |
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |
Acetylen (bắt nguồn từ từ tiếng Pháp acétylène /asetilɛn/),[6] tên hệ thống: ethyn) là hợp chất hóa học có công thức hóa học là C
2H
2 hay H−C≡C−H. Đây là hydrocarbon và là alkyn đơn giản nhất.[7] Acetylen là một khí không màu, sử dụng rộng rãi làm nhiên liệu và tiền chất tổng hợp các hợp chất. Acetylen không ổn định ở dạng nguyên chất, do đó thường được xử lý trong dung dịch.[8] Acetylen nguyên chất không có mùi, nhưng trong sản phẩm hóa chất thương mại thì thường có mùi đặc trưng do tạp chất divinyl sulfide và phosphin.[8][9]
Với tính chất của một alkyn, acetylen là hợp chất không bão hòa (không no) vì hai nguyên tử carbon liên kết với nhau bằng liên kết ba. Liên kết ba carbon-carbon khiến cấu trúc bốn nguyên tử trong phân tử này cùng nằm trên một đường thẳng, góc liên kết CCH là 180°.[10]
Khám phá
[sửa | sửa mã nguồn]Edmund Davy là người đầu tiên phát hiện acetylen vào năm 1836. Ông là người sử dụng acetylen trong "bộ chế hòa khí hydro".[11][12] Đây là một phát hiện tình cờ khi ông cố gắng điều chế kim loại kali. Ông nung kali carbonat với carbon ở nhiệt độ rất cao, tạo ra sản phẩm phụ là mà ngày nay gọi là kali carbide, (K2C2), cho chất này phản ứng với nước để giải phóng khí mới. Năm 1860, nhà hóa học người Pháp Marcellin Berthelot tiếp tục phát hiện ra khí này và đặt tên là acétylène.[13] Công thức thực nghiệm của Berthelot cho acetylen là C4H2, đặt tên là " quadricarbure d'hydrogène " (hydro quadricarbide). Sở dĩ công thức trên không chính xác vì nhiều nhà hóa học thời đó đã sử dụng sai nguyên tử khối của carbon (6 thay vì 12).[14] Berthelot điều chế loại khí này bằng cách cho hơi của các hợp chất hữu cơ (methanol, ethanol, v.v.) đi qua ống nung nóng và thu sản phẩm. Ông cũng phát hiện ra rằng acetylen hình thành bằng cách phóng điện qua hỗn hợp khí cyanide và hydro. Acetylen còn được điều chế trực tiếp bằng cách cho hydro đi qua giữa các cực của hồ quang carbon.[15][16]
Điều chế
[sửa | sửa mã nguồn]Acetylen không tồn tại trong tự nhiên.
Acetylen sản xuất tại Trung Quốc chủ yếu dựa vào quá trình đốt cháy một phần khí tự nhiên.[17]
Đốt cháy một phần hydrocarbon
[sửa | sửa mã nguồn]Từ thập niên 1950, acetylen chủ yếu được sản xuất bằng cách đốt cháy một phần khí methan.[18][19] C
2H
2 là sản phẩm phụ được thu hồi trong quá trình sản xuất ethylen bằng cách cracking hydrocarbon. Khoảng 400 000 tấn được sản xuất bằng phương pháp này vào năm 1983.[8] C
2H
2 trong ethylen là sản phẩm phụ không mong muốn vì tính chất dễ nổ và khả năng hủy hoại chất chất xúc tác Ziegler–Natta. C
2H
2 được hydro hóa chọn lọc thành ethylen, thường sử dụng chất xúc tác là Pd–Ag.[20]
Đốt cháy một phần khí methan tạo ra acetylen theo phương trình phản ứng:
3 CH
4 + 3 O
2 → C
2H
2 + CO + 5 H
2O
Dehydro alkan
[sửa | sửa mã nguồn]Các alkan nặng nhất trong dầu mỏ và khí tự nhiên bị "bẻ gãy" thành các phân tử nhẹ hơn và dehydro ở nhiệt độ cao:
C
2H
6 → C
2H
2 + 2 H
2
2 CH
4→ C
2H+
2 3 H
2
Phản ứng cuối cùng này được thực hiện trong quá trình phân hủy yếm khí khí methan bằng plasma vi sóng (microwave plasma). Ưu điểm của công nghệ này là không phát thải CO
2 và hydro là một sản phẩm thứ cấp.[21]
Phương pháp hóa carbon
[sửa | sửa mã nguồn]Cho đến những năm 1950, khi dầu thay thế than đá làm nguồn khử carbon chủ yếu, acetylen (và các cấu phần thơm có trong nhựa than đá) là nguồn hóa chất hữu cơ chính trong ngành hóa chất. C
2H
2 được điều chế bằng cách thủy phân calci carbide, một phản ứng được Friedrich Wöhler phát hiện vào năm 1862[22] và vẫn quen thuộc với sinh viên:
CaC
2 + 2 H
2O → Ca(OH)
2 + C
2H
2
Sản xuất calci carbide cần nhiệt độ cao, ~ 2000 °C trong lò hồ quang điện. Ở Mỹ, quá trình này là một phần quan trọng của cuộc cách mạng hóa học cuối thế kỷ 19 nhờ dự án thủy điện khổng lồ ở thác Niagara.[23]
Liên kết
[sửa | sửa mã nguồn]Theo lý thuyết liên kết hóa trị, trong mỗi nguyên tử carbon, orbital 2s lai hóa với một orbital 2p tạo thành orbital lai hóa sp. Hai orbital 2p còn lại không bị lai hóa. Hai đầu của hai orbital lai hóa sp xen phủ lên nhau để tạo thành liên kết σ mạnh giữa các nguyên tử carbon, trong khi ở hai đầu còn lại, các nguyên tử hydro cũng liên kết bằng liên kết σ. Hai quỹ đạo 2p tạo thành một cặp liên kết π yếu hơn.[24]
Vì acetylen là một phân tử đối xứng tuyến tính nên cấu trúc phân tử có nhóm điểm (point group) D∞h.
Tính chất vật lý
[sửa | sửa mã nguồn]Dạng vật chất
[sửa | sửa mã nguồn]Ở áp suất khí quyển, acetylen không thể tồn tại ở thể lỏng và không có điểm nóng chảy. Điểm ba trên biểu đồ pha tương ứng với điểm nóng chảy (−80,8 °C) ở áp suất tối thiểu mà acetylen thể lỏng có thể tồn tại (1,27 atm). Ở nhiệt độ dưới điểm ba, acetylen thể rắn có thể chuyển trực tiếp thành thể hơi (khí) bằng cách thăng hoa. Điểm thăng hoa ở áp suất khí quyển là −84,0 °C.[25]
Các tính chất khác
[sửa | sửa mã nguồn]Ở nhiệt độ phòng, độ hòa tan của acetylen trong aceton là 27,9 g/kg. Hòa tan C
2H
2 cùng một lượng dimethylformamide (DMF), độ hòa tan là 51 g. Ở 20,26 bar, độ hòa tan aceton và DMF lần lượt là 689,0 và 628,0 g. Những dung môi này được sử dụng trong bình chứa khí điều áp.[26]
Các ứng dụng
[sửa | sửa mã nguồn]Hàn xì
[sửa | sửa mã nguồn]Khoảng 20% acetylen được ngành công nghiệp khí công nghiệp cung cấp để hàn và cắt, dưới dạng oxyacetylen. Đốt cháy acetylen với oxy tạo ra ngọn lửa tỏa ra nhiệt độ lên tới trên 3.600 K (3.330 °C; 6.020 °F), giải phóng 11,8 kJ /g. Oxyacetylene là loại khí đốt thông thường có nhiệt độ nóng nhất.[27] Acetylene là ngọn lửa hóa học tự nhiên nóng thứ ba sau dicyanoacetylen, nhiệt độ có thể lên tới 5.260 K (4.990 °C; 9.010 °F) và cyanogen, nhiệt độ có thể lên tới 4.798 K (4.525 °C; 8.177 °F). Hàn oxy-acetylen là một quá trình hàn phổ biến trong những thập kỷ trước. Sự phát triển và ưu điểm của quy trình hàn hồ quang đã làm cho hàn oxy-acetylen gần như "tuyệt chủng". Việc sử dụng acetylen để hàn đã giảm đáng kể. Mặt khác, thiết bị hàn oxy-acetylen khá linh hoạt - không chỉ vì mỏ hàn được ưa chuộng hơn cho một số loại hàn sắt hoặc thép (như trong một số ứng dụng nghệ thuật nhất định), mà còn bởi vì nó dễ dàng hàn đồng, hàn đồng thau., gia nhiệt kim loại (để ủ hoặc tôi, uốn hoặc tạo hình), nới lỏng các đai ốc và bu lông bị ăn mòn, và còn nhiều ứng dụng khác. Hàn oxyacetylene được sử dụng ở những nơi không có điện. Để sử dụng trong hàn và cắt, áp suất phải được kiểm soát nhờ bộ điều chỉnh, vì trên 15 psi (100 kPa), nếu chịu một sóng xung kích (ví dụ: do cháy ngược), acetylen phân hủy nhanh chóng thành hydro và carbon.[28]

Hóa chất
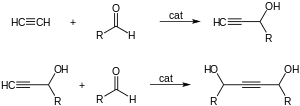
[sửa | sửa mã nguồn]Một trong những ứng dụng hóa học chính là ethynyl hóa formaldehyde.[29] Acetylen tác dụng với aldehyde và keton tạo thành rượu α-ethynyl:
Phản ứng tạo ra butynediol, với sản phẩm phụ là rượu propargyl. Chất xúc tác là đồng(I) acetylide.[30][31]
Ngoài quá trình ethynyl hóa, acetylen còn phản ứng với carbon monoxide, phản ứng tạo ra acid acrylic hoặc các ester acrylic. Phản ứng cần xúc tác kim loại. Các dẫn xuất này tạo thành các sản phẩm như sợi acrylic, thủy tinh, sơn, nhựa và polyme. Ngoại trừ Trung Quốc, việc sử dụng acetylen làm nguyên liệu hóa học đã giảm 70% từ năm 1965 đến năm 2007 do những cân nhắc về chi phí và môi trường.[32]
Ứng dụng
[sửa | sửa mã nguồn]Năm 1881, nhà hóa học người Nga Mikhail Kucherov[33] mô tả phản ứng hydrat hóa acetylen thành acetaldehyde bằng cách sử dụng các chất xúc tác như thủy ngân(II) bromide. Trước khi có quy trình Wacker, phản ứng này được tiến hành ở quy mô công nghiệp.[34]
Phản ứng trùng hợp acetylen với xúc tác Ziegler–Natta tạo ra polyacetylen. Polyacetylene là một chuỗi các trung tâm CH và các liên kết đơn và đôi xen kẽ. Đây là một trong những chất bán dẫn hữu cơ được phát hiện đầu tiên. Phản ứng của polymer với iod tạo ra vật liệu dẫn điện cao. Mặc dù những vật liệu như vậy không hữu ích nhưng những khám phá này đã dẫn tới sự phát triển của chất bán dẫn hữu cơ. Giải Nobel Hóa học năm 2000 được trao tặng cho Alan J. Heeger, Alan G MacDiarmid và Hideki Shirakawa về đề tài này.
Vào thập niên 1920, acetylen nguyên chất đã được sử dụng thực nghiệm làm thuốc gây mê dạng hít.[35]
Acetylene đôi khi được sử dụng để thấm carbon (nghĩa là làm cứng) thép khi lượng lớn thép có trong lò nung.[36]
Acetylene được sử dụng để làm bay hơi carbon trong quá trình xác định niên đại bằng carbon phóng xạ. Vật liệu carbon trong mẫu khảo cổ được xử lý bằng kim loại lithi trong lò nghiên cứu chuyên dụng nhỏ để tạo thành lithi carbide (còn gọi là lithi acetylide). carbide sau đó có thể phản ứng với nước để tạo thành khí acetylen, sau đó dẫn khí vào máy quang phổ khối nhằm đo tỷ lệ đồng vị của carbon-14 và carbon-12.[37]
Quá trình đốt cháy acetylen tạo ra ánh sáng mạnh, sáng. Sự phổ biến của đèn caride thúc đẩy quá trình thương mại hóa acetylen vào đầu thế kỷ 20. Vào thời điểm này, acetylen được sử dụng trong ngọn hải đăng ven biển,[38] đèn đường,[39] và ô tô[40] và đèn pha khai thác mỏ đeo trên mũ bảo hộ lao động.[41] Trong hầu hết các ứng dụng này, việc đốt trực tiếp acetylen gây nguy cơ hỏa hoạn. Do vậy mà acetylen bị thay thế bằng đèn sợi đốt, sau này là đèn LED công suất thấp nhưng mà độ sáng cao. Tuy nhiên, đèn acetylen vẫn được sử dụng hạn chế ở các khu vực xa xôi hoặc khó tiếp cận và ở các quốc gia có hệ thống điện lưới còn hạn chế.[41]
Xuất hiện trong tự nhiên
[sửa | sửa mã nguồn]Liên kết ba C≡C giàu năng lượng và khả năng hòa tan khá cao của acetylen trong nước làm cho nó trở thành cơ chất thích hợp cho vi khuẩn.[42] Đã tìm thấy một số vi khuẩn sống bằng acetylen. Enzym acetylene hydratase xúc tác quá trình hydrat hóa acetylen để tạo ra acetaldehyde:[43]
- C
2H
2 + H
2O → CH
3CHO
Acetylene là một hóa chất khá phổ biến trong vũ trụ, thường gắn liền với bầu khí quyển của các hành tinh khí khổng lồ.[44] Acetylen được phát hiện là tồn tại trên Enceladus, một vệ tinh của Sao Thổ. Acetylen tự nhiên được cho là hình thành từ quá trình phân hủy xúc tác các hydrocarbon chuỗi dài ở nhiệt độ 1.700 K (1.430 °C; 2.600 °F) trở lên. Vì nhiệt độ như vậy rất khó xảy ra trên một thiên thể nhỏ ở xa như vậy nên phát hiện này có khả năng gợi ý về các phản ứng xúc tác bên trong vệ tinh đó, khiến thiên thể này trở thành địa điểm đầy hứa hẹn để tìm kiếm hóa học tiền sinh học.[45][46]
Phản ứng
[sửa | sửa mã nguồn]Phản ứng vinyl hóa
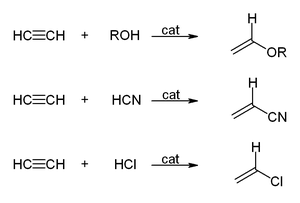
[sửa | sửa mã nguồn]Trong các phản ứng vinyl hóa, các hợp chất H−X phản ứng cộng với liên kết ba. Alcohol và phenol phản ứng với acetylen tạo ra vinyl ether. Thiol tạo ra vinyl thioether. Vinylpyrrolidone và vinylcarbazole sản xuất trong công nghiệp bằng cách vinyl hóa 2-pyrrolidone và carbazole.[29]
Quá trình hydrat hóa acetylen là phản ứng vinyl hóa, nhưng vinyl alcohol tạo thành sẽ đồng phân hóa thành acetaldehyde. Phản ứng được xúc tác bởi muối thủy ngân. Phản ứng này từng là công nghệ chủ đạo để sản xuất acetaldehyde, nhưng đã bị quy trình Wacker thay thế. Quy trình Wacker tạo ra acetaldehyde bằng cách oxy hóa ethylen, một nguyên liệu rẻ tiền hơn. Quá trình hydrochlor hóa biến đổi acetylen thành vinyl chloride cũng được thay thế bằng quá trình oxychlor hóa ethylene.
Vinyl acetat được sử dụng thay cho acetylen cho một số phản ứng vinyl hóa, đứng hơn là phản ứng transvinyl hóa.[47] Các ester của vinyl acetat đã được sử dụng để tổng hợp vinyl format.
Hóa học cơ-kim
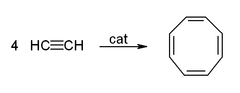
[sửa | sửa mã nguồn]Acetylene và các dẫn xuất của nó (2-butyn, diphenylacetylen, v.v.) tạo thành phức chất với các kim loại chuyển tiếp (phức alkyn kim loại chuyển tiếp). Liên kết của acetylen với kim loại có phần giống với liên kết của phức ethylen. Các phức chất này là chất trung gian trong nhiều phản ứng xúc tác như trimer hóa alkyn thành benzen, phản ứng tetramer hóa thành cyclooctatetraen, và carbonyl hóa thành hydroquinone:[48]
- Fe(CO)
5 + 4 C
2H
2 + 2 H
2O → 2 C
6H
4(OH)
2 + FeCO
3 trong điều kiện 50–80 °C, 20–25 atm.
Acetylide kim loại có dạng L
nM−C
2R, ví dụ: đồng(I) acetylide và bạc acetylide.[49]
Phản ứng acid-base
[sửa | sửa mã nguồn]Acetylen có pKa bằng 25, acetylen bị deproton hóa bởi một siêu base để tạo thành acetylide:[49]
Nhiều loại chất hóa học cơ kim[50] và hợp chất vô cơ[51] đều có tính chất trên.
Hydro hóa
[sửa | sửa mã nguồn]Acetylen có thể được hydro hóa một phần thành ethylen, cung cấp nguyên liệu cho nhiều loại nhựa polyethylen. Halogen phản ứng cộng vào liên kết ba.
An toàn và xử lý
[sửa | sửa mã nguồn]Acetylen không độc hại, nhưng khi được tạo ra từ calci carbide thì một số tạp chất độc hại như phosphine và arsine khiến hỗn hợp khí có mùi giống tỏi. Acetylen cũng rất dễ cháy, giống như hầu hết các hydrocarbon nhẹ, do đó nó được sử dụng trong hàn. Hầu hết các bộ điều chỉnh và đồng hồ đo áp suất trên thiết bị đều báo cáo áp suất đo được và giới hạn an toàn đối với acetylen là 101 kPagage, hoặc 15 psig.[52][53] Do đó, lưu trữ aceton hoặc dimethylformamide (DMF) dưới dạng hòa tan,[53][54][55] để trong bình chứa khí chứa lớp làm đầy có tính chất xốp (Agamassan), giúp vận chuyển và sử dụng an toàn. Nên sử dụng bình chứa acetylen ở vị trí bình thẳng đứng để tránh lấy phải aceton trong quá trình sử dụng.[56]
Đồng xúc tác cho quá trình phân hủy acetylen và do đó acetylen không được vận chuyển trong ống đồng.[57]
Bình chứa khí phải được bảo quản ở khu vực cách ly với các chất oxy hóa để tránh phản ứng trầm trọng hơn trong trường hợp cháy/rò rỉ.[53][58] Không nên cất giữ bình khí chứa acetylen trong không gian chật hẹp, được đậy kín, trong nhà để xe và tòa nhà để tránh trường hợp nếu có rò rỉ ngoài ý muốn thì có nguy cơ cháy nổ cao.[53]
Tham khảo
[sửa | sửa mã nguồn]- ^ Acyclic Hydrocarbons. Rule A-3. Unsaturated Compounds and Univalent Radicals Lưu trữ 10 tháng 10 năm 2000 tại Wayback Machine, IUPAC Nomenclature of Organic Chemistry
- ^ Thông tin từ Acetylene trong GESTIS-Stoffdatenbank của IFA
- ^ a b c d “NIOSH Pocket Guide to Chemical Hazards #0008”. Viện An toàn và Sức khỏe Nghề nghiệp Quốc gia Hoa Kỳ (NIOSH).
- ^ “Acetylene – Gas Encyclopedia Air Liquide”. Air Liquide. Lưu trữ bản gốc ngày 4 tháng 5 năm 2022. Truy cập ngày 27 tháng 9 năm 2018.
- ^ a b CRC handbook of chemistry and physics: a ready-reference book of chemical and physical data. William M. Haynes, David R. Lide, Thomas J. Bruno (ấn bản thứ 97). Boca Raton, Florida. 2016. ISBN 978-1-4987-5428-6. OCLC 930681942. Lưu trữ bản gốc ngày 4 tháng 5 năm 2022. Truy cập ngày 4 tháng 5 năm 2022.Quản lý CS1: khác (liên kết)
- ^ Đặng Thái Minh, "Dictionnaire vietnamien - français. Les mots vietnamiens d'origine française", Synergies Pays riverains du Mékong, n° spécial, năm 2011. ISSN: 2107-6758. Trang 49.
- ^ R. H. Petrucci; W. S. Harwood; F. G. Herring (2002). General Chemistry (ấn bản thứ 8). Prentice-Hall. tr. 1072.
- ^ a b c Pässler, Peter; Hefner, Werner; Buckl, Klaus; Meinass, Helmut; Meiswinkel, Andreas; Wernicke, Hans-Jürgen; Ebersberg, Günter; Müller, Richard; Bässler, Jürgen; Behringer, Hartmut; Mayer, Dieter (2008). “Acetylene Chemistry”. Bách khoa toàn thư Ullmann về Hóa chất công nghiệp. Weinheim: Wiley-VCH. doi:10.1002/14356007.a01_097.pub3. ISBN 978-3527306732.
- ^ Compressed Gas Association (1995) Material Safety and Data Sheet – Acetylene Lưu trữ 11 tháng 7 năm 2012 tại Wayback Machine
- ^ Whitten K. W., Gailey K. D. and Davis R. E. General Chemistry (4th ed., Saunders College Publishing 1992), pp. 328–329, 1046. ISBN 0-03-072373-6
- ^ Edmund Davy (August 1836) "Notice of a new gaseous bicarburet of hydrogen" Lưu trữ 6 tháng 5 năm 2016 tại Wayback Machine, Report of the Sixth Meeting of the British Association for the Advancement of Science ..., 5: 62–63.
- ^ Miller, S. A. (1965). Acetylene: Its Properties, Manufacture and Uses. 1. Academic Press Inc. Bản gốc lưu trữ ngày 15 tháng 4 năm 2021. Truy cập ngày 16 tháng 7 năm 2021.
- ^ Bertholet (1860) "Note sur une nouvelle série de composés organiques, le quadricarbure d'hydrogène et ses dérivés" Lưu trữ 13 tháng 7 năm 2015 tại Wayback Machine (Note on a new series of organic compounds, tetra-carbon hydride and its derivatives), Comptes rendus, series 3, 50: 805–808.
- ^ Ihde, Aaron J. (1961). “The Karlsruhe Congress: A centennial retrospective”. Journal of Chemical Education. 38 (2): 83. Bibcode:1961JChEd..38...83I. doi:10.1021/ed038p83. Lưu trữ bản gốc ngày 30 tháng 12 năm 2021. Truy cập ngày 29 tháng 12 năm 2021.
Atomic weights of 6 and 12 were both in use for carbon.
- ^ Berthelot (1862) "Synthèse de l'acétylène par la combinaison directe du carbone avec l'hydrogène" Lưu trữ 14 tháng 8 năm 2020 tại Wayback Machine (Synthesis of acetylene by the direct combination of carbon with hydrogen), Comptes rendus, series 3, 54: 640–644.
- ^ Acetylene Lưu trữ 28 tháng 1 năm 2012 tại Wayback Machine.
- ^ Gannon, Richard E. (2000). “Acetylene from Hydrocarbons”. Kirk‐Othmer Encyclopedia of Chemical Technology. doi:10.1002/0471238961.0103052007011414.a01. ISBN 9780471484943.
- ^ Habil, Phil; Sachsse, Hans (1954). “Herstellung von Acetylen durch unvollständige Verbrennung von Kohlenwasserstoffen mit Sauerstoff (Production of acetylene by incomplete combustion of hydrocarbons with oxygen)”. Chemie Ingenieur Technik. 26 (5): 245–253. doi:10.1002/cite.330260502.
- ^ Habil, Phil; Bartholoméa, E. (1954). “Probleme großtechnischer Anlagen zur Erzeugung von Acetylen nach dem Sauerstoff-Verfahren (Problems of large-scale plants for the production of acetylene by the oxygen method)”. Chemie Ingenieur Technik. 26 (5): 253–258. doi:10.1002/cite.330260503.
- ^ Acetylene: How Products are Made Lưu trữ 20 tháng 1 năm 2007 tại Wayback Machine
- ^ “How it Works”. Transform Materials (bằng tiếng Anh). Truy cập ngày 21 tháng 7 năm 2023.
- ^ Wohler (1862) "Bildung des Acetylens durch Kohlenstoffcalcium" Lưu trữ 12 tháng 5 năm 2016 tại Wayback Machine (Formation of actylene by calcium carbide), Annalen der Chemie und Pharmacie, 124: 220.
- ^ Freeman, Horace (1919). “Manufacture of Cyanamide”. The Chemical News and the Journal of Physical Science. 117: 232. Lưu trữ bản gốc ngày 15 tháng 4 năm 2021. Truy cập ngày 23 tháng 12 năm 2013.
- ^ Organic Chemistry 7th ed. by J. McMurry, Thomson 2008
- ^ Handbook of Chemistry and Physics (60th ed., CRC Press 1979–80), p.
- ^ Harreus, Albrecht Ludwig; Backes, R.; Eichler, J.-O.; Feuerhake, R.; Jäkel, C.; Mahn, U.; Pinkos, R.; Vogelsang"2-Pyrrolidone, R. Bách khoa toàn thư Ullmann về Hóa chất công nghiệp. Weinheim: Wiley-VCH. doi:10.1002/14356007.a22_457.pub2. ISBN 978-3-527-30673-2.
- ^ “Acetylene”. Products and Supply > Fuel Gases. Linde. Lưu trữ bản gốc ngày 12 tháng 1 năm 2018. Truy cập ngày 30 tháng 11 năm 2013.
- ^ ESAB Oxy-acetylene welding handbook – Acetylene properties Lưu trữ 10 tháng 5 năm 2020 tại Wayback Machine.
- ^ a b Pässler, Peter; Hefner, Werner; Buckl, Klaus; Meinass, Helmut; Meiswinkel, Andreas; Wernicke, Hans-Jürgen; Ebersberg, Günter; Müller, Richard; Bässler. “Acetylene Chemistry”. Bách khoa toàn thư Ullmann về Hóa chất công nghiệp. Weinheim: Wiley-VCH. doi:10.1002/14356007.a01_097.pub3. ISBN 978-3-527-30673-2. Lỗi chú thích: Thẻ
<ref>không hợp lệ: tên “Ullmann” được định rõ nhiều lần, mỗi lần có nội dung khác - ^ Gräfje, Heinz; Körnig, Wolfgang; Weitz, Hans-Martin; Reiß, Wolfgang; Steffan, Guido; Diehl, Herbert; Bosche, Horst; Schneider, Kurt; Kieczka, Heinz (15 tháng 6 năm 2000), Wiley-VCH Verlag GmbH & Co. KGaA (biên tập), “Butanediols, Butenediol, and Butynediol”, Ullmann's Encyclopedia of Industrial Chemistry (bằng tiếng Anh), Weinheim, Germany: Wiley-VCH Verlag GmbH & Co. KGaA, tr. a04_455, doi:10.1002/14356007.a04_455, ISBN 978-3-527-30673-2, Bản gốc lưu trữ ngày 19 tháng 3 năm 2022, truy cập ngày 3 tháng 3 năm 2022
- ^ Falbe, Jürgen; Bahrmann, Helmut; Lipps, Wolfgang; Mayer, Dieter (15 tháng 6 năm 2000), Wiley-VCH Verlag GmbH & Co. KGaA (biên tập), “Alcohols, Aliphatic”, Ullmann's Encyclopedia of Industrial Chemistry (bằng tiếng Anh), Weinheim, Germany: Wiley-VCH Verlag GmbH & Co. KGaA, tr. a01_279, doi:10.1002/14356007.a01_279, ISBN 978-3-527-30673-2, Bản gốc lưu trữ ngày 9 tháng 3 năm 2022, truy cập ngày 3 tháng 3 năm 2022
- ^ Takashi Ohara; Takahisa Sato; Noboru Shimizu; Günter Prescher; Helmut Schwind; Otto Weiberg; Klaus Marten; Helmut Greim (2003). “Acrylic Acid and Derivatives”. Ullmann's Encyclopedia of Industrial Chemistry: 7. doi:10.1002/14356007.a01_161.pub2. ISBN 3527306730.
- ^ Kutscheroff, M. (1881). “Ueber eine neue Methode direkter Addition von Wasser (Hydratation) an die Kohlenwasserstoffe der Acetylenreihe”. Berichte der Deutschen Chemischen Gesellschaft. 14: 1540–1542. doi:10.1002/cber.188101401320. Lưu trữ bản gốc ngày 2 tháng 12 năm 2020. Truy cập ngày 9 tháng 9 năm 2019.
- ^ Dmitry A. Ponomarev; Sergey M. Shevchenko (2007). “Hydration of Acetylene: A 125th Anniversary” (PDF). J. Chem. Educ. 84 (10): 1725. Bibcode:2007JChEd..84.1725P. doi:10.1021/ed084p1725. Lưu trữ (PDF) bản gốc ngày 11 tháng 6 năm 2011. Truy cập ngày 18 tháng 2 năm 2009.
- ^ “Acetylene in medicine”. Encyclopaedia Britannica (bằng tiếng Anh). 1 (ấn bản thứ 14). 1930. tr. 119.
- ^ “Acetylene”. Products and Services. BOC. Bản gốc lưu trữ ngày 17 tháng 5 năm 2006.
- ^ Geyh, Mebus (1990). “Radiocarbon dating problems using acetylene as counting gas”. Radiocarbon. 32 (3): 321–324. doi:10.2458/azu_js_rc.32.1278. Lưu trữ bản gốc ngày 26 tháng 12 năm 2013. Truy cập ngày 26 tháng 12 năm 2013.
- ^ “Lighthouse Lamps Through Time by Thomas Tag | US Lighthouse Society”. uslhs.org (bằng tiếng Anh). Lưu trữ bản gốc ngày 25 tháng 2 năm 2017. Truy cập ngày 24 tháng 2 năm 2017.
- ^ Myers, Richard L. (2007). The 100 Most Important Chemical Compounds: A Reference Guide (bằng tiếng Anh). ABC-CLIO. ISBN 978-0-313-33758-1. Bản gốc lưu trữ ngày 17 tháng 6 năm 2016. Truy cập ngày 21 tháng 11 năm 2015.
- ^ Grainger, D., (2001).
- ^ a b Thorpe, Dave (2005). Carbide Light: The Last Flame in American Mines. Bergamot Publishing. ISBN 978-0976090526.
- ^ Akob, Denise (tháng 8 năm 2018). “Acetylenotrophy: a hidden but ubiquitous microbial metabolism?”. FEMS Microbiology Ecology. 94 (8). doi:10.1093/femsec/fiy103. PMC 7190893. PMID 29933435. Truy cập ngày 28 tháng 7 năm 2022.
- ^ ten Brink, Felix (2014). “Chapter 2. Living on acetylene. A Primordial Energy Source”. Trong Peter M. H. Kroneck and Martha E. Sosa Torres (biên tập). The Metal-Driven Biogeochemistry of Gaseous Compounds in the Environment. Metal Ions in Life Sciences. 14. Springer. tr. 15–35. doi:10.1007/978-94-017-9269-1_2. PMID 25416389.
- ^ “Precursor to Proteins and DNA found in Stellar Disk” (Thông cáo báo chí). W. M. Keck Observatory. 20 tháng 12 năm 2005. Bản gốc lưu trữ ngày 23 tháng 2 năm 2007.
- ^ Emily Lakdawalla (17 tháng 3 năm 2006). “LPSC: Wednesday afternoon: Cassini at Enceladus”. The Planetary Society. Bản gốc lưu trữ ngày 20 tháng 2 năm 2012.
- ^ John Spencer; David Grinspoon (25 tháng 1 năm 2007). “Planetary science: Inside Enceladus”. Nature. 445 (7126): 376–377. Bibcode:2007Natur.445..376S. doi:10.1038/445376b. PMID 17251967.
- ^ Manchand, Percy S. (2001). “Vinyl Acetate”. Encyclopedia of Reagents for Organic Synthesis. doi:10.1002/047084289X.rv008. ISBN 0471936235.
- ^ Reppe, Walter; Kutepow, N; Magin, A (1969). “Cyclization of Acetylenic Compounds”. Angewandte Chemie International Edition in English. 8 (10): 727–733. doi:10.1002/anie.196907271.
- ^ a b Viehe, Heinz Günter (1969). Chemistry of Acetylenes (ấn bản thứ 1). New York: Marcel Dekker, inc. tr. 170–179 & 225–241. ISBN 978-0824716752. Lỗi chú thích: Thẻ
<ref>không hợp lệ: tên “Viehe” được định rõ nhiều lần, mỗi lần có nội dung khác - ^ Midland, M. M.; McLoughlin, J. I.; Werley, Ralph T. (Jr.) (1990). “Preparation and Use of Lithium Acetylide: 1-Methyl-2-ethynyl-endo-3,3-dimethyl-2-norbornanol”. Organic Syntheses. 68: 14. doi:10.15227/orgsyn.068.0014.
- ^ Coffman, Donald D. (1940). “Dimethylethhynylcarbinol”. Organic Syntheses. 40: 20. doi:10.15227/orgsyn.020.0040.
- ^ “Acetylene Specification”. CFC StarTec LLC. Lưu trữ bản gốc ngày 11 tháng 3 năm 2014. Truy cập ngày 2 tháng 5 năm 2012.
- ^ a b c d “law.resource.org CGA g-1 2009 (incorporated by reference)” (PDF). Lưu trữ (PDF) bản gốc ngày 10 tháng 10 năm 2016. Truy cập ngày 30 tháng 11 năm 2016. Lỗi chú thích: Thẻ
<ref>không hợp lệ: tên “:0” được định rõ nhiều lần, mỗi lần có nội dung khác - ^ Downie, N. A. (1997). Industrial Gases. London; New York: Blackie Academic & Professional. ISBN 978-0-7514-0352-7.
- ^ Korzun, Mikołaj (1986). 1000 słów o materiałach wybuchowych i wybuchu. Warszawa: Wydawnictwo Ministerstwa Obrony Narodowej. ISBN 83-11-07044-X. OCLC 69535236.
- ^ “EIGA Code of Practice: Acetylene” (PDF). Bản gốc (PDF) lưu trữ ngày 1 tháng 12 năm 2016. Truy cập ngày 30 tháng 11 năm 2016.
- ^ Daniel_Sarachick (16 tháng 10 năm 2003). “ACETYLENE SAFETY ALERT” (PDF). Office of Environmental Health & Safety (EHS). Lưu trữ (PDF) bản gốc ngày 13 tháng 7 năm 2018. Truy cập ngày 27 tháng 9 năm 2018.
- ^ “OSHA 29 CFR 1926.350 Gas Welding and cutting”. Lưu trữ bản gốc ngày 1 tháng 12 năm 2016. Truy cập ngày 30 tháng 11 năm 2016.
Liên kết ngoài
[sửa | sửa mã nguồn]- Acetylene Production Plant and Detailed Process Lưu trữ 11 tháng 4 năm 2015 tại Wayback Machine
- Acetylene at Chemistry Comes Alive!
- Acetylene, the Principles of Its Generation and Use tại Dự án Gutenberg
- Movie explaining acetylene formation from calcium carbide and the explosive limits forming fire hazards
- Calcium Carbide & Acetylene at The Periodic Table of Videos (University of Nottingham)
- CDC – NIOSH Pocket Guide to Chemical Hazards – Acetylene
 GIẢM
31%
GIẢM
31%
 GIẢM
21%
GIẢM
21%
 GIẢM
15%
GIẢM
15%
 GIẢM
3%
GIẢM
3%
 GIẢM
50%
GIẢM
50%
 GIẢM
17%
GIẢM
17%