Streptozotocine
| streptozotocine | |
| |
| Identification | |
|---|---|
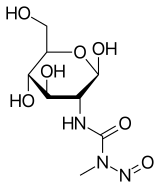
| Nom UICPA | 2-désoxy-2-({[méthyl(nitroso)amino]carbonyl}amino)-β-D-glucopyranose |
| Synonymes |
streptozocine |
| No CAS | |
| Code ATC | L01 |
| DrugBank | DB00428 |
| PubChem | 29327 |
| ChEBI | 9288 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C8H15N3O7 |
| Masse molaire[1] | 265,220 6 ± 0,010 2 g/mol C 36,23 %, H 5,7 %, N 15,84 %, O 42,23 %, 265,221 g/mol |
| Données pharmacocinétiques | |
| Biodisponibilité | 17 - 25% (100% si IV) |
| Métabolisme | Hépatique, rénal |
| Demi-vie d’élim. | 35 à 40 minutes |
| Considérations thérapeutiques | |
| Classe thérapeutique | Antinéoplasique |
| Voie d’administration | IV |
| Grossesse | Contre-indiqué |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
La streptozotocine (STZ) est une molécule de la famille des nitro-urées, utilisée comme agent alkylant à visée néoplasique ou comme antibiotique. Elle est particulièrement toxique envers les cellules β des îlots de Langerhans chez les mammifères, elle est à ce titre indiquée dans le traitement des insulinomes et employée en recherche médicale dans l’induction chimique du diabète de type 1 chez des modèles animaux.
Historique
[modifier | modifier le code]La streptozotocine a été identifiée vers la fin des années 1950 en tant qu’antibiotique naturel à large spectre[2],[3],[4], isolée à partir d’une souche de la bactérie Gram-positive Streptomyces achromogenes var. streptozoticus[5]. Des scientifiques du laboratoire pharmaceutique Upjohn, basé à Kalamazoo (Michigan) et maintenant partie de Pfizer, ont découvert en 1958-1959 cette molécule dans un échantillon de sol contaminé par la bactérie et prélevé dans « un sol sablonneux, non cultivé, dans une région de prairie » à Blue Rapids (Kansas).[source insuffisante] Un brevet leur a été accordé en . En 2019, Balskus et al. ont apporté de nouveaux éléments de compréhension de la biosynthèse de la streptozotocine, en mettant en évidence le cluster de gènes responsable de la production chez Streptomyces achromogenes et en découvrant la fonction de la SznF, une métallo-enzyme à fer non-héminique, qui permet de former la liaison N-N dans le pharmacophore N-nitroso-urée par réarrangement oxydatif[6].
Durant les années 1960, les scientifiques ont constaté que la streptozotocine était sélectivement cytotoxique envers les cellules β des îlots de Langerhans, ce qui permet d’entraver l’insulinosécrétion. Ces découvertes ont suscité un intérêt concernant l’utilisation de la molécule dans des modèles animaux du diabète sucré[7],[8] et dans le traitement des cancers des cellules β[9]. Dans les années 1970, le National Cancer Institute entreprend des études sur l’indication de la streptozotocine en tant qu’anticancéreux. Le médicament obtient une autorisation de mise sur le marchée par la FDA en 1982, sous le nom commercial Zanosar. Le brevet ayant expiré depuis longtemps, de nombreuses formulations génériques sont aujourd'hui disponibles.
Mécanismes d'action
[modifier | modifier le code]La structure de la streptozotocine correspond à un 2-désoxy-D-glucose substitué en C2 par un groupe N-nitroso-N-méthylurée[10]. Elle entre dans les cellules grâce au transporteur GLUT1, mais n’est pas reconnue par les autres transporteurs de glucose. Cela explique sa toxicité relative envers les cellules β, puisque celles-ci ont un niveau d’expression de GLUT1 très élevé. La streptozotocine peut également pénétrer dans les hépatocytes. Comme d'autres agents alkylants, elle exerce sa toxicité en causant la méthylation des bases puriques de l'ADN, causant des adduits covalents, et peut même entraîner des ruptures des brins d'ADN[11]. La streptozotocine est également une molécule donneuse de NO qui génère des ROS, contribuant à la déterioration de l'ADN. Tous ces dommages à l'ADN stimulent la voie de réparation PARP, ayant pour conséquences une augmentation de l'ATP et une diminution du FADPH,H+ ; la contribution de ces dernières est certainement plus importante dans la diabétogenèse que la génotoxicité seule[12].
Injectée à des doses faibles et répétées (20 à 40 mg/kg) chez le rat ou la souris, la streptozotocine diminue l'insulinosécrétion sans pour autant entraîner la mort cellulaire, ce qui permet de mimer chez l'animal l’insulite (en) rencontrée dans le diabète de type 1. Le déclenchement de la réaction inflammatoire des îlots β est rendu possible par la production de cytokines pro-inflammatoires et par le recrutement de macrophages — alors que la pathologie humaine est associée à un recrutement de lymphocytes T.
À des doses élevées (100 à 200 mg/kg) et en injection unique, la streptozotocine entraîne la destruction rapide des cellules β. La régénération spontanée des cellules est toutefois possible, ce qui limite la pertinence du modèle murin.
Utilisations
[modifier | modifier le code]La streptozotocine est titulaire d’une AMM dans le traitement des adénocarcinomes métastatiques des îlots de Langerhans et des tumeurs carcinoïdes métastasées[13]. En raison de sa forte toxicité rénale, hépatique et hématologique, et de son efficacité mitigée, son utilisation est généralement limitée aux patients pour lesquels le cancer ne peut être réséqué par chirurgie ou après échec d’une chirurgie. Chez les patients traités, la streptozotocine permet de réduire la taille de la tumeur et d’atténuer les symptômes, en particulier l'hypoglycémie secondaire à la sécrétion excessive d'insuline par les insulinomes[14]. La posologie classique est de 500 mg/m2 par administration, réalisée en IV, à la fréquence d’une injection par jour pendant 5 jours. Les cures doivent être espacées de 6 semaines[13].
Comme l'alloxane, la streptozotocine est utilisée depuis longtemps dans la recherche scientifique pour créer des modèles animaux de diabète sucré et d'insulite à faible dose, et d'hyperglycémie à forte dose, notamment chez les souris et les rats[15] mais aussi chez les lapins ou les poissons. Les modèles de diabète chimiquement induits sont peu coûteux, relativement simples d'exécution et rapides, en comparaison aux modèles génétiques (souris NOD (en)). Ces modèles sont potentiellement intéressants pour tester de nouvelles formulations de l'insuline, pour étudier la transplantation d'îlots pancréatiques (en), ou pour tester des médicaments empêchant la mort des cellules β. Toutefois, les modèles d'induction chimique ont de nombreux inconvénients : les agents chimiques peuvent être toxiques pour d'autres organes, les résultats sont variables selon la lignée, le sexe et le régime alimentaire, il n'existe pas de protocole standardisé de préparation et d'administration des produits chimiques, et le diabète induit est généralement moins stable et potentiellement réversible.
La streptozotocine a également été employée pour modéliser la perte de mémoire dans la maladie d'Alzheimer chez la souris[16].
Voir aussi
[modifier | modifier le code]Notes et références
[modifier | modifier le code]- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ J. J. Vavra, C. Deboer, A. Dietz et L. J. Hanka, « Streptozotocin, a new antibacterial antibiotic », Antibiotics Annual, vol. 7, 1959-1960, p. 230–235 (ISSN 0570-3131, PMID 13841501, lire en ligne, consulté le )
- ↑ W. T. Sokolski, J. J. Vavra et L. J. Hanka, « Assay methods and antibacterial studies on streptozotocin », Antibiotics Annual, vol. 7, 1959-1960, p. 241–246 (ISSN 0570-3131, PMID 13832573, lire en ligne, consulté le )
- ↑ C. Lewis et A. R. Barbiers, « Streptozotocin, a new antibiotic. In vitro and in vivo evaluation », Antibiotics Annual, vol. 7, 1959-1960, p. 247–254 (ISSN 0570-3131, PMID 14416496, lire en ligne, consulté le )
- ↑ F. Reusser, « Mode of action of streptozotocin », Journal of Bacteriology, vol. 105, no 2, , p. 580–588 (ISSN 0021-9193, PMID 4993338, PMCID PMC248427, lire en ligne, consulté le )
- ↑ Tai L. Ng, Roman Rohac, Andrew J. Mitchell et Amie K. Boal, « An N-nitrosating metalloenzyme constructs the pharmacophore of streptozotocin », Nature, vol. 566, no 7742, , p. 94–99 (ISSN 1476-4687, PMID 30728519, PMCID 6369591, DOI 10.1038/s41586-019-0894-z, lire en ligne, consulté le )
- ↑ K. R. Mansford et L. Opie, « Comparison of metabolic abnormalities in diabetes mellitus induced by streptozotocin or by alloxan », Lancet (London, England), vol. 1, no 7544, , p. 670–671 (ISSN 0140-6736, PMID 4170654, DOI 10.1016/s0140-6736(68)92103-x, lire en ligne, consulté le )
- ↑ C. C. Rerup, « Drugs producing diabetes through damage of the insulin secreting cells », Pharmacological Reviews, vol. 22, no 4, , p. 485–518 (ISSN 0031-6997, PMID 4921840, lire en ligne, consulté le )
- ↑ I. M. Murray-Lyon, A. L. Eddleston, R. Williams et M. Brown, « Treatment of multiple-hormone-producing malignant islet-cell tumour with streptozotocin », Lancet (London, England), vol. 2, no 7574, , p. 895–898 (ISSN 0140-6736, PMID 4176152, DOI 10.1016/s0140-6736(68)91058-1, lire en ligne, consulté le )
- ↑ Ross R. Herr, Heinz K. Jahnke et Alexander D. Argoudelis, « Structure of streptozotocin », Journal of the American Chemical Society, vol. 89, no 18, , p. 4808–4809 (ISSN 0002-7863, DOI 10.1021/ja00994a053, lire en ligne, consulté le )
- ↑ (en) Alejandro D Bolzán et Martha S Bianchi, « Genotoxicity of Streptozotocin », Mutation Research/Reviews in Mutation Research, vol. 512, nos 2-3, , p. 121–134 (DOI 10.1016/S1383-5742(02)00044-3, lire en ligne, consulté le )
- ↑ T. Szkudelski, « The mechanism of alloxan and streptozotocin action in B cells of the rat pancreas », Physiological Research, vol. 50, no 6, , p. 537–546 (ISSN 0862-8408, PMID 11829314, lire en ligne, consulté le )
- Agence nationale de sécurité du médicament (ANSM), « RCP de la streptozotocine », (consulté le )
- ↑ R. Brentjens et L. Saltz, « Islet cell tumors of the pancreas: the medical oncologist's perspective », The Surgical Clinics of North America, vol. 81, no 3, , p. 527–542 (ISSN 0039-6109, PMID 11459269, DOI 10.1016/s0039-6109(05)70141-9, lire en ligne, consulté le )
- ↑ (en) Kenneth K. Wu et Youming Huan, « Streptozotocin‐Induced Diabetic Models in Mice and Rats », Current Protocols in Pharmacology, vol. 40, no 1, (ISSN 1934-8282 et 1934-8290, DOI 10.1002/0471141755.ph0547s40, lire en ligne, consulté le )
- ↑ Michael Costa, Jamile Bernardi, Tiago Fiuza et Lidiane Costa, « N-acetylcysteine protects memory decline induced by streptozotocin in mice », Chemico-Biological Interactions, vol. 253, , p. 10–17 (ISSN 1872-7786, PMID 27087133, DOI 10.1016/j.cbi.2016.04.026, lire en ligne, consulté le )