Cementit
| Thép |
|---|
 |
| Pha |
| Tổ chức tế vi |
|
| Các loại thép |
|
| Vật liệu khác trên cơ sở sắt |
Cementit hay còn gọi sắt carbide, carbide sắt (tiếng Anh: cementite, iron carbide) là một hợp chất liên kim loại của sắt và cacbon, chính xác hơn là một carbide kim loại chuyển tiếp trung gian với công thức Fe3C. Theo trọng lượng, nó chứa 6,67% cacbon và 93,33% sắt. Nó có cấu trúc tinh thể trực thoi.[1] Nó là vật liệu cứng và giòn,[1] thường được phân loại như là một dạng gốm trong dạng tinh khiết của nó, và thường được tìm thấy như là một thành phần hợp thành quan trọng trong luyện kim đen. Trong khi carbide sắt có mặt trong phần lớn các loại gang thép,[2] thì nó cũng được sản xuất như là một loại nguyên liệu trong quy trình carbide sắt, một quy trình thuộc về họ các công nghệ sản xuất sắt thép thay thế.
Luyện kim
[sửa | sửa mã nguồn]
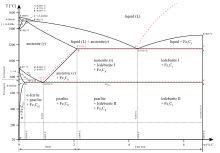
Trong hệ sắt–cacbon (như trong các loại thép cacbon thường và gang) nó là thành phần hợp thành phổ biến do ferrit chỉ có thể chứa tối đa không quá 0,02% trọng lượng là cacbon không kết hợp.[3] Vì thế, trong thép cacbon và gang được làm nguội chậm thì một phần cacbon nằm dưới dạng cementit.[4] Cementit hình thành trực tiếp từ khối kim loại nóng chảy trong trường hợp của gang trắng. Trong thép cacbon, cementit kết tủa từ austenit do austenit biến đổi thành ferrit khi làm nguội chậm, hoặc từ martensit trong quá trình ram. Hỗn hợp trộn nhuyễn với ferrit, một sản phẩm khác của austenit, hình thành một cấu trúc dạng phiến gọi là pearlit.
Trong khi cementit là không ổn định nhiệt động lực, cuối cùng chuyển hóa thành ferrit và graphit ở các mức nhiệt độ cao hơn, thì nó lại không phân hủy khi nung nóng ở nhiệt độ dưới eutectoid (723 °C) trên biểu đồ pha sắt-cacbon nửa ổn định.
Dạng tinh khiết
[sửa | sửa mã nguồn]Cementit thay đổi từ sắt từ sang thuận từ ở điểm Curie của nó, khoảng 480 K.[5]

Sắt carbide tự nhiên (chứa một lượng nhỏ niken và coban) có trong các vẫn thạch sắt và được gọi là cohenit theo tên nhà khoáng vật học người Đức Emil Cohen, người đầu tiên mô tả nó.[6][7] Do cacbon là một trong các thành phần tạo hợp kim nhẹ ở hàm lượng thấp của các lõi hành tinh kim loại, nên các tính chất trong điều kiện áp suất cao/nhiệt độ cao của cementit (Fe3C) như là đại diện đơn giản cho cohenit cũng được nghiên cứu về mặt thực nghiệm. Các số liệu trong hình bên chỉ ra trạng thái chịu nén ở nhiệt độ phòng.
Các carbide sắt khác
[sửa | sửa mã nguồn]Có các dạng khác của sắt carbide nửa ổn định đã được nhận dạng trong thép ram và trong quy trình Fischer-Tropsch công nghiệp. Chúng bao gồm epsilon carbide (ε-carbide), bó chặt lục phương Fe2-3C, kết tủa trong thép cacbon thường với hàm lượng cacbon > 0,2%, ram ở 100-200 °C. Ε-carbide phi lượng pháp hòa tan ở nhiệt độ trên 200 °C, khi các carbide Hägg và cementit bắt đầu hình thành. Carbide Hägg, Fe5C2 đơn nghiêng, kết tủa trong thép công cụ làm cứng được ram ở nhiệt độ khoảng 200-300 °C.[8][9][10] Đặc trưng hóa các carbide sắt khác biệt là nhiệm vụ không đơn giản, và thông thường nhiễu xạ tia X được bổ sung bởi phổ học Mössbauer.[11][12]
Tham khảo
[sửa | sửa mã nguồn]- ^ a b Smith, William F.; Hashemi, Javad (2006). Foundations of Materials Science and Engineering (ấn bản thứ 4). McGraw-Hill. tr. 363. ISBN 0-07-295358-6.
- ^ Durand-Charre, Madeleine (2004). Microstructure of Steels and Cast Irons. Springer. ISBN 978-3-642-05897-4.
- ^ “Cementite Formation from Hematite–Graphite Mixture by Simultaneous Thermal–Mechanical Activation”. Metallurgical and Materials Transactions B.
- ^ Smith, William F.; Hashemi, Javad (2006). Foundations of Materials Science and Engineering (ấn bản thứ 4). McGraw-Hill. tr. 366-372. ISBN 0-07-295358-6.
- ^ S.W.J. Smith; W. White; S.G. Barker (1911). “The Magnetic Transition Temperature of Cementite”. Proc. Phys. Soc. London. 24 (1): 62–69. doi:10.1088/1478-7814/24/1/310.
- ^ Vagn F. Buchwald, Handbook of Iron Meteorites, Nhà in Đại học California. 1975.
- ^ L.J.E. Cohen Nature of Carbides of Iron, Bulletin 631 US Bureau of Mines
- ^ Bauer-Grosse, E.; Frantz, C.; Le Caer, G.; Heiman, N. (tháng 6 năm 1981). “Formation of Fe7C3 and Fe5C2 type metastable carbides during the crystallization of an amorphous Fe75C25 alloy”. Journal of Non-Crystalline Solids. 44 (2–3): 277–286. doi:10.1016/0022-3093(81)90030-2.
- ^ Gunnar Hägg, Z. Krist., Vol. 89, p. 92-94, 1934.
- ^ Smith, William F. (1981). Structure and properties of engineering alloys. New York: McGraw-Hill. tr. 61–62. ISBN 0-07-0585601.
- ^ Mössbauer Spectroscopy of Iron Carbides: From Prediction to Experimental Confirmation
- ^ Le Caer, G.; Dubois, J. M.; Pijolat, M.; Perrichon, V.; Bussiere, P. (tháng 11 năm 1982). “Characterization by Moessbauer spectroscopy of iron carbides formed by Fischer-Tropsch synthesis”. The Journal of Physical Chemistry. 86 (24): 4799–4808. doi:10.1021/j100221a030.
Liên kết ngoài
[sửa | sửa mã nguồn]- Cấu trúc tinh thể của cementit tại NRL
- Cấu trúc tinh thể của cementit, Đại học Cambridge
- Alternative Ironmaking Technologies Lưu trữ 2016-03-04 tại Wayback Machine
- Hallstedt, Bengt; Djurovic, Dejan; von Appen, Jörg; Dronskowski, Richard; Dick, Alexey; Körmann, Fritz; Hickel, Tilmann; Neugebauer, Jörg (tháng 3 năm 2010). “Thermodynamic properties of cementite (Fe3C)”. Calphad. 34 (1): 129–133. doi:10.1016/j.calphad.2010.01.004.
- Ester Esna du Plessis. The Crystal Structures of Iron Carbides, Luận án tiến sĩ, 185 trang, Đại học Johannesburg, 2006
 GIẢM
30%
GIẢM
30%
 GIẢM
17%
GIẢM
17%
 GIẢM
20%
GIẢM
20%
 GIẢM
18%
GIẢM
18%
 GIẢM
11%
GIẢM
11%




