Ytri(III) sulfat
| Ytri(III) sulfat | |
|---|---|
 | |
| Danh pháp IUPAC | Yttrium(III) sulfate |
| Tên khác | Yttrium sesquisulfate Yttrium sulfate |
| Nhận dạng | |
| Số CAS | |
| PubChem | |
| Ảnh Jmol-3D | ảnh |
| SMILES | đầy đủ
|
| InChI | đầy đủ
|
| ChemSpider | |
| Thuộc tính | |
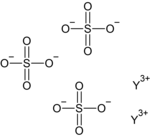
| Công thức phân tử | Y2(SO4)3 |
| Khối lượng mol | 610.1 |
| Bề ngoài | Chất rắn màu trắng |
| Điểm nóng chảy | |
| Điểm sôi | |
| Độ hòa tan trong nước | Hòa tan |
| Các nguy hiểm | |
| Ký hiệu GHS |  |
| Báo hiệu GHS | Warning |
| Chỉ dẫn nguy hiểm GHS | H315, H319, H335 |
| Chỉ dẫn phòng ngừa GHS | P261, P264, P271, P280, P302+P352, P304+P340, P305+P351+P338, P312, P321, P332+P313, P337+P313, P362, P403+P233, P405, P501 |
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |
Ytri(III) sulfat là một hợp chất vô cơ có công thức hóa học là Y2(SO4)3. Dạng phổ biến nhất là anhydrat và octahydrat.
Phản ứng
[sửa | sửa mã nguồn]Ytri(III) sulfat có thể phản ứng để tạo ra các muối kép như MY(SO4)2[1][2][3] và M3Y(SO4)3[4][5][6]:
- Y2(SO4)3 + M2SO4 → 2MY(SO4)2
- Y2(SO4)3 + 3M2SO4 → 2M3Y(SO4)3 (M = kim loại kiềm)
Tổng hợp
[sửa | sửa mã nguồn]Ytri(III) sulfat có thể được tổng hợp bằng cách sử dụng oxide, hydroxide hoặc muối carbonat tương ứng.
- 2Y(OH)3 + 3H2SO4 → Y2(SO4)3 + 6H2O[7]
Tham khảo
[sửa | sửa mã nguồn]- ^ Prokof'ev, M. V.; Pokrovskii, A. N.; Kovba, L. M. Double sulfates of rubidium and rare earth elements. Zhurnal Neorganicheskoi Khimii, 1979. 24(8): 2114-2121. ISSN 0044-457X
- ^ Baldanova, D. D.; Evdokimov, A. A.; Petrov, K. I.; Kondratov, O. I.; Fomichev, V. V. X-ray phase analysis and vibrational spectroscopic study of cesium lanthanide sulfate molybdates (in Russian). Deposited Doc.(Report) 1983, 1316-1384. CAN102:71568
- ^ Degtiarev, P.A.; Pokrovskii, A.N.; Kovba, L.M.; Korytnaia, F.M. (1977). “Investigation of double sulfates of potassium and rare earth elements with composition KRE(SO4)2”. Journal of Solid State Chemistry. 22 (4): 419–422. doi:10.1016/0022-4596(77)90019-6. ISSN 0022-4596.
- ^ Prokof'ev, M. V.; Pokrovskii, A. N.; Kovba, L. M. X-ray diffraction study of rubidium lanthanide sulfates (Rb3Ln(SO4)3). Vestnik Moskovskogo Universiteta, Seriya 2: Khimiya, 1979. 20 (6): 571-574. ISSN 0579-9384
- ^ Samartsev, B. G.; Pokrovskii, A. N.; Kovba, L. M. X-ray diffraction study of double sulfates, isostructural with cesium neodymium sulfate (Cs3Nd(SO4)3) (in Russian). Vestnik Moskovskogo Universiteta, Seriya 2: Khimiya, 1980. 21 (2): 190-192. ISSN 0579-9384
- ^ Kudin, O. V.; Efremov, V. A.; Pokrovskii, A. N.; Degtyarev, P. A.; Trunov, V. K. Synthesis and x-ray diffraction study of double sulfates K3R(SO4)3. Zhurnal Neorganicheskoi Khimii, 1977. 22 (1): 95-97
- ^ “Y(OH)3 + H2SO4 = Y2(SO4)3 + H2O | Chemical reaction and equation”. Lưu trữ bản gốc ngày 15 tháng 3 năm 2018. Truy cập ngày 23 tháng 1 năm 2022.
Chúng tôi bán
 GIẢM
17%
GIẢM
17%
50.000 ₫
60.000 ₫
 GIẢM
32%
GIẢM
32%
297.000 ₫
435.000 ₫
 GIẢM
-50%
GIẢM
-50%
736.000 ₫
492.000 ₫
 GIẢM
17%
GIẢM
17%
50.000 ₫
60.000 ₫
 GIẢM
27%
GIẢM
27%
132.000 ₫
182.000 ₫




