Techneti(VI) fluoride
| Tecneti(VI) fluoride | |
|---|---|
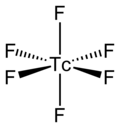 Cấu trúc của tecneti(VI) fluoride | |
| Tên khác | Tecneti hexafluoride |
| Nhận dạng | |
| Số CAS | |
| Thuộc tính | |
| Công thức phân tử | TcF6 |
| Khối lượng mol | 211,8974 g/mol |
| Bề ngoài | tinh thể màu vàng kim loại[1] |
| Khối lượng riêng | 3,58 g/cm³ (-140 ℃), rắn[2] |
| Điểm nóng chảy | 37,4 °C (310,5 K; 99,3 °F)[1] |
| Điểm sôi | 55,3 °C (328,4 K; 131,5 °F)[1] |
| Độ hòa tan trong nước | phản ứng |
| Các nguy hiểm | |
| Nguy hiểm chính | tính phản ứng cao, phóng xạ |
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |
Tecneti(VI) fluoride, còn được gọi với tên gọi khác là tecneti hexafluoride là một hợp chất vô cơ màu vàng, với thành phần chính gồm hai nguyên tố là tecneti và fluoride, với công thức hóa học được quy định là TcF6. Hợp chất này có điểm nóng chảy thấp, lần đầu tiên được phát hiện vào năm 1961.[3] Trong hợp chất này, tecneti có trạng thái oxy hóa là +6, trạng thái oxy hóa cao nhất tìm thấy trong các hợp chất tecneti halide. Hợp chất tương tự khác là tecneti(VI) chloride, TcCl6. Về mặt này, tecneti khác với rheni, tạo thành heptafluoride, ReF7.[4] Tecneti hexafluoride tồn tại như một tạp chất trong urani(VI) fluoride, vì tecneti là một sản phẩm phân hạch của urani.
Điều chế
[sửa | sửa mã nguồn]Tecneti(VI) fluoride được điều chế bằng cách gia nhiệt kim loại tecneti với khí flo dư, ở nhiệt độ 400 ℃.[3]
- Tc + 3F2 → TcF6
Tổng quan hợp chất
[sửa | sửa mã nguồn]Tecneti(VI) fluoride là một chất rắn màu vàng kim loại ở nhiệt độ phòng. Điểm nóng chảy của nó là 37,4 ℃ và điểm sôi của nó là 55,3 ℃.[1]
Hóa tính
[sửa | sửa mã nguồn]TcF6 phản ứng với dung dịch kiềm chloride trong dung dịch iod pentafluoride (IF5) để hình thành hexaflorotecnetat.[5][6]
TcF6 không tỷ lệ về phản ứng thủy phân với dung dịch NaOH, và kết quả tạo thành kết tủa đen, là hợp chất tecneti(IV) oxit TcO2.[3] Trong dung dịch hydro fluoride, TcF6 phản ứng với hydrazini fluoride để tạo ra hợp chất có công thức phân tử là N2H6TcF6 hoặc N2H6(TcF6)2.[7]
Tham khảo
[sửa | sửa mã nguồn]- ^ a b c d CRC Handbook of Chemistry and Physics, 90th Edition, CRC Press, Boca Raton, Florida, 2009, ISBN 978-1-4200-9084-0, Section 4, Physical Constants of Inorganic Compounds, tr. 4-93.
- ^ Drews, T.; Supeł, J.; Hagenbach, A.; Seppelt, K. (2006). “Solid State Molecular Structures of Transition Metal Hexafluorides”. Inorganic Chemistry. 45 (9): 3782–3788. doi:10.1021/ic052029f. PMID 16634614.
- ^ a b c Selig, H.; Chernick, C.L.; Malm, J.G. (1961). “The Preparation and Properties of TcF6”. Journal of Inorganic and Nuclear Chemistry. 19 (3–4): 377–381.
- ^ Greenwood, Norman N.; Earnshaw, A. (1997), Chemistry of the Elements (ấn bản thứ 2), Oxford: Butterworth-Heinemann, ISBN 0-7506-3365-4
- ^ Edwards, A. J.; Hugill, D.; Peacock, R. D. (1963). “New Fluorine Compounds of Technetium”. Nature. 200 (4907): 672. Bibcode:1963Natur.200..672E. doi:10.1038/200672a0.
- ^ D. Hugill & R. D. Peacock (1966). “Some quinquevalent fluorotechnetates”. Journal of the Chemical Society A: 1339–1341. doi:10.1039/J19660001339.
- ^ Frlec B; Selig H & Hyman H.H (1967). “Hydrazinium(+2) Hexafluorometalates(IV) and -(V) in the 4d and 5d Transition Series”. Inorganic Chemistry. 6 (10): 1775–1783. doi:10.1021/ic50056a004.
 GIẢM
20%
GIẢM
20%
 GIẢM
18%
GIẢM
18%
![[Review Sách] Đọc vị tâm trí](https://down-bs-vn.img.susercontent.com/sg-11134201-7qvdk-libws1cgh4ks57.webp) GIẢM
3%
GIẢM
3%
 GIẢM
49%
GIẢM
49%
 GIẢM
33%
GIẢM
33%
 GIẢM
48%
GIẢM
48%